一氧化铅
一氧化铅是一种无机化合物,化学式为PbO。它以两种同质异形体存在:具有四方晶系结构的密陀僧和斜方晶系结构的黄丹。一氧化铅在现代主要用于铅基工业玻璃和工业陶瓷,包括计算机组件。它为两性氧化物。[3]
| 一氧化铅 | |
|---|---|

| |
| |
| IUPAC名 Lead(II) oxide | |
| 别名 | 密陀僧 黄丹 铅黄 |
| 识别 | |
| CAS号 | 1317-36-8 |
| PubChem | 14827 |
| ChemSpider | 140169 |
| SMILES |
|
| UN编号 | 3288 2291 3077 |
| ChEBI | 81045 |
| RTECS | OG1750000 |
| KEGG | C17379 |
| 性质 | |
| 化学式 | PbO |
| 摩尔质量 | 223.20 g·mol⁻¹ |
| 外观 | 红色或黄色粉末 |
| 密度 | 9.53 g/cm3 |
| 熔点 | 888 °C(1161 K) |
| 沸点 | 1477 °C(1750 K) |
| 溶解性(水) | 0.017 g/L[1] |
| 溶解性 | 不溶于稀碱,醇 溶于浓碱 溶于盐酸,氯化铵 |
| 磁化率 | 4.20×10−5 cm3/mol |
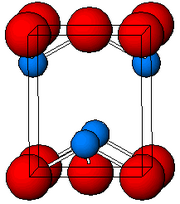
| 结构 | |
| 晶体结构 | 四方,tP4 |
| 空间群 | P4/nmm, No. 129 |
| 危险性 | |
GHS危险性符号  
| |
| GHS提示词 | 危险 |
| H-术语 | H302, H332, H351, H360, H362, H373, H410 |
| P-术语 | P201, P202, P260, P261, P263, P264, P270, P271, P273, P281, P301+312, P304+312, P304+340, P308+313 |
| NFPA 704 | |
| 闪点 | 不可燃 |
| 致死量或浓度: | |
LDLo(最低)
|
1400 mg/kg(犬,经口)[2] |
| 相关物质 | |
| 其他阴离子 | 硫化铅 硒化铅 碲化铅 |
| 其他阳离子 | 一氧化碳 一氧化硅 一氧化锗 一氧化锡 |
| 相关铅的氧化物 | 四氧化三铅 二氧化铅 |
| 相关化学品 | 三氧化二铊 三氧化二铋 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
一氧化铅在唐代由波斯传入中国,其俗称“密陀僧”是波斯语古称“مُرداسنگ”(Mardasang,波斯文又作 مُردارسنگ 或 مُرداسنج)的音译,当时用作治疗痔疮的药物。[4]
制备
编辑一氧化铅可以通过在大约600 °C(1,100 °F)的空气中加热铅来制备。在此温度下,它也是空气中其他铅氧化物分解的最终产物:[5]
- 2 Pb(NO
3)
2 → 2 PbO + 4 NO
2 + O
2 - PbCO
3 → PbO + CO
2
一氧化铅作为将铅矿石精炼成金属铅的中间产品。通常的铅矿石是方铅矿(PbS2)。在大约1,000 °C(1,800 °F)的温度下,硫化物将转化为氧化物:[6]
- 2 PbS + 3 O
2 → 2 PbO + 2 SO
2
反应
编辑一氧化铅的红色和黄色形式与焓的微小变化有关:
- PbO(红色) → PbO(黄色) ΔH = 1.6 kJ/mol
PbO 是两性的,这意味着它会与酸和碱反应。与酸作用会通过氧簇的中介作用形成Pb2+
的盐,如[Pb
6O(OH)
6]4+
。与强碱作用则会溶解形成亚铅酸盐:[8]
- PbO + H
2O + OH−
→ [Pb(OH)
3]−
用途
编辑铅玻璃中的铅通常是一氧化铅,而一氧化铅广泛用于制造玻璃。根据玻璃的不同,在玻璃中使用一氧化铅的好处可以是增加玻璃的折射率、降低玻璃的粘度、增加玻璃的电阻率和增加玻璃的吸收X射线能力中的一种或多种。在工业陶瓷(以及玻璃)中添加一氧化铅可以使材料提高居里温度,以此在磁性和电学上更具惰性。[9]历史上,一氧化铅也广泛用于家用陶瓷的釉料,但现在不再广泛使用。其他不太占主导地位的应用包括橡胶的硫化以及某些颜料和油漆的生产。[3]一氧化铅可用于阴极射线管玻璃,以阻挡X射线发射,但主要用于颈部和漏斗,因为它在面板中使用时会导致变色。故面板优选氧化锶和氧化钡。[10]
铅的消耗以及一氧化铅的加工与汽车数量相关,因为它仍然是汽车中铅酸电池的关键组成部分。[11]
少见或过时的用途
编辑一氧化铅与甘油的混合物凝固成坚硬的防水水泥,用于连接水族箱的平板玻璃侧面和底部,也曾用于密封窗框中的玻璃面板。它是含铅油漆的成分。
一氧化铅是传统皮蛋的制作原料之一,但由于健康问题已被逐渐取代。
参考文献
编辑- ^ Blei(II)-oxid[失效链接]. Merck
- ^ Lead compounds (as Pb). Immediately Dangerous to Life and Health Concentrations (IDLH). National Institute for Occupational Safety and Health (NIOSH).
- ^ 3.0 3.1 Carr, Dodd S., Lead Compounds, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, 2005, doi:10.1002/14356007.a15_249
- ^ (美)爱德华·谢弗.《唐代的外来文明》
- ^ Greenwood, Norman Neill; Earnshaw, Alan. Chemistry of the elements. 2016: 382–387. ISBN 978-0-7506-3365-9. OCLC 1040112384 (英语).
- ^ Abdel-Rehim, A. M. Thermal and XRD analysis of Egyptian galena. Journal of Thermal Analysis and Calorimetry. 2006, 86 (2): 393–401. S2CID 96393940. doi:10.1007/s10973-005-6785-6.
- ^ 朱文祥. 无机化合物制备手册. 化学工业出版社,2006. pp581-582. 【XIV-368】氧化铅 [Lead(II) oxide]
- ^ Holleman, Arnold Frederik; Wiberg, Egon, Wiberg, Nils , 编, Inorganic Chemistry, 由Eagleson, Mary; Brewer, William翻译, San Diego/Berlin: Academic Press/De Gruyter, 2001, ISBN 0-12-352651-5[页码请求]
- ^ Chapter 9, "Lead Compounds", in the book Ceramic and Glass Materials: Structure, Properties and Processing (页面存档备份,存于互联网档案馆), published by Springer, year 2008.
- ^ Compton, Kenneth. Image Performance in CRT Displays. SPIE Press. 5 December 2003 [2022-06-03]. ISBN 9780819441447. (原始内容存档于2022-06-03) –通过Google Books.
- ^ Sutherland, Charles A.; Milner, Edward F.; Kerby, Robert C.; Teindl, Herbert; Melin, Albert; Bolt, Hermann M., Lead, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, 2005, doi:10.1002/14356007.a15_193.pub2
- ^ Corson, B. B. (1936). "1,4-Diphenylbutadiene". Org. Synth. 16: 28; Coll. Vol. 2: 229.
