菲克定律
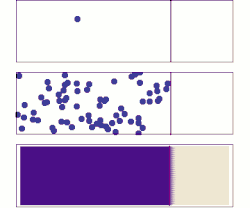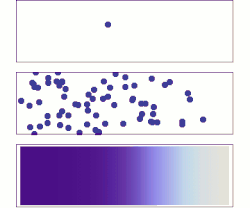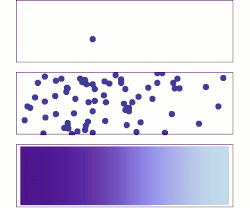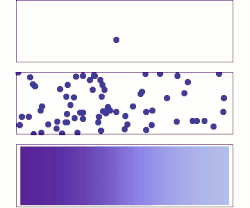
菲克定律描述扩散作用,可以使用这条定律来求得扩散系数,D。定律由阿道夫·菲克于1855年推导出来。
菲克第一定律
编辑假设从高浓度区域往低浓度流的通量大小与浓度梯度(空间导数)成正比,通过这个假设,菲克第一定律把扩散通量与浓度联系起来。在一维空间下的菲克定律如下:
其中
- 为“扩散通量”(于某单位时间内通过某单位面积的物质量),例如 。 量度在一段短时间内物质流过一小面积的量。
- 为扩散系数或扩散度,其量纲为[长度2 时间−1],例如
- 为浓度(假设为理想混合物),其量纲为[(物质的量) 长度−3],例如
- 为位置长度,例如
根据斯托克斯-爱因斯坦关系, 的大小取决于温度、流体黏度与分子大小,并与扩散分子流动的平均速度平方成正比。在稀的水溶液中,大部分离子的扩散系数都相近,在室温下其数值大概在0.6×10−9至2×10−9 m2/s。而生物分子的扩散系数一般介于10−11及10−12 m2/s之间。
在二维或以上的情况下,我们必须使用 (劈形或梯度算子)来把第一导数通用化,得
- 。
一维扩散的驱动力为 ,而对理想混合物而言,这股驱动力就是浓度的梯度。在非理想溶液或混合物的化学系统中,每一种物质的扩散驱动力则为各自种类的化学势梯度。此时菲克第一定律(一维状况)为:
其中标记i代表第i种物质,c为摩尔浓度(mol/m3),R为通用气体常数(J/(K mol)),T为绝对温度(K)及μ为化学势(J/mol)。
菲克第二定律
编辑菲克第二定律预测扩散会如何使得浓度随时间改变:
其中
- 为浓度,其量纲为[(物质的量) 长度−3],例如
- 为时间[s]
- 为扩散系数,其量纲为[长度2 时间−1],例如
- 为位置[长度],例如
可从菲克第一定律及质量守恒定律导出菲克第二定律:
假设扩散常数D不变(常数),用链式法则展开,得:
由此可得上述的菲克方程。
对于二维或以上的扩散,其菲克第二定律为:
- ,
其形式跟热传导方程类似。
若扩散系数不是常数,但大小取决于坐标及/或浓度,则菲克第二定律为:
其中一个重要的例子就是,当 处于稳定态的时候,即浓度不会因时间而变动,因此方程的左边等于零。在D不变及一维的情况下,浓度会随位置x作线性的变动。在二维或以上情况则:
例:一维解(扩散长度)
编辑在一维(x轴)扩散的情况下,设时间为t,初始点位于 的边界上,该点浓度值为 ,则扩散情况近似为
历史
编辑生理学家阿道夫·菲克最早于1855年发表[1][2]他那著名的定律,这定律支配所有通过扩散所进行的质量运输。菲克的研究受到之前托马斯·格雷姆的实验所启发,但这些实验就差在没有提出任何基础定律,而菲克就因提供了这样的定律而闻名。菲克定律与同时代的其他著名科学家所发现的定律有近似的地方:达西定律(水流)、欧姆定律(电荷运输)、及傅里叶定律(热运输)。
菲克的实验(模仿格雷姆的实验)主要由两个盐槽组成,两个槽由多条含水的管道连接,实验量度水管中的盐浓度及通量。有一点值得注意的是,菲克主要研究的是液体的扩散,而不是固体,因为当时普遍认为固体扩散并不可行[3]。时至今日,在研究固体、液体及气体扩散(假设后两者不会有大团的流体运动)时,菲克定律还是我们理解的核心。当扩散不遵从菲克定律时(确实有这种情况),我们把这种过程称为“非菲克扩散”,把它们称作例外的这点,“证实”了菲克于1855年提出的定律的重要性。
应用
编辑不同领域在需要模拟运输过程时,普遍地都会用到各种基于菲克定律的方程,这些领域包括食品、神经元、生物聚合物、药剂、有孔土壤、族群动态及半导体掺杂过程等。所有电压电流测定法的方法都是基于菲克方程的解。聚合物科学及食品科学的大量实验研究指出,在玻璃转化下需要使用更通用的手法来描述运输的分量。在玻璃转化发生时,周围的流动会变得“非菲克”。
生物学上的应用
编辑从第一定律可得下式[4]:
其中:
菲克第一定律在辐射传送方程中也是有重要性的。然而,当扩散系数很小的时候,辐射被光速所限制,而不是被物质的抵抗力所限制,菲克第一定律与辐射传送方程的关系就不准确。在这个时候可以采取通量限制。
在计算气体通过流体膜的交换率时,可将上式及格雷姆定律一起运用。
液体的菲克流
编辑当两种互溶液体接触时,扩散发生,宏观(或平均)浓度会跟随菲克定律而定。在介观角度下,也就是介于菲克定律所描述的宏观及分子的微观(分子随机运动发生的比例)的角度下,我们不可以忽略涨落。这个时候可以使用兰道-李佛西兹涨落水动力学来进行模拟。在这个理论框架下,扩散的起因是涨落,这些涨落的大小可由分子比例至宏观比例[5]。
有意思的是,涨落水动力方程含有一个描述菲克流的项,内有扩散系数,还有描述涨落的随机项及水动力方程。在使用摄动手法计算涨落时,其零度近似就菲克定律。通过第一度近似可得涨落,然后涨落造成扩散。因为这个由低度近似描述的现象是高度近似的结果,所以某程度上这代表一个永真式。只须把水动力方程重整化就可以解决这个问题。
半导体生产上的应用
编辑不少生产半导体的技术及成型过程都有用到由菲克定律所得出的扩散方程,这些技术包括化学气相沉积(CVD)、热氧化、湿式氧化法及掺杂等。
在某些情况下,解方程用的边界条件为扩散时源头浓度不变、有限源头浓度或边界会移动。
另见
编辑注释
编辑- ^ A. Fick, Pogg. Ann. (1855), 94, 59, doi:10.1002/andp.18551700105(德文).
- ^ A. Fick, Phil. Mag. (1855), 10, 30.(英文)
- ^ Jean Philibert, One and a Half Century of Diffusion: Fick, Einstein, before and beyond, Diffusion Fundamentals 2, 2005 1.1-1.10 互联网档案馆的存档,存档日期2009-02-05.
- ^ MCG生理学 3/3ch9/s3ch9_2
- ^ D. Brogioli and A. Vailati, Diffusive mass transfer by nonequilibrium fluctuations: Fick's law revisited, Phys. Rev. E 63, 012105/1-4 (2001) [1] (页面存档备份,存于互联网档案馆)
参考来源
编辑- W.F. Smith, Foundations of Materials Science and Engineering 3rd ed., McGraw-Hill (2004)
- H.C. Berg, Random Walks in Biology, Princeton (1977)
外部链接
编辑- 扩散的基础 (页面存档备份,存于互联网档案馆)(英文)
- 聚合物料中的扩散(英文)
- 菲克定律及玻尔兹曼变换等(附图及动画) (页面存档备份,存于互联网档案馆)(英文)
- 比尔·威尔逊,菲克第二定律,Connexions教育网,2007年8月21日 (页面存档备份,存于互联网档案馆)(英文)