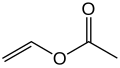
乙酸乙烯酯
乙酸乙烯酯的化学式为CH3COOCH=CH2,是一种无色有刺激性液体,也是制备工业中很重要的一种聚合物——聚乙酸乙烯酯的原料。和其它工业上很重要的化合物一样,乙酸乙烯酯有很多不同的名字或缩写。
| 乙酸乙烯酯 | |||
|---|---|---|---|
| |||
| IUPAC名 Ethenyl acetate 乙酸乙烯酯 | |||
| 英文名 | Vinyl acetate | ||
| 别名 | 醋酸乙烯酯,VAM | ||
| 识别 | |||
| CAS号 | 108-05-4 | ||
| PubChem | 7904 | ||
| ChemSpider | 7616 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | XTXRWKRVRITETP-UHFFFAOYAB | ||
| EINECS | 203-545-4 | ||
| ChEBI | 46916 | ||
| KEGG | C19309 | ||
| MeSH | C011566 | ||
| 性质 | |||
| 化学式 | C4H6O2 | ||
| 摩尔质量 | 86.09 g·mol⁻¹ | ||
| 外观 | 无色液体 | ||
| 密度 | 0.934 g/cm3 | ||
| 熔点 | -93 °C(180 K) | ||
| 沸点 | 72.7 °C(346 K) | ||
| 危险性 | |||
| 警示术语 | R:R11 | ||
| 安全术语 | S:S16, S23, S29, S33 | ||
| NFPA 704 | |||
| 闪点 | -8 °C | ||
| 自燃温度 | 427 °C | ||
| 爆炸极限 | 2.6–13.40% | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
制备
编辑乙酸乙烯酯的主要工业制备途径是通过乙烯和乙酸在氧气存在的情况下的催化反应,催化剂为钯。[1]
- 乙烯 + 乙酸 + 1/2 O2 → CH3COOCH=CH2 (乙酸乙烯酯) + H2O
此反应也会产生副反应:
- 乙烯 + 3 O2 → 2 CO2 + 2 H2O
聚合
编辑乙酸乙烯酯是一个单体,可以自身聚合形成聚乙酸乙烯酯,也可以和其它的单体聚合生成共聚物,例如乙烯/醋酸乙烯酯共聚物。因其自由基的不稳定,试图控制聚合进程的尝试都有一些问题。但是,RAFT(或更准确的说MADIX)聚合提供了一种更加简便的合成聚乙酸乙烯酯的方法,在该方法中,加入了黄酸盐作为链转移试剂。
衍生物
编辑乙酸乙烯酯可以发生大部分烯或酯能发生的反应。例如加入溴生成二溴化物,加入卤化氢生成1-卤代乙酸乙烯酯,这也是制备该物质的唯一方法,因为不存在对应的卤代醇。在钯催化下加入乙酸可以生成亚乙基二乙酸酯,CH3CH(OAc)2。后者能和许多羧酸发生酯交换反应。[3] 作为一个烯,乙酸乙烯酯也可以发生Diels-Alder反应和2+2环加成
毒性
编辑根据国际癌症研究机构的研究表明,乙酸乙烯酯在试验小白鼠中可能会导致癌症,一份加拿大的政府报告草案可能会标记其为有毒性。[4]
参考资料
编辑- ^ Y.-F. Han, D. Kumar, C. Sivadinarayana, and D.W. Goodman. Kinetics of ethylene combustion in the synthesis of vinyl acetate over a Pd/SiO2 catalyst (PDF). Journal of Catalysis. 2004, 224: 60–68 [2008-10-16]. doi:10.1016/j.jcat.2004.02.028. (原始内容 (PDF)存档于2008-03-07).
- ^ G. Roscher "Vinyl Esters" in Ullmann’s Encyclopedia of Chemical Technology, 2007 John Wiley & Sons: New York.
- ^ D. Swern and E. F. Jordan, Jr. Vinyl Laurate and Other Vinyl Esters (PDF). Organic Syntheses, Collected Volume 4. 1963: 977 [2008-10-16]. (原始内容 (PDF)存档于2011-06-05).
- ^ Chewing gum substance could be toxic. Vancouver Sun. 2008-05-13: A4.
外部链接
编辑- 美国环保署关于乙酸乙烯酯的健康评估(页面存档备份,存于互联网档案馆)(英文)