内源性反转录病毒
内源性反转录病毒(Endogenous retrovirus,简称ERV)是脊椎动物基因组中的一类具有长末端重复序列(LTR)的基因元件,与LTR反转录转座子非常相似,但除了gag与pol两基因外还多了编码包膜蛋白的env基因,可能源于千万年前感染细胞的反转录病毒,这些反转录病毒整合进宿主细胞基因组中,大部分已累积许多突变而不再能组装成完整病毒颗粒,仅能透过细胞复制垂直传播而不能在细胞间水平传播,许多甚至已丢失了开放阅读框,只剩两侧的LTR[1],不过有些仍能表现病毒蛋白,甚至有能组装成颗粒感染其他细胞者[2]。细胞中有许多机制可抑制内源性反转录病毒的基因表现,但这些序列仍可能在生殖细胞中与发育早期的胚胎里转录,进而复制增殖,内源性反转录病毒的过度表现可能与一些癌症与神经退化性疾病有关[3]。
反转录病毒丢失env基因后可能转为LTR反转录转座子,反之LTR反转录转座子获得env基因后可能转为反转录病毒[4],不过文献中常见混用两者的状况,且许多内源性反转录病毒丢失了编码蛋白的序列,有些LTR反转录转座子新获得类似env蛋白的序列,使两者差异更趋模糊[4]。有研究发现内源性反转录病毒丢失env基因而转为反转录转座子后,虽不能作为病毒感染其他细胞,但在基因组中增殖的能力大大增加[5]。
实例
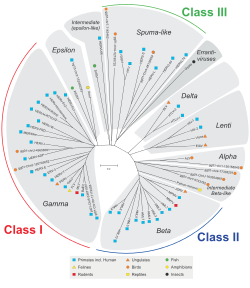
编辑人类基因组序列中有约5%至8%为内源性反转录病毒[6][7],可分为30至40个基因家族,并可依序列归为三型,第一型人类内源性反转录病毒(HERV)与Γ反转录病毒属和Ε反转录病毒属接近,第二型HERV与Β反转录病毒属接近,第三型HERV则与泡沫反转录病毒接近[8]。HERV-K(属第二型HERV)约在数百万年前进入灵长类基因组[9],现在人类基因组中约有数百个HERV-K,有些尚有完整的开放阅读框,在胚胎发育与某些疾病中可生成蛋白质[10][11]。另外还有HERV-T、HERV-L(最古老、存在于许多哺乳类类群中,但无发现env序列)、HERV-H(数量最多的HERV)、HERV-W(env基因被细胞用来编码合胞素-1)[12]。小鼠基因组中的内源性反转录病毒则包括与小鼠白血病病毒相关的元件、与鼠乳腺癌病毒相关的元件(如IAP元件)、MusD2/ETn元件和MuERV-L元件等[13]。猪基因组的内源性反转录病毒(porcine endogenous retroviruses,PERV)分为PERVA、PERVB与PERVC三型,其中有些可能仍保有组成病毒颗粒以感染其他细胞的能力[14],为过去进行异种器官移植(将猪的器官移植到病人身上)的一项隐忧,2017年有研究人员成功以CRISPR将猪基因组中所有内源性反转录病毒都去活化,以避免它们跨物种感染病患[15]。
影响基因表现
编辑有些内源性反转录病毒和LTR反转录转座子被细胞用作调控自身基因表现的一种方式[16][17]。LTR序列插入基因的5'后可能被用作启动子或强化子影响基因表现,在某些案例中甚至可影响下游约70kb处基因的表现[18][19]。人类AMY1C基因的启动子中即有完整的内源性反转录病毒序列,可调控其在唾腺的表现[20];BAAT基因主要的启动子也是来自内源性反转录病毒的LTR[21]。有些案例中,内源性反转录病毒的序列成为基因新的启动子,进而影响基因表现的组织种类,生殖组织中即有许多此类案例[22],例如编码芳香化酶的CYP19基因在大部分哺乳类中表现于脑部与生殖器官,但在灵长类中,因内源性反转录病毒LTR的插入而可在胎盘细胞中转录出一个5端序列却有差异的mRNA(transcript variant),进而在胎盘中表现蛋白,影响怀孕时雌激素的水平[19]。NOS3、IL2RB和HSD17B1也都由启动子的LTR序列调控其在胎盘的表现[21][23],这些现象显示LTR可能可与胎盘表现的转录因子结合,也能是胎盘DNA缺乏甲基化而不抑制其表现所致[24]。另外有假说认为胚胎中深入胎盘的滋胚层细胞可能利用内源性反转录病毒抑制母体的免疫反应,以避免受到母体免疫细胞的攻击,此机制可能对胎生的演化相当重要[25]。
除了影响基因表现,内源性反转录病毒还可能与宿主DNA重组成新的基因,例如新大陆猴与旧大陆猴的IRGM基因开放阅读框因Alu元件的插入而被破坏,使其成为不能编码蛋白的伪基因,但在大猩猩等人科动物基因组中,内源性反转录病毒ERV9的插入将其开放阅读框恢复,使其可编码蛋白[26];人类的内源性反转录病毒HERV-W虽已不具完整序列,但其env基因被细胞用来编码合胞素1,在胚胎的合胞体滋胚层(胎盘外层入侵子宫内膜的细胞)中表现。
参考文献
编辑- ^ Ishak, Charles A.; De Carvalho, Daniel D. Reactivation of Endogenous Retroelements in Cancer Development and Therapy. Annual Review of Cancer Biology. 2020, 4: 159–176. doi:10.1146/annurev-cancerbio-030419-033525.
- ^ van der Laan LJ, Lockey C, Griffeth BC, Frasier FS, Wilson CA, Onions DE; et al. Infection by porcine endogenous retrovirus after islet xenotransplantation in SCID mice.. Nature. 2000, 407 (6800): 90–4. PMID 10993079. doi:10.1038/35024089.
- ^ Meyer TJ, Rosenkrantz JL, Carbone L, Chavez SL. Endogenous Retroviruses: With Us and against Us.. Front Chem. 2017, 5: 23. PMC 5384584 . PMID 28439515. doi:10.3389/fchem.2017.00023.
- ^ 4.0 4.1 Hayward A. Origin of the retroviruses: when, where, and how?. Curr Opin Virol. 2017, 25: 23–27. PMC 5962544 . PMID 28672160. doi:10.1016/j.coviro.2017.06.006.
- ^ Magiorkinis G, Gifford RJ, Katzourakis A, De Ranter J, Belshaw R. Env-less endogenous retroviruses are genomic superspreaders.. Proc Natl Acad Sci U S A. 2012, 109 (19): 7385–90. PMC 3358877 . PMID 22529376. doi:10.1073/pnas.1200913109.
- ^ Belshaw R, Pereira V, Katzourakis A, Talbot G, Paces J, Burt A, Tristem M. Long-term reinfection of the human genome by endogenous retroviruses. Proc Natl Acad Sci USA. April 2004, 101 (14): 4894–99. Bibcode:2004PNAS..101.4894B. PMC 387345 . PMID 15044706. doi:10.1073/pnas.0307800101.
- ^ Nelson PN, Hooley P, Roden D, Davari Ejtehadi H, Rylance P, Warren P, et al. Human endogenous retroviruses: transposable elements with potential?. Clinical and Experimental Immunology. October 2004, 138 (1): 1–9. PMC 1809191 . PMID 15373898. doi:10.1111/j.1365-2249.2004.02592.x.
- ^ Vargiu L, Rodriguez-Tomé P, Sperber GO, Cadeddu M, Grandi N, Blikstad V; et al. Classification and characterization of human endogenous retroviruses; mosaic forms are common.. Retrovirology. 2016, 13: 7. PMC 4724089 . PMID 26800882. doi:10.1186/s12977-015-0232-y.
- ^ Barbulescu M, Turner G, Seaman MI, Deinard AS, Kidd KK, Lenz J. Many human endogenous retrovirus K (HERV-K) proviruses are unique to humans.. Curr Biol. 1999, 9 (16): 861–8. PMID 10469592. doi:10.1016/s0960-9822(99)80390-x.
- ^ Wildschutte JH, Williams ZH, Montesion M, Subramanian RP, Kidd JM, Coffin JM. Discovery of unfixed endogenous retrovirus insertions in diverse human populations.. Proc Natl Acad Sci U S A. 2016, 113 (16): E2326–34. PMC 4843416 . PMID 27001843. doi:10.1073/pnas.1602336113.
- ^ Grow EJ, Flynn RA, Chavez SL, Bayless NL, Wossidlo M, Wesche DJ; et al. Intrinsic retroviral reactivation in human preimplantation embryos and pluripotent cells.. Nature. 2015, 522 (7555): 221–5. PMC 4503379 . PMID 25896322. doi:10.1038/nature14308.
- ^ Magiorkinis G, Belshaw R, Katzourakis A. 'There and back again': revisiting the pathophysiological roles of human endogenous retroviruses in the post-genomic era.. Philos Trans R Soc Lond B Biol Sci. 2013, 368 (1626): 20120504. PMC 3758188 . PMID 23938753. doi:10.1098/rstb.2012.0504.
- ^ McCarthy EM, McDonald JF. Long terminal repeat retrotransposons of Mus musculus.. Genome Biol. 2004, 5 (3): R14. PMC 395764 . PMID 15003117. doi:10.1186/gb-2004-5-3-r14.
- ^ Patience C, Takeuchi Y, Weiss RA. Infection of human cells by an endogenous retrovirus of pigs. Nature Medicine. March 1997, 3 (3): 282–86. PMID 9055854. doi:10.1038/nm0397-282.
- ^ Niu D, Wei HJ, Lin L, George H, Wang T, Lee IH, Zhao HY, Wang Y, Kan Y, Shrock E, Lesha E, Wang G, Luo Y, Qing Y, Jiao D, Zhao H, Zhou X, Wang S, Wei H, Güell M, Church GM, Yang L. Inactivation of porcine endogenous retrovirus in pigs using CRISPR-Cas9. Science. September 2017, 357 (6357): 1303–07. Bibcode:2017Sci...357.1303N. PMC 5813284 . PMID 28798043. doi:10.1126/science.aan4187.
- ^ Khodosevich K, Lebedev Y, Sverdlov E. Endogenous retroviruses and human evolution. Comparative and Functional Genomics. October 2002, 3 (6): 494–98. PMC 2448423 . PMID 18629260. doi:10.1002/cfg.216.
- ^ Kim FJ, Battini JL, Manel N, Sitbon M. Emergence of vertebrate retroviruses and envelope capture. Virology. January 2004, 318 (1): 183–91. PMID 14972546. doi:10.1016/j.virol.2003.09.026.
- ^ Pi W, Zhu X, Wu M, Wang Y, Fulzele S, Eroglu A, Ling J, Tuan D. Long-range function of an intergenic retrotransposon. PNAS. July 2010, 107 (29): 12992–97. Bibcode:2010PNAS..10712992P. PMC 2919959 . PMID 20615953. doi:10.1073/pnas.1004139107.
- ^ 19.0 19.1 van de Lagemaat LN, Landry JR, Mager DL, Medstrand P. Transposable elements in mammals promote regulatory variation and diversification of genes with specialized functions. Trends Genet. October 2003, 19 (10): 530–36. PMID 14550626. doi:10.1016/j.tig.2003.08.004.
- ^ Ting CN, Rosenberg MP, Snow CM, Samuelson LC, Meisler MH. Endogenous retroviral sequences are required for tissue-specific expression of a human salivary amylase gene. Genes Dev. 1992, 6 (8): 1457–65. PMID 1379564. doi:10.1101/gad.6.8.1457.
- ^ 21.0 21.1 Cohen CJ, Lock WM, Mager DL. Endogenous retroviral LTRs as promoters for human genes: a critical assessment. Gene. 2009, 448 (2): 105–14. PMID 19577618. doi:10.1016/j.gene.2009.06.020.
- ^ Oliver KR, Greene WK. Mobile DNA and the TE-Thrust hypothesis: supporting evidence from the primates. Mob DNA. 2011, 2 (1): 8. PMC 3123540 . PMID 21627776. doi:10.1186/1759-8753-2-8.
- ^ Huh JW, Ha HS, Kim DS, Kim HS. Placenta-restricted expression of LTR-derived NOS3.. Placenta. 2008, 29 (7): 602–8. PMID 18474398. doi:10.1016/j.placenta.2008.04.002.
- ^ Cohen CJ, Lock WM, Mager DL. Endogenous retroviral LTRs as promoters for human genes: a critical assessment.. Gene. 2009, 448 (2): 105–14. PMID 19577618. doi:10.1016/j.gene.2009.06.020.
- ^ Villarreal LP, Villareal LP. On viruses, sex, and motherhood.. J Virol. 1997, 71 (2): 859–65. PMC 191132 . PMID 8995601. doi:10.1128/JVI.71.2.859-865.1997.
- ^ Bekpen C, Marques-Bonet T, Alkan C, Antonacci F, Leogrande MB, Ventura M; et al. Death and resurrection of the human IRGM gene.. PLoS Genet. 2009, 5 (3): e1000403. PMC 2644816 . PMID 19266026. doi:10.1371/journal.pgen.1000403.