六氟化锝
六氟化锝是一个低熔点的金黄色无机化合物[1],其化学式为TcF6,发现于1961年[3]。在这化合物中,锝有+6价,是目前发现的锝化合物中,氧化价最高的2个卤化物之一,另一个是六氯化锝(Technetium(VI) chloride, TcCl6)。其中,这里的锝与形成七氟化铼(ReF7)的铼不同[4]。六氟化锝会出现在六氟化铀的杂质中,因为锝是铀的裂变产物。
| 六氟化锝 | |
|---|---|
| |
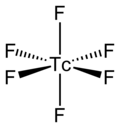
| IUPAC名 Technetium(VI) fluoride | |
| 识别 | |
| CAS号 | 13842-93-8 |
| PubChem | 57470148 |
| SMILES |
|
| InChIKey | PRVOBRCYHYXCMU-UHFFFAOYSA-H |
| 性质 | |
| 化学式 | TcF6 |
| 摩尔质量 | 212 g/mol (98Tc) g·mol⁻¹ |
| 外观 | 金黄色晶体[1] |
| 密度 | 3.58 g/cm3 (−140 °C、固态)[2] |
| 熔点 | 37.4 °C(311 K) |
| 沸点 | 55.3 °C(328 K) |
| 结构 | |
| 晶体结构 | 立方晶系 |
| 危险性 | |
| 欧盟分类 | 不在名单中 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
制备
编辑制备六氟化锝的方式是将锝金属和过量的氟气(F2)加热到摄氏400度。[3]
- Tc + 3 F
2 → TcF
6
特征
编辑六氟化锝在室温下为金黄色固体。其熔点较低,约为37.4℃[1],当环境温度高于38℃就会熔化,沸点为55.3℃[1],其在标准状态下液相的范围不大,仅有17.9℃。
六氟化锝在−4.54 °C会发生一次相变,高于该温度时,晶体结构为立方晶系,其晶格常数 a 为 6.16 Å[注 1]。每单位晶格有两个化学式单位[注 2],其密度为3.02 g·cm−3;而低于该温度时,晶体结构为正交晶系,其晶格常数a 为 9.55 Å、b 为 8.74 Å,、c 为 5.02 Å[注 3]。每单位晶格有四个化学式单位[注 2],其密度为3.38 g·cm−3。而当温度降到了摄氏−140℃时,晶格虽然保持为正交晶系,但晶格常数改变了,a 变为 9.360 Å、b 变为 8.517 Å而c 则变为 4.934 Å,密度也改变了,变为3.58 g·cm−3。[2]
而TcF6的分子本身[注 4]的分子结构为八面体形分子构型,点群为八面体对称(Oh)、Tc-F键的键长为1.812Å[2]、其磁矩测量值为0.45 μB[5]。
性质
编辑由于锝没有稳定的同位素,因此六氟化锝具有放射性,常温下为黄色固体。
物理
编辑六氟化锝在红外光谱学和拉曼光谱学的测定下呈现八面体形分子构型[6][7]。在低温下,六氟化锝和其他金属的六氟化物(如六氟化铑、六氟化锇)一样,会从室温的高对称性立方晶系结构转换成正交晶系结构[8]。其磁矩初步测量的数值约为0.45μB,比预期的d1八面体化合物来得低[9]。
化学
编辑六氟化锝在五氟化碘(IF5)溶液中能与碱性的氯反应形成六氟化物 [10][11]。六氟化锝会在氢氧化钠的水溶液(NaOH(aq))中水解,并形成黑色的二氧化锝(TcO2)沉淀[3] 。在氟化氢(HF)溶液中,六氟化锝会与氟化肼(hydrazinium fluoride、N2H5F)反应,得到N2H6TcF6或N2H6(TcF6)2[12]。
注解
编辑参考文献
编辑- ^ 1.0 1.1 1.2 1.3 CRC Handbook of Chemistry and Physics, 90th Edition, CRC Press, Boca Raton, Florida, 2009, ISBN 978-1-4200-9084-0, Section 4, Physical Constants of Inorganic Compounds, p. 4-93.
- ^ 2.0 2.1 2.2 Drews, T.; Supeł, J.; Hagenbach, A.; Seppelt, K. Solid State Molecular Structures of Transition Metal Hexafluorides. Inorganic Chemistry. 2006, 45 (9): 3782–3788. PMID 16634614. doi:10.1021/ic052029f.
- ^ 3.0 3.1 3.2 Selig, H.; Chernick, C.L.; Malm, J.G. The Preparation and Properties of TcF6. Journal of Inorganic and Nuclear Chemistry. 1961, 19 (3–4): 377–381.
- ^ Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ Selig, H.; Cafasso, F. A.; Gruen, D. M.; Malm, J. G. Magnetic Susceptibility of ReF6. Journal of Chemical Physics. 1962, 36 (12): 3440. Bibcode:1962JChPh..36.3440S. doi:10.1063/1.1732477.
- ^ Howard H. Claassen; Henry Selig & John G. Malm. Vibrational Spectra of MoF6 and TcF6. Journal of Chemical Physics. 1962, 36 (11): 2888–2890. Bibcode:1962JChPh..36.2888C. doi:10.1063/1.1732396.
- ^ Howard H. Claassen; Gordon L. Goodman; John H. Holloway & Henry Selig. Raman Spectra of MoF6, TcF6, ReF6, UF6, SF6, SeF6, and TeF6 in the Vapor State. Journal of Chemical Physics. 1970, 53 (1): 341–348. Bibcode:1970JChPh..53..341C. doi:10.1063/1.1673786.
- ^ Siegel S & Northrop DA. X-Ray Diffraction Studies of Some Transition Metal Hexafluorides. Inorganic Chemistry. 1966, 5 (12): 2187–2188. doi:10.1021/ic50046a025.
- ^ Selig, H; Cafasso, F A.; Gruen, D M.; Malm, J G. Magnetic Susceptibility of ReF6. Journal of Chemical Physics. 1962, 36 (12): 3440–3444. Bibcode:1962JChPh..36.3440S. doi:10.1063/1.1732477.
- ^ Edwards, A. J.; Hugill, D.; Peacock, R. D. New Fluorine Compounds of Technetium. Nature. 1963, 200 (4907): 672. Bibcode:1963Natur.200..672E. doi:10.1038/200672a0.
- ^ D. Hugill & R. D. Peacock. Some quinquevalent fluorotechnetates. Journal of the Chemical Society A. 1966: 1339–1341. doi:10.1039/J19660001339.
- ^ Frlec B; Selig H & Hyman H.H. Hydrazinium(+2) Hexafluorometalates(IV) and -(V) in the 4d and 5d Transition Series. Inorganic Chemistry. 1967, 6 (10): 1775–1783. doi:10.1021/ic50056a004.