布兰克氯甲基化反应
布兰克氯甲基化反应(Blanc氯甲基化,或氯甲基化)是无水氯化锌作用下芳香族化合物与甲醛和氯化氢作用生成氯甲基芳香化合物的反应。[1][2] 这个反应由化学家 Grassi-Cristaldi 和 Maselli 在 1898 年左右首次发现[3] ,以法国化学家古斯塔夫-路易·勃朗而命名,他于1923年进一步发展这个反应[4][5] 。该反应在化学工业和有机合成中有很重要的应用。用苯作原料,反应产物是氯化苄:
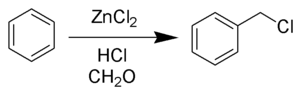
反应中可以使用其他路易斯酸(如氯化铝、氯化镍(II))等取代氯化锌[6]。盐酸可以用磷酸代替。而所用的甲醛也可以用其三聚体1,3,5-三𫫇烷做替代物[7]。
反应机理
编辑在酸性环境下进行,以氯化锌做催化剂。反应是质子化的甲醛对苯环的亲电芳香取代,然后伴随芳香环的重新构建,生成苄醇。在反应条件下,苄醇很容易被转化产物苄基氯。反应的机理如下图所示。
在氯化锌存在下,(氯甲基)氧𬭩离子(ClH2C–OH2+)和氯卡宾碳𬭩离子(ClCH2+)等也有机会成为亲电试剂[8]。
由于苯酚、苯胺等非常活泼的芳烃容易进行进一步跟产物苄基氯/苄醇发生傅-克烷基化反应,因此不适合用来做这反应的底物。其实一般来说,副产物二芳基甲烷的生成很普遍[9]。下图为此副反应的反应机理,图中以二苯基甲烷的生成作为例子:
相应的氟甲基化、溴甲基化和碘甲基化可以透过使用对应的氢卤酸来进行[10]。
副产物二氯甲基醚具有强致癌性,故在一定程度上限制了反应在工业上的应用。
相关反应
编辑在浓盐酸、甲醛存在下,硫醇也可以进行氯甲基化[11]:
- ArSH + CH2O + HCl → ArSCH2Cl + H2O
氯甲醚(MOM-Cl)也可以在此反应中作为氯甲基化试剂[12]。对于活性小的底物,使用MOM-Cl、60%硫酸的条件会有更好的反应结果[8]。这个反应可以应用于离子交换树脂、梅里菲尔德树脂的生产中苯乙烯的氯甲基化[13]。
参见
编辑参考资料
编辑- ^ Gustave Louis Blanc Bull. Soc. Chim. France 1923, 33, 313.
- ^ Fuson, R. C.; McKeever, C. H. Org. React. 1942, 1, 63.(综述)
- ^ Zerong Wang: Comprehensic Organic Name Reactions and Reagents, Volume 1, Wiley, 2009, S. 429, ISBN 978-0-471-70450-8.
- ^ Blanc, Gustave Louis. Sur la préparation de dérivés chlorométhyléniques aromatiques. Bulletin de la Société Chimique de France. Série 4. 1923, 33: 313–319.
- ^ Grassi, G.; Maselli, C. Su alcuni derivati clorurati de trossimetilene [On some chlorinated derivatives of 1,3,5-trioxane]. Gazzetta Chimica Italiana. 1898, 28 (pt 2): 477–500 [495].
- ^ Louis F. Fieser, Arnold M. Seligman, Journal of the American Chemical Society, 57: pp. 942–946, (德文)
- ^ Yolanda T. Pratt, Journal of the American Chemical Society, 73: pp. 3803–3807, (德文)
- ^ 8.0 8.1 Laali, Kenneth K. Formaldehyde–Hydrogen Chloride. Encyclopedia of Reagents for Organic Synthesis. American Cancer Society. 2001. ISBN 978-0-470-84289-8. doi:10.1002/047084289x.rf022 (英语).
- ^ McKeever, C. H.; Fuson, Reynold C. Chloromethylation of Aromatic Compounds. Organic Reactions. American Cancer Society. 2011-03-15: 63–90. ISBN 978-0-471-26418-7. doi:10.1002/0471264180.or001.03 (英语).
- ^ C., Norman, Richard O. Principles of Organic Synthesis. Coxon, James M. 3rd. Boca Raton: Routledge. 2017. ISBN 978-1-351-42173-7. OCLC 1042320639.
- ^ D. Enders; S. Von Berg; B. Jandeleit. Diethyl [(Phenylsulfonyl)methyl]phosphonate. Organic Syntheses. 2002, 78: 169. doi:10.15227/orgsyn.078.0169.
- ^ Wuts, Peter G. M. Chloromethyl Methyl Ether. Encyclopedia of Reagents for Organic Synthesis. 2001. ISBN 0471936235. doi:10.1002/047084289X.rc118.
- ^ Dardel, François; Arden, Thomas V., Ion Exchangers, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, 2005, doi:10.1002/14356007.a14_393.pub2