七氧化二铼
化合物
七氧化二铼,又称氧化铼(VII)或高铼酸酐,是铼最常见的氧化物,化学式为Re2O7,为挥发性黄色晶体。
| 七氧化二铼 | |
|---|---|
| |

| |
| IUPAC名 Rhenium(VII) oxide | |
| 别名 | 氧化铼(VII) |
| 识别 | |
| CAS号 | 1314-68-7 |
| PubChem | 123106 |
| SMILES |
|
| InChI |
|
| 性质 | |
| 化学式 | Re2O7 |
| 摩尔质量 | 484.410 g·mol⁻¹ |
| 外观 | 黄色结晶性粉末 |
| 密度 | 6.103 g/cm3 (固) |
| 熔点 | 360 °C |
| 沸点 | 升华 |
| 危险性 | |
| 欧盟分类 | 未列明 |
| 相关物质 | |
| 相关化学品 | 七氧化二锰、七氧化二锝、高铼酸 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
结构
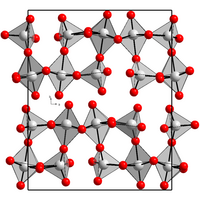
编辑X射线单晶衍射证实,七氧化二铼晶体中,一个铼原子以扭曲的八面体与氧原子配位,一个铼原子以四面体与氧原子配位。八面体与四面体结构共用一个顶点,八面体还和另一个八面体共边相连。气态时,七氧化二铼以分子存在,存在两个ReO4四面体结构,共用一个顶点。[1]
制取
编辑金属铼于150°C以上在空气中或氧气中燃烧,或二氧化铼在空气中强热都能生成七氧化二铼,氧浓度较低时还可观察到红色三氧化铼的生成。此外,金属铼与过氧化氢作用制得高铼酸溶液,然后与五氧化二磷在真空下共热,便会有七氧化二铼升华出来。
七氧化二铼可通过真空升华进行提纯,制成黄色的大的角状晶体。
反应
编辑七氧化二铼溶于水生成高铼酸溶液:
- Re2O7 + 2 H2O → Re2O7·2 H2O
参考资料
编辑- ^ Wells, A.F. (1984) Structural Inorganic Chemistry, Oxford: Clarendon Press. ISBN 0-19-855370-6.
- ^ W. A. Herrmann and F. E. Kuhn. Organorhenium Oxides. Acc. Chem. Res. 1997, 30 (4): 169–180. doi:10.1021/ar9601398.
| 这是一篇关于无机化合物的小作品。您可以通过编辑或修订扩充其内容。 |