细胞毒性T细胞
细胞毒性T细胞(英语:cytotoxic T cell,TC或CTL,简称胞毒T细胞)又称杀手T细胞(killer T cell)、TC细胞、胞杀T细胞、效应T细胞或CD8+ T细胞,属于T细胞的一种,可以杀死癌细胞、受病毒感染的细胞,以及其他受损细胞。胞毒T细胞属于后天免疫系统的成员,当其杀伤活性开始表现时,属于先天免疫系统的NK细胞活性就会逐步降低。T细胞的一种。 执行清除被感染细胞。 分泌穿孔素使被感染细胞穿孔,导致细胞凋亡。
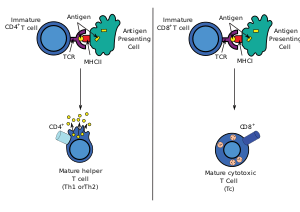
大多数细胞毒性T细胞会表达T细胞受体(TCR),此受体可以识别特定的抗原,而那些抗原常常是由癌细胞和病毒制造的。胞内抗原会与第一型MHC分子结合,并被带到细胞表面,以利于T细胞辨识。T细胞一旦透过T细胞受体辨识出特定的抗原,便会摧毁该细胞。
有些T细胞受体中含有一种称为CD8的糖蛋白,可与MHC1类分子结合,故这些细胞又名CD8+ T细胞。
和第一型MHC分子结合的CD8 T细胞会发育为细胞毒性T细胞,而CD8分子则会持续牢牢地抓着第一型MHC分子,不让目标细胞离开,以进行细胞毒杀。
发育
编辑免疫系统必须有能力辨识数百万种抗原,但身体内却只有30,000对基因,所以不可能一个抗原就花费一组基因来辨识。因此,身体内采用的势必是另一套机制。骨髓中的未成熟白血球DNA会改变,制造出特定的白血球受体,而每一种白血球则可以与不同的抗原结合。但这种方式制造出来的白血球有可能会与身体中的物质结合,如果放任这些白血球四处发生免疫反应,称为自身免疫疾病,严重者可致死。因此,身体将这些未成熟的白血球送到胸腺,将这些会与体内物质结合的白血球摧毁。
T细胞受体(T cell receptor,简称TCRs)有两个部分,分别是α链和β链(有些有γ链和δ链)。骨髓中的造血干细胞会移动到胸腺,并在胸腺进行β链的VDJ重组,称为前T细胞受体。如果重组成功,那么原先的α链TCR DNA就会转为αβ TCR复合体。这种高变异的重组模式,可以产生数百万种不同的T细胞,可以辨识出不同的抗原。大部分的T细胞的受体为αβ TCR(αβ T细胞)但有一些表皮中的T细胞含有γδ TCR(γδ T细胞),可以辨识一些非蛋白质性抗原。
T细胞受体稳定的幼年T细胞会同时表现CD4和CD8协同受体,因此被称为双阳性T细胞(double-positive T cell,简称DP T cell),胸腺中的双阳性T细胞会接触到大量的自身抗原,并进行两种株落选择:
经过这两道筛检之后所剩下来的T细胞才会成熟,会转变为单阳性T细胞(CD4+或CD8+),如果是CD8+,那么成熟的T细胞就会辨识第一类MHC分子;如果是CD4+,那么成熟的T细胞就会辨识第二类MHC分子。决定辨识CD8的T细胞就会变成细胞毒性T细胞。
活化
编辑除了一些少数细胞和没有细胞核的细胞(如红血球),宿主的细胞表面几乎都会表现第一类MHC分子。当细胞被病毒感染时(或其他胞内病原体),细胞会降解外来蛋白质,并由第一类MHC分子将蛋白质片段表现于细胞表面,以利于CD8+ T细胞辨识,此动作称为抗原呈现。
细胞毒性T细胞的活化取决于T细胞表面的分子和抗原呈递细胞表面分子之间的交互作用。例如双讯息模型:
| 讯息 | T细胞 | APC | 描述 |
| 第一讯息 | TCR | 第一类MHC分子 | CD8辅助受体和第一类MHC分子之间会引发交互作用以稳定信息分子。 |
| 第二讯息 | T细胞上的CD8 | CD80或CD86(又称B7-1和B7-2) | 由辅助型T细胞释出,可活化细胞毒性T细胞。CD80和CD86在T细胞活化中扮演着“协同刺激信号”的角色。 |
杀手T细胞的活化大多是靠TCR侦测到抗原所引发,但也有少部分是靠替代路径。举例来说,研究显示细胞毒性T细胞如果被其他CD8 T细胞视为目标,会引起对于后者的耐受作用。[3]
细胞毒性T细胞一旦活化,便会在IL-2的刺激下开始快速增殖。IL-2是一种T细胞的成长和细胞分化因子,使T细胞能够更有效的清除体内含有抗原的体细胞。
作用机制
编辑当细胞毒性T细胞遇到受感染或是不健康的体细胞,细胞毒性T细胞会释放出细胞毒素,如穿孔素、颗粒酶,以及颗粒溶解素。这些酵素会进入目标细胞的细胞质,并使细胞内的丝氨酸蛋白酶诱发胱天蛋白酶的级联反应,这个反应会使一连串的胱胺酸蛋白酶活化,引发细胞凋亡。
另外一种诱发细胞凋亡的途径是借由细胞表面受体的结合。细胞毒性T细胞表面上有种表面蛋白,叫FAS配体(FasL,又称Apo1L、CD95L)。这种蛋白会和目标细胞上的Fas受体(Apo1,又称CD95)结合[4]。Fas与FasL结合后,会引来死亡诱导讯号复合体(death-induced signaling complex,简称DISC),Fas关联死亡区域(Fas-associated death domain,FADD)会随着DISC移位,引来胱天蛋白酶原8和10[5],之后胱天蛋白酶会被胱天蛋白酶3、6,和7活化,导致如lamin A、lamin B1、lamin B2、PARP(聚ADP核糖聚合酶),和DNAPK(DNA活化蛋白激酶)等蛋白被水解,导致细胞凋亡。
疾病病理学
编辑在乙型肝炎病毒(HBV)的感染上,细胞毒性T细胞扮演了一个相当重要的致病原。因为被HBV感染的肝细胞会被细胞毒性T细胞所毒杀,因此造成肝部的严重损坏。[6]近期研究显示,血小板可吸引专门对付病毒的细胞毒性T细胞来到受感染的肝脏。[7]
参见
编辑参考文献
编辑- ^ 1.0 1.1 S. Munir Alam, Paul J. Travers, Jay L. Wung, Wade Nasholds, Stella Redpath, Stephen C. Jameson, Nicholas R. J. Gascoigne. T-cell-receptor affinity and thymocyte positive selection. Nature. 1996-06, 381 (6583): 616–620 [2018-04-02]. ISSN 1476-4687. doi:10.1038/381616a0. (原始内容存档于2010-06-26) (英语).
- ^ 2.0 2.1 Timothy K. Starr, Stephen C. Jameson, Kristin A. Hogquist. Positive and Negative Selection of T Cells. Annual Review of Immunology. 2003-04-01, 21 (1): 139–176 [2018-04-02]. ISSN 0732-0582. doi:10.1146/annurev.immunol.21.120601.141107. (原始内容存档于2022-04-12).
- ^ Milstein, O., Hagin, D., Lask, A., Reich-Zeliger, S., Shezan E., Ophir E., Eidelshtein Y., Afik R., Antebi YE., Dustin ML. and Reisner Y. (2011) CTLs respond with activation and granule secretion when serving target for T cell recognition. Blood 117,1042-1052 (页面存档备份,存于互联网档案馆)
- ^ Andersen MH, Schrama D, Thor Straten P, Becker JC. Cytotoxic T cells. The Journal of Investigative Dermatology. 2006年1月, 126 (1): 32–41. PMID 16417215. doi:10.1038/sj.jid.5700001.
- ^ M. Muzio, A. M. Chinnaiyan, F. C. Kischkel, K. O'Rourke, A. Shevchenko, J. Ni, C. Scaffidi, J. D. Bretz, M. Zhang, R. Gentz, M. Mann, P. H. Krammer, M. E. Peter, V. M. Dixit. FLICE, a novel FADD-homologous ICE/CED-3-like protease, is recruited to the CD95 (Fas/APO-1) death--inducing signaling complex. Cell. 1996-06-14, 85 (6): 817–827 [2019-02-13]. ISSN 0092-8674. PMID 8681377. (原始内容存档于2019-06-03).
- ^ Iannacone, Matteo; Sitia, Giovanni; Guidotti, Luca G. Pathogenetic and antiviral immune responses against hepatitis B virus. Future Virology. 2006, 1 (2): 189–96. doi:10.2217/17460794.1.2.189.
- ^ Iannacone, Matteo; Sitia, Giovanni; Isogawa, Masanori; Marchese, Patrizia; Castro, Maria G; Lowenstein, Pedro R; Chisari, Francis V; Ruggeri, Zaverio M; Guidotti, Luca G. Platelets mediate cytotoxic T lymphocyte–induced liver damage. Nature Medicine. 2005, 11 (11): 1167–9. PMC 2908083 . PMID 16258538. doi:10.1038/nm1317.
- ^ Subramanian S and Ramalingam K. Electron microscopic evidence on the participation Cytotoxic T Lymphocytes and Macrophages in Mtb adjuvant induced connective tissue inflammation and arthritogenesis in Rattus norvegicus. Asian Journal of Microbiology, Biotechnology and Environmental Sciences. 2005, 7 (2): 227–233. ISSN 0972-3005.
外部链接
编辑- (英文)T-cell Group - Cardiff University
- (英文)Malaria (Flash Animation)