碳酸鹽
碳酸根是一種鹽,它的化學式為CO32-,雖然碳酸根含碳,但含碳酸根的物質卻多是無機物。碳酸根是一種弱酸根,在水中很容易水解產生碳酸氫根離子和氫氧根離子,從而使水偏向鹼性。
| 碳酸鹽 | |
|---|---|
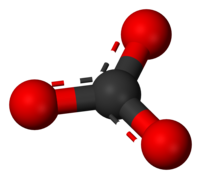
| |
| IUPAC名 Carbonate | |
| 系統名 Trioxidocarbonate[1]:127 | |
| 識別 | |
| CAS號 | 3812-32-6 |
| PubChem | 19660 |
| ChemSpider | 18519 |
| SMILES |
|
| InChI |
|
| InChIKey | BVKZGUZCCUSVTD-NUQVWONBAE |
| 性質 | |
| 化學式 | CO32- |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
碳酸鹽
編輯碳酸鹽有很多,在生活中有許多常見的碳酸鹽,比如純鹼[2]、石灰石[3]等。
碳酸鹽中有如下幾個沉澱及難溶物,但這些難溶物均溶於酸[4]:
通常,碳酸鹽中只有 可溶於水。
碳酸根的鑑別
編輯通常情況下,碳酸根可以用酸來鑑別。因為碳酸根離子很容易和氫離子結合生成碳酸,然後分解為二氧化碳和水,故只要加入酸便會產生氣體。[5]
對於水溶液中的碳酸根鑑別,嚴謹一些的方法則是:加入可溶性鈣鹽或者鋇鹽,生成的白色沉澱溶於酸後放出無色無味、使澄清石灰水變渾濁的氣體。
應用
編輯註解
編輯- ^ International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. Electronic version.
- ^ 即碳酸鈉,化學式Na2CO3
- ^ 主要成分為碳酸鈣,化學式CaCO3,不溶於水
- ^ 反應方程式:CO32- + 2H+ = H2O+ CO2↑
這個反應式也同樣用於在實驗室中製取二氧化碳。 - ^ 如:CaCO3 + 2HCl = CaCl2 + H2O + CO2↑
- ^ 反應式:CaCO3 → CaO + CO2↑