化学平衡
此条目没有列出任何参考或来源。 (2019年7月2日) |
化学平衡(英语:Chemical equilibrium)是指在宏观条件的可逆反应中,化学反应正逆反应速率相等,且反应物浓度和生成物浓度不再改变的状态。
化学平衡也是化学热力学的主要研究内容。
化学平衡的特征
编辑当一个化学反应达到化学平衡后,需要外部变因恒定才能保持此平衡状态。如果外部变因有所改变,此平衡状态将被打破,反应将往另外一个平衡状态进行。根据勒夏特列原理,当一个已达平衡的系统被变动,该系统会随之改变,以抗衡该变动。
化学平衡的判断
编辑直接标志
编辑- 正逆反应速率相等
- 反应物与生成物物质的量不再改变
间接标志
编辑- 反应前后气体体积不同的反应,气体体积不发生改变。
- 如反应 ,若其体积不发生改变,则说明已经达到平衡。
- 反应物和生成物颜色不同的反应,混合物的颜色不发生改变。
- 如反应 (红棕色) (无色),若混合气体颜色不发生改变,则说明已经达到平衡。
- 反应前后气体体积不同的反应,气体密度不发生改变。
- 如反应 ,若混合气体密度不发生改变,则说明已经达到平衡。
- 反应体系的热量不再发生变化。
- 如反应 ,若混合气体不放热或吸热,则说明反应已经达到平衡。
热力学
编辑判断化学反应是否平衡,还可使用此式判断
ΔrGm=ΣνΑμΑ=0
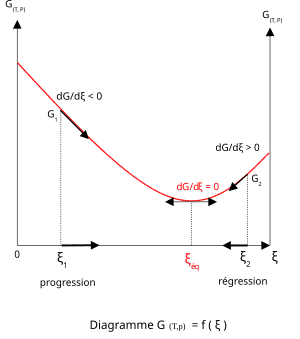
其中,μA是指反应中A物质的化学势。也就是说,化学反应达到平衡状态,意味着生成物的吉布斯自由能G达到最小。理论上来讲,对于产物已知的化学反应,应用吉布斯最小自由能法,结合反应物和生成物的热力学数据,就可以计算出平衡产物。
化学平衡反应的种类以及示例
编辑1.一般化学平衡(可逆反应)
- 平衡示例:
2.溶解平衡
- 平衡示例:
3.沉淀平衡
- 平衡示例:
4.电离平衡
- 平衡示例:
- 弱酸:
- 弱碱:
平衡混合物
编辑体系处于平衡状态时,反应物和生成物的混合物称为平衡混合物。