蒸气压
此条目可参照外语维基百科相应条目来扩充。 (2017年5月21日) |
此条目没有列出任何参考或来源。 (2014年7月18日) |
一种物质的蒸气压也称作饱和蒸气压,指的是这种物质的气相与其非气相达到平衡状态时的压强;任何物质(包括液态与固态)都有挥发成为气态的趋势,其气态也同样具有凝结为液态或者凝华为固态的趋势。在给定的温度下,一种物质的气态与其凝聚态(固态或液态)之间会在某一个压强下存在动态平衡。此时单位时间内由气态转变为凝聚态的分子数与由凝聚态转变为气态的分子数相等。这个压强就是此物质在此温度下的饱和蒸气压。
在密闭空间,物质在给定的温度下,可使该物质沸腾的气体分压,此时蒸发/凝结过程达到动态平衡。当气体的压力(分压)与饱和蒸汽压相等时,对应的温度称为露点,这时空气的相对湿度为100%。此时如果降低温度或者增加空气中水蒸气的含量,就会出现水凝结的现象。
它们之间的关系可以用克劳修斯-克拉佩龙方程(Clausius–Clapeyron relation)描述[1]。随着温度的升高,物质蒸气压随之升高直到足以克服周围大气的压强从而在物质本体内的任何位置发生气化而产生大量气泡。这一现象叫做沸腾,而这个温度叫做此压强下的沸点。物质的常压沸点就是此物质的饱和蒸气压等于一个标准大气压时候的温度。需要注意的是在较深液体中发生的沸腾所需温度会高于较浅液体中的沸腾,因为除了大气压强外还需要克服液体自身深度所造成的压强。对于溶液,计算需用拉乌尔定律[2]。
水的饱和蒸汽压可以根据Goff-Gratch方程式确定。
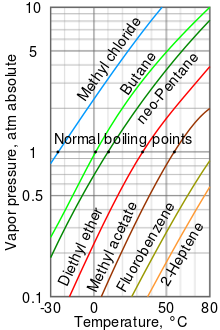
使用安托万方程计算蒸气压
编辑安托万方程[3][4]是一个用来描述液体或固体的蒸气压与温度的经验表达式。安托万方程的原始表达式如下:
将温度项单独移至等号左边后可得:
其中:
- 为该物质的蒸气压。
- 为该物质的温度。
- , 与 为与物质相关的系数 (可为常数或变数),每组 , , 值只适用于特定物质的特定温度范围。
而上式在某些情况项又可以被化简为如下:
总体来说,安托万方程的使用上有许多限制。例如,该方程无法找出一组可适用于熔点与临界温度的范围内的 , 与 。另外,在建表当时的仪器导致该表于10托下的低压环境也相当不精准。
参见
编辑参考文献
编辑- ^ Clausius-Clapeyron Equation. Chemistry LibreTexts. 2014-06-01 [2024-02-16]. (原始内容存档于2021-04-15) (英语).
- ^ Raoult's Law. Chemistry LibreTexts. 2013-10-02 [2024-02-16]. (原始内容存档于2024-02-16) (英语).
- ^ Coulson, J. M.; Richardson, J. F.; Sinnott, Raymond K. Chemical engineering. 6: Chemical engineering design. Chemical Engineering Design 4. ed. Amsterdam Heidelberg: Elsevier. 2005: 331. ISBN 978-0-7506-6538-4.
- ^ Antoine's Equation. uweb.engr.arizona.edu. [2024-02-16]. (原始内容存档于2024-02-16).