乙醯乙酸
化合物
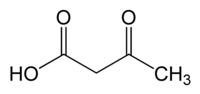
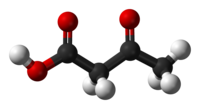
乙醯乙酸是最簡單的β-酮酸,化學式為C4H6O3,室溫下為無色結晶。它有弱酸性,可以與水和醇混溶。與其他β-酮酸一樣,乙醯乙酸不穩定,加熱到100 °C時便迅速分解為丙酮和二氧化碳。乙醯乙酸酯比乙醯乙酸穩定得多,因此用途也比較廣。
| 乙醯乙酸 | |
|---|---|
| |
| |
| IUPAC名 3-oxobutanoic acid 3-氧代丁酸 | |
| 別名 | 乙醯醋酸、β-丁酮酸、3-丁酮酸 |
| 識別 | |
| CAS號 | 541-50-4 |
| PubChem | 96 |
| ChemSpider | 94 |
| SMILES |
|
| InChI |
|
| InChIKey | WDJHALXBUFZDSR-UHFFFAOYAH |
| ChEBI | 15344 |
| DrugBank | DB04025 |
| KEGG | C00164 |
| 性質 | |
| 化學式 | C4H6O3 |
| 莫耳質量 | 102.09 g·mol⁻¹ |
| 外觀 | 無色油狀液體或結晶 |
| 熔點 | 36.5 °C |
| 沸點 | 分解 |
| 溶解性(水) | 混溶 |
| pKa | 3.77 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
- CH3C(O)CH2CO2H → CH3C(O)CH3 + CO2
乙醯乙酸由乙醯乙酸乙酯水解得到。[1]一般都是在0 °C時製備,而且現配先用。[2]
乙醯乙酸在鹼溶液中更加穩定。37 °C時,酸性溶液中的乙醯乙酸半衰期為140分鐘,在鹼性溶液中則為130小時。[3]
乙醯乙酸是脂肪酸β氧化時,乙醯輔酶A的縮合產物,是酮體的三個組成之一。 脂肪酸代謝過度之後,糖尿病、飢餓、急性乙醇中毒等均會使乙醯乙酸的含量增高。可用於鑑別和監護糖尿病酮症酸中毒病人的診斷和治療。
參見
編輯參考資料
編輯- ^ Robert C. Krueger. Crystalline Acetoacetic Acid. Journal of the American Chemical Society. 1952, 74 (21): 5536–5536. doi:10.1021/ja01141a521.
- ^ George A. Reynolds and J. A. VanAllan "Methylglyoxal-ω-Phenylhydrazone" Organic Syntheses, Collected Volume 4, p.633 (1963)存档副本 (PDF). [2008-10-28]. ([.http://www.orgsyn.org/orgsyn/pdfs/CV4P0633.pdf 原始內容] 請檢查
|url=值 (幫助) (PDF)存檔於2007-09-27). - ^ Hay, R. W.; Bond, M. A. Kinetics of decarboxilation of acetoacetic acid. Aust. J. Chem. 1967, 20 (9): 1823–8.