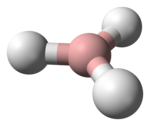
甲硼烷
甲硼烷,又稱三氫化硼,是一種無機化合物,化學式為BH3。它很不穩定,具有高反應性。羰基甲硼烷(BH3CO)的製備在探索甲硼烷的化學過程中起著重要作用,因為它可能存在甲硼烷分子。 [1] 但是,BH3分子是非常強的路易斯酸。因此,它具有很高的反應性,只能直接在流動系統中以連續產生的,短暫的產物形式觀察到。甲硼烷也可以通過雷射燒蝕的原子硼與氫的反應而直接觀察到。 [2]
| 甲硼烷 | |||
|---|---|---|---|

| |||
| |||
| IUPAC名 Borane trihydridoboron | |||
| 識別 | |||
| CAS號 | 13283-31-3 | ||
| PubChem | 6331 | ||
| ChemSpider | 6091 | ||
| SMILES |
| ||
| Gmelin | 44 | ||
| ChEBI | 30149 | ||
| 性質 | |||
| 化學式 | BH3 | ||
| 莫耳質量 | 13.83 g·mol⁻¹ | ||
| 結構 | |||
| 偶極矩 | 0 D | ||
| 危險性 | |||
| 自燃溫度 | 38 °C | ||
| 相關物質 | |||
| 相關硼化合物 | 乙硼烷 三氟化硼 | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
結構
編輯BH3中,硼原子為sp2雜化,分子為平面三角形結構,D3h對稱群,與價層電子對互斥理論的預測相吻合。儘管B-H鍵是極性共價鍵,但其分子對稱性抵消了偶極矩,使得偶極矩為0。B–H鍵的鍵長為119 pm。[3]
在正常情況下,BH3會二聚成B2H6。甲硼烷是製備乙硼烷時的中間產物:[4]
- BX3 +BH4− → HBX3− + (BH3) (X=F, Cl, Br, I)
- 2 BH3 → B2H6
估計BH3的二聚標準焓為−170 kJ mol−1。[5] BH3 中的硼有 6 顆價電子。 因此,它是強路易斯酸,並與任何路易斯鹼,也就是下方的L反應,形成加合物。
- BH3 + L → L—BH3
路易斯鹼會把一對價電子捐給甲硼烷分子,形成一個共價配位鍵。 有一些化合物是熱穩定的,不過容易被空氣氧化。含有甲硫醚硼烷和四氫呋喃硼烷的溶液可商購獲得,不過要在四氫呋喃硼烷中加入穩定劑,以防止THF氧化甲硼烷。 [6] 根據光譜和熱化學數據估算的幾種甲硼烷常見的加合物的穩定性序列如下:
BH3 是一種軟酸,和硫原子加合所形成的化合物比和氧原子加合穩定。[4]BH3 的水溶液極度不穩定。[7][8]
- BH
3 + 3H
2O → B(OH)
3 + 3 H
2
反應
編輯BH3是乙硼烷反應時的中間活性體,可以合成更大的硼烷:[4]
之後的過程會產生更大的硼烷,最終產物是 B10H14 作為受聚合物材料污染的最穩定物質,還有少量的 B20H26。
硼烷氨,可以由其它甲硼烷加合物的置換反應獲得。加熱時,硼烷氨中的氫氣流失,形成環硼氮烷,化學式(HBNH)3。[9]
甲硼烷的加合物被廣泛用於有機合成的硼氫化反應。在硼氫化反應中, BH3 被加入到烯烴的 C=C 雙鍵並形成三烷基硼:
- (THF)BH3 + 3 CH2=CHR → B(CH2CH2R)3 + THF
該反應是區域選擇性的,可以使用其他硼烷衍生物來提供更高的區域選擇性。 [10] 產物三烷基硼可以轉化為有用的有機衍生物。使用大體積烯烴可以製備諸如[HBR2]2的物質,它們在更專業的應用中也是有用的試劑。 比四氫呋喃硼烷穩定的甲硫醚硼烷也能被使用。[11][10]
硼氫化反應可以與氧化反應結合,形成硼氫化-氧化反應。在該反應中,生成的有機硼化合物中的硼烷基會被羥基取代。
甲硼烷(5)
編輯甲硼烷(5)是甲硼烷的雙氫配合物,化學式BH5 或 BH3(η2-H2).[12]它只能在低溫下存在。[13][14] 甲硼烷(5)和甲鎓離子 (CH5+) 是等電子體。[15]它是硼氫離子的共軛鹼。
參見
編輯參考資料
編輯- ^ Burg, Anton B.; Schlesinger, H. I. Hydrides of boron. VII. Evidence of the transitory existence of borine (BH
3): Borine carbonyl and borine trimethylammine. Journal of the American Chemical Society. May 1937, 59 (5): 780–787. doi:10.1021/ja01284a002. - ^ Tague, Thomas J.; Andrews, Lester. Reactions of Pulsed-Laser Evaporated Boron Atoms with Hydrogen. Infrared Spectra of Boron Hydride Intermediate Species in Solid Argon. Journal of the American Chemical Society. 1994, 116 (11): 4970–4976. ISSN 0002-7863. doi:10.1021/ja00090a048.
- ^ Kawaguchi, Kentarou. Fourier transform infrared spectroscopy of the BH3 ν3 band. The Journal of Chemical Physics. 1992, 96 (5): 3411. Bibcode:1992JChPh..96.3411K. ISSN 0021-9606. doi:10.1063/1.461942.
- ^ 4.0 4.1 4.2 Greenwood, N. N.; Earnshaw, A. Chemistry of the Elements 2nd. Oxford:Butterworth-Heinemann. 1997. ISBN 0-7506-3365-4.
- ^ Page, M.; Adams, G.F.; Binkley, J.S.; Melius, C.F. Dimerization energy of borane. J. Phys. Chem. 1987, 91 (11): 2675–2678. doi:10.1021/j100295a001.
- ^ Hydrocarbon Chemistry, George A. Olah, Arpad Molner, 2d edition, 2003, Wiley-Blackwell ISBN 978-0471417828
- ^ Finn, Patricia; Jolly, William L. Asymmetric cleavage of diborane by water. The structure of diborane dihydrate. Inorganic Chemistry. August 1972, 11 (8): 1941–1944 [2020-10-21]. doi:10.1021/ic50114a043. (原始內容存檔於2021-04-27).
- ^ D'Ulivo, Alessandro. Mechanism of generation of volatile species by aqueous boranes. Spectrochimica Acta Part B: Atomic Spectroscopy. May 2010, 65 (5): 360–375. doi:10.1016/j.sab.2010.04.010.
- ^ Housecroft, C. E.; Sharpe, A. G. Chapter 13: The Group 13 Elements. Inorganic Chemistry 3rd. Pearson. 2008: 336. ISBN 978-0-13-175553-6.
- ^ 10.0 10.1 Burkhardt, Elizabeth R.; Matos, Karl. Boron reagents in process chemistry: Excellent tools for selective reductions. Chemical Reviews. July 2006, 106 (7): 2617–2650. doi:10.1021/cr0406918.
- ^ Kollonitisch, J. Reductive Ring Cleavage of Tetrahydrofurans by Diborane. J. Am. Chem. Soc. 1961, 83 (6): 1515. doi:10.1021/ja01467a056.
- ^ Szieberth, Dénes; Szpisjak, Tamás; Turczel, Gábor; Könczöl, László. The stability of η2-H2 borane complexes – a theoretical investigation. Dalton Transactions. 19 August 2014, 43 (36): 13571–13577. PMID 25092548. doi:10.1039/C4DT00019F.
- ^ Tague, Thomas J.; Andrews, Lester. Reactions of Pulsed-Laser Evaporated Boron Atoms with Hydrogen. Infrared Spectra of Boron Hydride Intermediate Species in Solid Argon. Journal of the American Chemical Society. 1 June 1994, 116 (11): 4970–4976. doi:10.1021/ja00090a048.
- ^ Schreiner, Peter R.; Schaefer III, Henry F.; Schleyer, Paul von Ragué. The structure and stability of BH5. Does correlation make it a stable molecule? Qualitative changes at high levels of theory. The Journal of Chemical Physics. 1 June 1994, 101 (9): 7625. Bibcode:1994JChPh.101.7625S. doi:10.1063/1.468496.
- ^ A Life of Magic Chemistry: Autobiographical Reflections Including Post-Nobel Prize Years and the Methanol Economy, 159p