氯金酸
化合物
氯金酸也稱為四氯合金酸,是分子式為H[AuCl4]的無機化合物。
| 氯金酸 | |
|---|---|
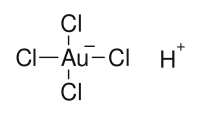
| |

| |
| 别名 | 四氯合金酸 |
| 识别 | |
| CAS号 | 16903-35-8 |
| ChemSpider | 26171 |
| SMILES |
|
| InChI |
|
| InChIKey | IXPWAPCEBHEFOV-ACHCXQQJAP |
| 性质 | |
| 化学式 | HAuCl4 |
| 摩尔质量 | 339.785 g/mol (無水) 393.833 g/mol (三水) 411.85 g/mol (四水) g·mol⁻¹ |
| 外观 | 金黃色晶體 潮解 |
| 密度 | 3.9 g/cm3 (四水) |
| 熔点 | 254°C |
| 溶解性(水) | 可溶 |
| 溶解性 | 可溶於乙醇、乙醚 |
| 危险性 | |
| 欧盟危险性符号 [1] | |
| 警示术语 | R:R22, R36, R37, R38[1] |
| MSDS | JT Baker |
| 欧盟分类 | 未列出 |
| NFPA 704 | |
| 相关物质 | |
| 其他阴离子 | 溴金酸 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
製備及結構
编辑- Au + HNO3 + 4 HCl → H[AuCl4] + NO↑ + 2 H2O
加熱時,氯金酸會分解為氯化氫及三氯化金,此反應是可逆反應,因此將三氯化金溶解在鹽酸中也可產生氯金酸。
- AuCl3 + HCl⇌H[AuCl4]
化学性质
编辑氯金酸會被大部分的金屬所還原,還原反應的速度很快,還原後的產物是元素態的金。
氯金酸能够表现出较强的氧化性。
氯金酸被二甲硫醚還原後會生成二甲硫醚氯化亚金,也常用來生成其他的含金配合物[4]。
氯金酸和氨或铵盐反应,可以得到灰色且具有强爆炸性的“雷金”,它被认为是Au2O3·3NH3和HNAuCl·NH3的混合物。过量氨和这种混合物反应,产生Au(OH)3·3NH3,用热水处理得到Au2O3·2NH3。[5]
應用
编辑膠體金及金的纳米顆粒一般可由檸檬酸鈉還原氯金酸溶液來製備,也可用其他的程序來製備奈米金,例如燙金過程使用的Norrish反應及乙醛还原反應[6]。
參考資料
编辑- ^ 1.0 1.1 MSDS of Chloroauric Acid
- ^ Handbook of Preparative Inorganic Chemistry, 2nd Ed. Edited by G. Brauer, Academic Press, 1963, NY. Vol. 1. p. 1057.
- ^ Greenwood, N. N.; & Earnshaw, A. (1997). Chemistry of the Elements (2nd Edn.), Oxford:Butterworth-Heinemann. ISBN 0-7506-3365-4.
- ^ Marie-Claude Brandys , Michael C. Jennings and Richard J. Puddephatt. Luminescent gold(I) macrocycles with diphosphine and 4,4-bipyridyl ligands. J. Chem. Soc., Dalton Trans. 2000, (24): 4601–4606. doi:10.1039/b005251p.
- ^ 钟兴厚 等. 无机化学丛书 第六卷 卤素 铜分族 锌分族. 科学出版社,2012.3. pp 468. 3.6.7 氮化物、叠氮化物、硝酸盐、磷化物和砷酸盐
- ^ Facile Photochemical Synthesis of Unprotected Aqueous Gold Nanoparticles Katherine L. McGilvray, Matthew R. Decan, Dashan Wang, and Juan C. Scaiano, J. Am. Chem. Soc.; 2006; 128(50) pp 15980 - 15981; (Communication) doi:10.1021/ja066522h
拓展阅读
编辑- Explosive Gold - Explosionandfire (页面存档备份,存于互联网档案馆)(视频). 氯金酸和氨水反应

