草酰二氨基丙酸
草酰二氨基丙酸(英語:Oxalyldiaminopropionic acid,ODAP),也称草酰氨基丙氨酸(英語:β-N-oxalylamino-L-alanine,BOAA),又称三七素(Dencichin),是一种存在于山黛豆(俗称草豌豆)中谷氨酸类神经递质结构类似物。它是导致运动神经退化综合征山黛豆中毒(Lathyrism)的神经毒素[1][2]。
| 草酰二氨基丙酸 | |
|---|---|
| |
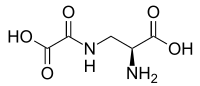
| 系统名 (2S)-2-Amino-3-(oxaloamino)propanoic acid | |
| 别名 |
|
| 识别 | |
| 缩写 |
|
| CAS号 | 7554-90-7 5302-45-4((S)) |
| PubChem | 2360 440259((S)) |
| ChemSpider | 389238 (S), 2270 (rac) |
| SMILES |
|
| 3DMet | B00693 |
| ChEBI | 16399 |
| KEGG | C04209 |
| MeSH | oxalyldiaminopropionic+acid |
| 性质 | |
| 化学式 | C5H8N2O5 |
| 摩尔质量 | 176.13 g·mol−1 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
来源
编辑ODAP在豆科植物山黛豆(Lathyrns sativus)种子中发现,含量为0.5 % w/w.[3]。山黛豆广泛分布于南欧、中欧和东欧、地中海盆地、伊拉克和阿富汗以及亚洲和非洲地区[4]。
历史
编辑在一些地区,包括印度次大陆、孟加拉国、埃塞俄比亚和尼泊尔,山黛豆已成为当地主食[4]。这种植物对环境条件的耐受性很高,因此在饥荒或干旱时期,它是唯一可用的食物来源。在干旱发生的几个月之后,可能会爆发神经性山黛豆中毒疫情[5]。最后一次发生这种疫情(截至2013年)是在埃塞俄比亚1995-1997年干旱期间[6],当时有2000人导致永久残疾[4]。
生物学效应
编辑ODAP是一种离子型AMPA谷氨酸受体激动剂[7][6]。已知它会引发人类神经性山黛豆中毒,这是一种运动神经退行性疾病,其特征是脊髓和控制腿部的皮质区域内的锥体束神经元退化,导致下半身麻痹和瘫痪[7]。目前尚无直接解释ODAP如何引发神经性山黛豆中毒,不过,有证据支持一些生物学效应。其作用机制尚不完全清楚的原因之一可能是到目前为止还没有找到一个良好的动物模型来研究ODAP对人类的影响[6]。其LD50也是未知的。
兴奋毒性
编辑ODAP激活AMPA受体,可诱发兴奋毒性或过度刺激谷氨酸受体。一次或长时间释放过多的谷氨酸会导致细胞质中Ca2+离子水平升高。由于Ca2+是释放谷氨酸进入突触的信号离子,这可能导致谷氨酸释放周期的强化和兴奋毒性损伤向邻近神经元的扩散。在神经元内部,额外的Ca2+会离开细胞质,进入线粒体或内质网中,导致错误折叠或未折叠的蛋白质在内质网中积累,并最终导致细胞死亡。除了作为激动剂外,有证据表明,ODAP还通过反向转运蛋白转运到细胞中,该反向转运蛋白还同时将谷氨酸转运到突触中[7]。
氧化应激
编辑ODAP的第二个生物学效应是产生氧化应激。人体在代谢过程中会在线粒体内产生活性氧物种,正常人体机制会将活性氧分子造成损害之前将其中和。氧化应激是由于这些途径的正常功能受到干扰而导致的。中和途径中的一种抗氧化剂是谷胱甘肽(GSH),其合成需要含硫氨基酸甲硫氨酸和半胱氨酸作为前体。人们认为ODAP诱发的兴奋毒性可能是ODAP通过其反向转运蛋白减少了半胱氨酸的摄入量,抑制了谷胱甘肽的合成,并最终导致产生的活性氧增加和线粒体损伤。运动神经元可能对ODAP中毒最敏感,因为它们对甲硫氨酸的依赖性更大。此外,山黛豆缺乏含硫氨基酸,因此在摄入时会增强ODAP造成的伤害[7]。
合成
编辑生物合成
编辑在未成熟的山黛豆中,ODAP由β-异噁唑啉-5-酮-2-基丙氨酸(BIA)作为前体合成得到。在成熟植物和种子种则没有BIA。其合成路径先由O-乙酰-L-丝氨酸(OAS)与异噁唑啉-5-酮合成BIA。BIA经过开环形成短暂的2,3-L-二氨基丙酸(DAPRO)中间体,中间体经草酰辅酶A形成ODAP[8]。
化学合成
编辑ODAP可以由L-α,β-二氨基丙氨酸与草酸二甲酯在pH为4.5-5的条件下合成得到。反应过程中可使用氧化铜临时保护L-α,β-二氨基丙氨酸中的α-氨基[3]。
参考文献
编辑- ^ 1.0 1.1 Woldeamanuel, Yohannes W.; Hassan, Anhar; Zenebe, Guta. Neurolathyrism: two Ethiopian case reports and review of the literature. Journal of Neurology. 2011-11-12, 259 (7): 1263–1268. ISSN 0340-5354. PMID 22081101. S2CID 27543906. doi:10.1007/s00415-011-6306-4 (英语).
- ^ 李志孝,孟延发,张立,陈耀祖. 山黧豆中α—及β—草酰二氨基丙酸相对含量的电泳测定及分离. 兰州大学学报. 1992, (03): 89–92. doi:10.13885/j.issn.0455-2059.1992.03.016.
- ^ 3.0 3.1 Rao, S; Adiga, P; Sarma, P. The Isolation and Characterization of β-N-Oxalyl-L-α,β-Diaminopropionic Acid: A Neurotoxin from the Seeds of Lathyrus sativus. Biochemistry. March 1964, 3 (3): 432–436. PMID 14155110. doi:10.1021/bi00891a022.
- ^ 4.0 4.1 4.2 Heuzé V., Tran G., Hassoun P., Lessire M., Lebas F., 2016. Grass pea (Lathyrus sativus). Feedipedia, a programme by INRA, CIRAD, AFZ and FAO. https://www.feedipedia.org/node/285 (页面存档备份,存于互联网档案馆) Last updated on April 19, 2016, 15:36
- ^ Lathyrus Research. Universiteit Gent. [April 8, 2015]. (原始内容存档于April 16, 2015).
- ^ 6.0 6.1 6.2 Singh, S; Rao, S. Lessons from neurolathyrism: A disease of the past & the future of Lathyrus sativus (Khesari dal). Indian Journal of Medical Research. July 2013, 138 (1): 32–37. PMC 3767245 . PMID 24056554.
- ^ 7.0 7.1 7.2 7.3 Moorhem, M; Lambein, F; Laybaert, L. Unraveling the mechanism of β-N-oxalyl-α,β-diaminopropionic acid (β-ODAP) induced excitotoxicity and oxidative stress, relevance for neurolathyrism prevention. Food and Chemical Toxicology. March 2011, 49 (3): 550–555. PMID 20510327. doi:10.1016/j.fct.2010.03.054.
- ^ Kuo, Y; Khan, J; Lambein, F. Biosynthesis of the neurotoxin β-odap in developing pods of Lathyrus sativus. Phytochemistry. March 1994, 35 (4): 911–913. Bibcode:1994PChem..35..911K. doi:10.1016/s0031-9422(00)90637-x.