钽
历史
编辑1802年,安德斯·古斯塔夫·埃克贝格(Anders Gustaf Ekeberg)在瑞典发现了钽元素。一年之前,查理斯·哈契特发现钶元素(Columbium,后改名为铌)。[5]1809年,英国化学家威廉·海德·沃拉斯顿对钽和钶的氧化物进行了对比,虽然得出不同的密度值,但他认为两者是完全相同的物质。[6]德国化学家弗里德里希·维勒其后证实了这一结果,因此人们以为钽和钶是同一种元素。另一德国化学家海因里希·罗泽(Heinrich Rose)在1846年驳斥这一结论,并称原先的钽铁矿样本中还存在着另外两种元素。他以希腊神话中坦塔洛斯的女儿尼俄伯(Niobe,泪水女神)和儿子珀罗普斯(Pelops)把这两种元素分别命名为“Niobium”和“Pelopium”。[7][8]后者其实是钽和铌的混合物,而前者则与先前哈契特所发现的钶相同。
1864年,克利斯蒂安·威廉·布隆斯特兰(Christian Wilhelm Blomstrand)、[9]亨利·爱丁·圣克莱尔·德维尔和路易·约瑟夫·特罗斯特(Louis Joseph Troost)明确证明了钽和铌是两种不同的化学元素,并确定了一些相关化合物的化学式。[9][10]瑞士化学家让-夏尔·加利萨·德马里尼亚(Jean Charles Galissard de Marignac)[11]在1866年进一步证实除钽和铌以外别无其他元素。然而直到1871年还有科学家发表有关第三种元素“Ilmenium”的文章。[12]1864年,德马里尼亚在氢气环境中加热氯化钽,从而经还原反应首次制成钽金属。[13]早期炼成的钽金属都含有较多的杂质。维尔纳·冯·博尔顿(Werner von Bolton)在1903年首次制成纯钽金属。钽曾被用作电灯泡灯丝,直到被钨淘汰为止。[14]
科学家最早使用分层结晶法把钽(七氟钽酸钾)从铌(一水合五氟氧铌酸钾)中提取出来。这一方法由德马里尼亚于1866年发现。今天科学家所用的则是对含氟化物的钽溶液进行溶剂萃取法。[10]
性质
编辑物理属性
编辑钽是一种灰蓝色[15]高密度坚硬金属,具高延展性、导热性和导电性。钽能抵抗酸的腐蚀,它在150 °C以下甚至能够抵抗王水的侵蚀。能够溶解钽的物质包括:氢氟酸、含氟离子和三氧化硫的酸性溶液以及氢氧化钾溶液。钽的熔点高达3017 °C(沸点5458 °C),只有钨、铼、锇和碳的熔点比它更高。
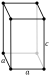
钽有两种晶体相,分别称为α和β。其中α态柔软,具延展性,晶体结构为体心立方(空间群为Im3m,晶格常数a = 0.33058 nm),努普硬度为200至400 HN,电阻率为15至60 µΩ⋅cm。β态则坚硬易碎,晶体结构属于四方晶系(空间群为P42/mnm,a = 1.0194 nm,c = 0.5313 nm),努普硬度为1000至1300 HN,电阻率为170至210 µΩ⋅cm。β态是一种亚稳态,在加温至750至775 °C后会转变为α态。钽金属块几乎完全由α态晶体组成,β态通常以薄片形式存在,可经磁控溅射、化学气相沉积或从共晶液态盐电化学沉积而得。[16]
化学属性
编辑钽可以形成氧化态为+5和+4的氧化物,分别为五氧化二钽(Ta2O5)和二氧化钽(TaO2),[17]其中五氧化二钽较为稳定。[17]五氧化二钽可以用来合成多种钽化合物,过程包括将其溶解在碱性氢氧化物溶液中,或与另一种金属氧化物一同熔化。如此形成的物质有钽酸锂(LiTaO3)和钽酸镧(LaTaO4)等。在钽酸锂中,钽酸离子TaO−
3并不出现,这其实代表TaO7−
6所形成的八面体钙钛矿骨架结构。钽酸镧则含有单个TaO3−
4四面体基。[17]
氟化钽可以用来从铌当中分离出钽元素。[18]钽的卤化物可以有+5、+4和+3氧化态,分别对应TaX
5、TaX
4和TaX
3型的化合物,另外还存在多核配合物以及亚化学计量化合物。[17][19]五氟化钽(TaF5)是一种白色固体,熔点为97.0 °C;五氯化钽(TaCl5)也是白色固体,熔点为247.4 °C。五氯化钽可以被水解,且在高温下可与更多的钽反应,形成吸湿性很强、呈黑色的四氯化钽(TaCl4)。钽的五卤化物可以用氢还原成三卤化物,但无法进一步还原成二卤化物。[17]钽﹣碲合金会形成准晶体。[17]2008年一份文章表示存在氧化态为−1的钽化合物。[20]
与其他难熔金属一样,最坚硬的钽化合物是其氮化物和碳化物。碳化钽(TaC)与碳化钨相似,都是十分坚硬的陶瓷材料,常被用于制造切割工具。氮化钽(III)在某些微电子生产过程中被用作薄膜绝缘体。[21]美国洛斯阿拉莫斯国家实验室的化学家研发出了一种碳化钽﹣石墨复合材料,这是人们已知最坚硬的物质之一。韩国科学家研发了一种比常见钢合金强2至3倍的无定形钽﹣钨﹣碳合金,其柔韧度也比钢更高。[22]铝化钽有两种:TaAl3和Ta3Al。两者均稳定、耐火、反射率高,因此有可能可用作红外线反射镜涂层。[23]
同位素
编辑自然产生的钽由两种稳定同位素组成:180mTa(0.012%)和181Ta(99.988%)。180mTa(“m”表示亚稳态)有三种理论预测的衰变方式:内转换至基态180Ta,β衰变成180W,或经电子捕获形成180Hf。不过,尚未有实验证明该同核异构体具有放射性。其半衰期至少有2.9×1017年。[24]180Ta基态的半衰期只有8小时。180mTa是唯一一种自然产生的同核异构体,也是全宇宙最稀有的同位素(经其他元素衰变产生及宇宙射线产生的短寿命同核异构体除外)。[25]
钽可以作为盐弹的“盐”(铬是另一种“盐”)。盐弹是一种假想的大杀伤力核武器。其外层(所谓的盐)由181Ta组成,会因内部核弹爆炸所产生的高能中子流而嬗变成182Ta。这一同位素的半衰期为114.4天,衰变时产生112万电子伏特(即1.12 MeV)的伽马射线。这可大大加强爆炸后数月之内辐射落尘的危害性。这种盐弹从未投入生产或测试,也因而未曾在战争中使用过。[26]
存量
编辑钽在地球地壳中的含量依重量计约为百万分之1[27]至2[19]。钽矿物有许多种,其中钽铁矿、细晶石、锡锰钽矿、黑稀金矿、复稀金矿等可作为工业钽开采的原石。钽铁矿(Fe, Mn)Ta2O6是最重要的钽原石。钽铁矿的结构和钶铁矿(Fe, Mn) (Ta, Nb)2O6相同。如果矿物中的钽比铌更多,则称钽铁矿,相反则称钶铁矿(或铌铁矿)。钽及其矿物的密度都很高,所以最适宜用重力分离方法进行萃取。其他含钽矿物还有铌钇矿和褐钇铌矿等等。
钽的开采主要集中在澳洲,环球卓越金属(Global Advanced Metals)在西澳大利亚拥有两座矿场,一座位于西南部格林布什,另一座位于皮尔布拉地区的沃吉纳。[28]巴西和加拿大是铌的主要产国,当地的矿石开采也会产出少量的钽元素。另外,中国、埃塞俄比亚和莫桑比克也是重要的钽产国。钽在泰国和马来西亚是锌开采过程的副产品。[10][29]未来估计最大的钽来源依次为:沙特阿拉伯、埃及、格林兰、中国、莫桑比克、加拿大、澳洲、美国、芬兰及巴西。[30][31]
钶铁矿和钽铁矿合称钶钽铁矿,[32]在中非有一定的存量。第二次刚果战争就与此有关。根据2003年10月23日的一份联合国报告,[33]钶钽铁矿的走私和运输使得当地战争得以持续。该战争自1998年以来已导致约540万人死亡,[34]是第二次世界大战以来死伤最为严重的军事冲突。刚果盆地战地的钶钽铁矿开采所引发的企业道德、人权及环境生态问题成为广受关注的议题。[35][36][37][38]虽然钶钽铁矿开采对刚果经济十分重要,但是刚果的钽产量却只是世界总产量的很少一部分。根据美国地质调查局的年报告,该地区的钽产量在2002至2006年期间占了不到世界总量的1%,在2000及2008年也只达到10%。[29]
根据目前的趋势预测,所有钽资源在50年以内会消耗殆尽,因此急需加大回收再用。[39]
生产
编辑钽从钽铁矿中的萃取过程有多个步骤。首先原石在压碎后经重力分离提高钽矿物的含量。这一步一般在矿场附近进行。
化学提炼
编辑钽矿石一般含有大量铌元素,因此两者都会经提炼后出售。整个湿法冶金过程由淋洗开始,矿石浸溶在氢氟酸和硫酸中,产生水溶氢氟化物。这样就可以把钽从各种非金属杂质中分离出来。
- Ta2O5 + 14 HF → 2 H2[TaF7] + 5 H2O
- Nb2O5 + 10 HF → 2 H2[NbOF5] + 3 H2O
氢氟化钽和氢氟化铌可经溶剂提取法从水溶液中提取出来,适用的有机溶剂包括环己酮和甲基异丁基酮。这一步会移除各种金属杂质(如铁、锰、钛、锆)的水溶氟化物。通过调节pH值可将钽从铌中分离出来。铌在有机溶剂中需较高的酸度才可溶解,因此在酸度较低的环境下可以轻易地移除。剩余的纯氢氟化钽溶液在经氨水中和之后,会形成氢氧化钽(Ta(OH)5),煅烧后产生五氧化二钽(Ta2O5)。[41]
- H2[TaF7] + 5 H2O + 7 NH3 → Ta(OH)5 + 7 NH4F
- 2 Ta(OH)5 → Ta2O5 + 5 H2O
氢氟化钽还可以与氟化钾反应形成七氟钽酸钾(K2[TaF7])
- H2[TaF7] + 2 KF → K2[TaF7] + 2 HF
它与钠在800 °C左右的熔融盐中会发生还原反应,从而制成钽金属。[42]
- K2[TaF7] + 5 Na → Ta + 5 NaF + 2 KF
更早期的一种分离方法在氢氟化物混合溶液中加入氟化钾,这种过程叫做德马里尼亚过程。
- H2[TaF7] + 2 KF → K2[TaF7] + 2 HF
- H2[NbOF5] + 2 KF → K2[NbOF5] + 2 HF
这样产生的K2[TaF7]和K2[NbOF5]具有不同的水溶性,所以能利用分离结晶法分开。
电解
编辑钽的电解提炼方法与霍尔-埃鲁电解炼铝法相似。与其不同的是,钽的电解提炼法的起始氧化物和金属产物都不是液态,而是固态粉末。这一方法由剑桥大学科学家于1997年发现。他们将少量金属氧化物置于熔融盐中,并用电流对其进行还原。阴极是金属氧化物的粉末,而阳极则由碳组成。电解质是处于1000 °C的熔融盐。首个利用这种方法的精炼厂可产出全球钽需求量的3至4%。[43]
加工
编辑钽的焊接必须在氩气或氦气等惰性环境下进行,以避免空气中其他气体对其造成污染。钽不可软焊,也很难磨碎,特别是已退火的钽金属。已退火的钽可延展性极高,能轻易制成薄片。[44]
应用
编辑电子
编辑钽的最大应用是用钽粉末制成的电子元件,以电容器和大功率电阻器为主。钽电解电容利用钽能够形成氧化物保护层的原理,以压制成圆球状的钽粉末作为其中一块“偏板”,以其氧化物作为介电质,并以电解质溶液或固体导电体作为另一块“偏板”。由于介电质层非常薄,所以每单位体积内能够达到很高的电容。这样的电容器体积小、重量轻,很适用于作为手提电话、电脑以及汽车内的电子元件。[45]
合金
编辑钽可用来制造各种熔点高的可延展合金。这些合金可作为超硬金属加工工具的材料,以及制造高温合金,用于喷射引擎、化学实验器材、核反应堆以及导弹当中。[45][46]钽具有高可延展性,能够拉伸成丝。这些钽丝被用于气化各种金属,如铝。钽可以抵御生物体液的侵蚀,又不会刺激组织,所以被广泛用来制造手术工具和植入体。例如,钽可以直接与硬组织成键,因此不少骨骼植入物都有多孔钽涂层。[47]
除了氢氟酸和热硫酸之外,钽能抵抗几乎所有酸的腐蚀。因此钽可以作化学反应容器以及腐蚀性液体导管的材料。氢氯酸加热过程所用的热交换线圈就是钽制的。[48]特高频无线电发射器电子管的生产用到大量的钽,钽可以捕获电子管中的氧和氮,分别形成氧化物和氮化物,从而保持所需的高真空状态。[18][48]
其他用途
编辑钽的熔点高,且能抵御氧化,所以可作真空炉部件的材料。许多抗腐蚀部件都需要用到钽,包括热电偶套管、阀体和扣件等等。由于钽的密度很高,所以锥形装药和爆炸成形弹头内层都可用钽制成。[49]钽可以大大提升锥形装药的装甲穿透能力。[50][51]氧化钽可用来制造高折射率相机镜片玻璃。
注释
编辑参考资料
编辑- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英语).
- ^ 2.0 2.1 Moseley, P. T.; Seabrook, C. J. The crystal structure of β-tantalum. Acta Crystallographica Section B Structural Crystallography and Crystal Chemistry (International Union of Crystallography (IUCr)). 1973-05-01, 29 (5): 1170–1171. ISSN 0567-7408. doi:10.1107/s0567740873004140.
- ^ Magnetic susceptibility of the elements and inorganic compounds (PDF). [2014-01-02]. (原始内容 (PDF)存档于2011-03-03)., in Handbook of Chemistry and Physics 81st edition, CRC press.
- ^ 欧里庇得斯,《欧瑞斯忒斯》
- ^ Griffith, William P.; Morris, Peter J. T. Charles Hatchett FRS (1765–1847), Chemist and Discoverer of Niobium. Notes and Records of the Royal Society of London. 2003, 57 (3): 299. JSTOR 3557720. doi:10.1098/rsnr.2003.0216.
- ^ Wollaston, William Hyde. On the Identity of Columbium and Tantalum. Philosophical Transactions of the Royal Society of London. 1809, 99: 246–252. JSTOR 107264. doi:10.1098/rstl.1809.0017.
- ^ Rose, Heinrich. Ueber die Zusammensetzung der Tantalite und ein im Tantalite von Baiern enthaltenes neues Metall. Annalen der Physik. 1844, 139 (10): 317–341 [2014-01-02]. Bibcode:1844AnP...139..317R. doi:10.1002/andp.18441391006. (原始内容存档于2013-06-20) (德语).
- ^ Rose, Heinrich. Ueber die Säure im Columbit von Nordamérika. Annalen der Physik. 1847, 146 (4): 572–577 [2014-01-02]. Bibcode:1847AnP...146..572R. doi:10.1002/andp.18471460410. (原始内容存档于2014-05-11) (德语).
- ^ 9.0 9.1 Marignac, Blomstrand, H. Deville, L. Troost und R. Hermann. Tantalsäure, Niobsäure, (Ilmensäure) und Titansäure. Fresenius' Journal of Analytical Chemistry. 1866, 5 (1): 384–389. doi:10.1007/BF01302537.
- ^ 10.0 10.1 10.2 Gupta, C. K.; Suri, A. K. Extractive Metallurgy of Niobium. CRC Press. 1994. ISBN 0-8493-6071-4.
- ^ Marignac, M. C. Recherches sur les combinaisons du niobium. Annales de chimie et de physique. 1866, 4 (8): 7–75 [2014-01-02]. (原始内容存档于2013-12-05) (法语).
- ^ Hermann, R. Fortgesetzte Untersuchungen über die Verbindungen von Ilmenium und Niobium, sowie über die Zusammensetzung der Niobmineralien(有關Ilmenium和鈮化合物以及鈮礦物成份的進一步研究). Journal für Praktische Chemie. 1871, 3 (1): 373–427. doi:10.1002/prac.18710030137 (德语).
- ^ Niobium. Universidade de Coimbra. [2008-09-05]. (原始内容存档于2007-12-10).
- ^ Bowers, B. Scanning Our Past from London The Filament Lamp and New Materials. Proceedings of the IEEE. 2001, 89 (3): 413. doi:10.1109/5.915382.
- ^ Colakis, Marianthe; Masello, Mary Joan. Tantalum. Classical Mythology & More: A Reader Workbook. 2007-06-30. ISBN 978-0-86516-573-1.
- ^ Lee, S; Doxbeck, M.; Mueller, J.; Cipollo, M.; Cote, P. Texture, structure and phase transformation in sputter beta tantalum coating. Surface and Coatings Technology. 2004,. 177–178: 44. doi:10.1016/j.surfcoat.2003.06.008.
- ^ 17.0 17.1 17.2 17.3 17.4 17.5 Holleman, A. F., Wiberg, E., Wiberg, N. Lehrbuch der Anorganischen Chemie, 102nd ed.. de Gruyter. 2007. ISBN 978-3-11-017770-1.
- ^ 18.0 18.1 Soisson, Donald J.; McLafferty, J. J.; Pierret, James A. Staff-Industry Collaborative Report: Tantalum and Niobium. Ind. Eng. Chem. 1961, 53 (11): 861–868. doi:10.1021/ie50623a016.
- ^ 19.0 19.1 Agulyansky, Anatoly. The Chemistry of Tantalum and Niobium Fluoride Compounds. Elsevier. 2004 [2008-09-02]. ISBN 978-0-444-51604-6.
- ^ Morse, Paige M.; Shelby, Quinetta D.; Kim, Do Young; Girolami, Gregory S. Ethylene Complexes of the Early Transition Metals: Crystal Structures of [HfEt
4(C
2H
4)2-
] and the Negative-Oxidation-State Species [TaEt
4(C
2H
4)3-
3] and [WH(C
2H
4)3-
4]. Organometallics (American Chemical Society (ACS)). 2008, 27 (5): 984–993. ISSN 0276-7333. doi:10.1021/om701189e. - ^ Tsukimoto, S.; Moriyama, M.; Murakami, Masanori. Microstructure of amorphous tantalum nitride thin films. Thin Solid Films. 1961, 460 (1–2): 222–226. Bibcode:2004TSF...460..222T. doi:10.1016/j.tsf.2004.01.073.
- ^ Arirang, TV. Researchers Develop New Alloy. Digital Chosunilbo (English Edition) : Daily News in English About Korea. 2005-05-06 [2008-12-22]. (原始内容存档于2008-03-28).
- ^ Braun, Hilarion "Substance for front surface mirror" 美国专利第5,923,464号, Issued on July 13, 1999
- ^ Majorana Collaboration. Constraints on the Decay of 180mTa. Physical Review Letters. 2023-10-11, 131 (15). ISSN 0031-9007. doi:10.1103/PhysRevLett.131.152501.
- ^ Georges, Audi; Bersillon, O.; Blachot, J.; Wapstra, A.H. The NUBASE Evaluation of Nuclear and Decay Properties. Nuclear Physics A (Atomic Mass Data Center). 2003, 729: 3–128. Bibcode:2003NuPhA.729....3A. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ Win, David Tin; Al Masum, Mohammed. Weapons of Mass Destruction (PDF). Assumption University Journal of Technology. 2003, 6 (4): 199–219 [2014-01-02]. (原始内容 (PDF)存档于2009-03-26).
- ^ Emsley, John. Tantalum. Nature's Building Blocks: An A-Z Guide to the Elements. Oxford, England, UK: Oxford University Press. 2001: 420. ISBN 0-19-850340-7.
- ^ Talison Tantalum eyes mid-2011 Wodgina restart 2010-06-09. Reuters. 2010-06-09 [2010-08-27]. (原始内容存档于2011-01-19).
- ^ 29.0 29.1 Papp, John F. 2006 Minerals Yearbook Nb & Ta. US Geological Survey. 2006 [2008-06-03]. (原始内容存档于2013-01-28).
- ^ M. J. Tantalum supplement (PDF). Mining Journal. 2007-November [2008-06-03]. (原始内容 (PDF)存档于2008-09-10).
- ^ International tantalum resources — exploration and mining (PDF). GSWA Mineral Resources Bulletin. (原始内容 (PDF)存档于2007-09-26).
- ^ Tantalum-Niobium International Study Center: Coltan (页面存档备份,存于互联网档案馆) Retrieved 2008-01-27
- ^ S/2003/1027. 2003-10-26 [2008-04-19]. (原始内容存档于2013-08-03).
- ^ Special Report: Congo. International Rescue Committee. [2008-04-19]. (原始内容存档于2012-03-05).
- ^ Hayes, Karen; Burge, Richard. Coltan Mining in the Democratic Republic of Congo: How tantalum-using industries can commit to the reconstruction of the DRC. : 1–64. ISBN 1-903703-10-7.
|journal=被忽略 (帮助) - ^ Dizolele, Mvemba Phezo. Congo's Bloody Coltan. Pulitzer Center on Crisis Reporting. January 6, 2011 [2009-08-08]. (原始内容存档于2016-11-27).
- ^ Congo War and the Role of Coltan. [2009-08-08]. (原始内容存档于2009-07-13).
- ^ Coltan mining in the Congo River Basin. [2009-08-08]. (原始内容存档于2009-03-30).
- ^ How much is left?. [2013-01-13]. (原始内容存档于2013-06-15).
- ^ U.S. Geological Survey, 存档副本. [2013-06-17]. (原始内容存档于2013-06-04).
- ^ Agulyanski, Anatoly. Chemistry of Tantalum and Niobium Fluoride Compounds. 1st ed. Burlington: Elsevier. 2004. ISBN 9780080529028.
- ^ Okabe, Toru H.; Sadoway, Donald R. Metallothermic reduction as an electronically mediated reaction. Journal of Materials Research. 1998, 13 (12): 3372–3377. Bibcode:1998JMatR..13.3372O. doi:10.1557/JMR.1998.0459.
- ^ Manufacturing metals: A tantalising prospect. The Economist. 2013-02-16 [2013-04-17]. (原始内容存档于2018-03-06).
- ^ Machining Tantalum. [June 16, 2011]. (原始内容存档于2012-02-25).
- ^ 45.0 45.1 Commodity Report 2008: Tantalum (PDF). United States Geological Survey. [2008-10-24]. (原始内容 (PDF)存档于2014-01-23).
- ^ Buckman Jr., R. W. New applications for tantalum and tantalum alloys. JOM Journal of the Minerals, Metals and Materials Society. 2000, 52 (3): 40. Bibcode:2000JOM....52c..40B. doi:10.1007/s11837-000-0100-6.
- ^ Cohen, R.; Della Valle, CJ; Jacobs, JJ. Applications of porous tantalum in total hip arthroplasty. Journal of the American Academy of Orthopaedic Surgeons. 2006, 14 (12): 646–55. PMID 17077337.
- ^ 48.0 48.1 Balke, Clarence W. Columbium and Tantalum. Industrial and Engineering Chemistry. 1935, 20 (10): 1166. doi:10.1021/ie50310a022.
- ^ Nemat-Nasser, Sia; Isaacs, Jon B.; Liu, Mingqi. Microstructure of high-strain, high-strain-rate deformed tantalum. Acta Materialia. 1998, 46 (4): 1307. doi:10.1016/S1359-6454(97)00746-5.
- ^ Walters, William; Cooch, William; Burkins, Matthew. The penetration resistance of a titanium alloy against jets from tantalum shaped charge liners. International Journal of Impact Engineering. 2001, 26: 823. doi:10.1016/S0734-743X(01)00135-X.
- ^ Russell, Alan M.; Lee, Kok Loong. Structure-property relations in nonferrous metals. Hoboken, NJ: Wiley-Interscience. 2005: 218. ISBN 978-0-471-64952-6.
- ^ Musikant, Solomon. Optical Glas Composition. Optical materials : an introduction to selection and application. New York: CRC Press; 1 edition (May 22, 1985). 1985. ISBN 978-0-8247-7309-0.
外部链接
编辑- 元素钽在洛斯阿拉莫斯国家实验室的介绍(英文)
- EnvironmentalChemistry.com —— 钽(英文)
- 元素钽在The Periodic Table of Videos(诺丁汉大学)的介绍(英文)
- 元素钽在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – 钽(英文)
- Tantalum-Niobium International Study Center (页面存档备份,存于互联网档案馆)
- CDC - NIOSH Pocket Guide to Chemical Hazards (页面存档备份,存于互联网档案馆)