鉻酰氟
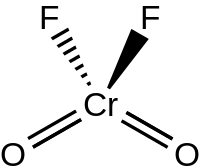
鉻酰氟是一種無機化合物,化學式 CrO2F2。它是一種紫紅色晶體(也有文獻報道為橙色晶體[2]),液態時為紅橙色。[3]
| 鉻酰氟 | |
|---|---|
| |
| IUPAC名 Difluoro(dioxo)chromium | |
| 別名 | 二氟二氧化鉻 |
| 識別 | |
| CAS號 | 7788-96-7 |
| PubChem | 53471881 |
| ChemSpider | 10329781 |
| SMILES |
|
| InChI |
|
| InChIKey | FRLBLFFATGQISB-UNDMLHRZAG |
| EINECS | 232-137-9 |
| 性質 | |
| 化學式 | CrF2O2 |
| 摩爾質量 | 121.99 g·mol−1 |
| 外觀 | 紫色晶體 |
| 熔點 | 31.6 °C(305 K) |
| 沸點 | 30 °C(303 K)(升華[1]) |
| 結構 | |
| 晶體結構 | 單斜 |
| 空間群 | P21/c, No. 14 |
| 危險性 | |
| 主要危害 | 氧化劑 |
| 相關物質 | |
| 相關化學品 | 鉻酰氯 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
結構
編輯液態和氣態的 CrO2F2 都是四面體型的,對稱群 C2v,這類似於鉻酰氯。[4]鉻酰氟在固態下二聚成含有橋接氟的二聚體(O2Cr(μ-F)4CrO2),空間群 P21/c。其中的 Cr=O 鍵長為 157 pm,Cr–F 鍵長則為 181.7、186.7和209.4 pm。鉻是六配位的,為扭曲八面體型結構。[5]
歷史和製備
編輯純鉻酰氟於 1952年首次分離,由Alfred Engelbrecht和Aristid von Grosse報告。[6]在19世紀早期,加熱螢石、鉻酸鹽和硫酸的混合物時,它首次以紅色蒸汽的形式被觀察到。這些紅色蒸汽最初被認為是CrF6,儘管一些化學家認為這是結構類似 CrO2Cl2的CrO2F2。[6]Fredenhagen 研究氟化氫與鹼金屬鉻酸鹽的反應,第一次成功合成鉻酰氟。後來,von Wartenberg 通過用氟氣處理鉻酰氯來製備不純的 CrO2F2。[7]Wiechert進行了另一次嘗試,它在 -40℃下用HF處理重鉻酸鹽,產生不純的CrO2F2液體。
Engelbrecht 和von Grosse的CrO2F2製備方法包括三氧化鉻被氟化劑氟化:[6]
- CrO3 + 2 HF → CrO2F2 + H2O
這個反應是可逆的,水會重新把 CrO2F2水解成CrO3。
- CrO3 + 2 ClF → CrO2F2 + Cl2 + O2
- CrO3 + COF2 → CrO2F2 + CO2
- CrO3 + MF6 → CrO2F2 + MOF4 (M = Mo, W)
最後一種方法涉及鎢和鉬的六氟化物。據Green和Gard報道,該方法是獲得大量純CrO2F2非常簡單和有效的途徑。[3]在120 °C下,產率是100%。正如從MoF6和WF6的相對反應性所預期的那樣,六氟化鉬的反應比六氟化鎢更容易進行。[8]
反應
編輯鉻酰氟是一種強氧化劑,可以把烴氧化成酮或羧酸。它也可以用來製備其它鉻酰化合物。[3]類似其它氟化物,CrO2F2 與玻璃和石英反應,因此需要無硅塑料或金屬容器來處理它。它在無機系統中的氧化性也已被探索。[9]鉻酰氟可以和金屬氧化物反應:
- CrO2F2 + MO → MF2 + CrO3
鉻酰氟也會把硼和硅的氧化物變成氟化物。[9]
在全氟庚烷溶劑中,鉻酰氟會於鹼金屬和鹼土金屬的氟化物,產生橙色的氟鉻酸鹽:[9]
- CrO2F2 + 2 MF → M2CrO2F4
鉻酸氟和路易斯酸反應,從酸酐中得到羧基類配體並產生酰氟副產物:[9]
- CrO2F2 + 2 (CF3CO)2O → CrO2(CF3COO)2 + 2 CF3COF
參考資料
編輯- ^ Brauer, Georg. Chromyl Fluoride – CrO
2F
2. Handbook of Preparative Inorganic Chemistry, Volume 1 2nd. Stuttgart; New York: Ferdinand Enke Verlag; Academic Press, Inc. 1963: 258–259 [1960] [2021-07-24]. ISBN 978-0-32316127-5. (原始內容存檔於2021-08-27). - ^ Hubert Schmidbaur, W. H. Eugen Schwarz. Permanganyl Fluoride: A Brief History of the Molecule MnO 3 F and of Those Who Cared For It. Chemistry – A European Journal. 2021-04-21, 27 (23): 6848–6859 [2022-06-27]. ISSN 0947-6539. PMC 8247864 . PMID 33219726. doi:10.1002/chem.202004759 (英語).
- ^ 3.0 3.1 3.2 Gard, G. L. (1986) "Chromium Difluoride Dioxide (Chromyl Fluoride)," Inorg. Synth., 24, 67-69, doi:10.1002/9780470132555.ch20.
- ^ Hobbs, W. E. (1958) "Infrared Absorption Spectra of Chromyl Fluoride and Chromyl Chloride," J. Chem. Phys. 28(6), 1220-1222, doi:10.1063/1.1744372.
- ^ Supeł, J.; Abram, U.; Hagenbach, A.; Seppelt, K. (2007) "Technetium Fluoride Trioxide, TcO3F, Preparation and Properties." Inorg. Chem., 46(14), 5591–5595, doi:10.1021/ic070333y.
- ^ 6.0 6.1 6.2 Engelbrecht, A.; von Grosse, A. (1952) "Pure Chromyl Fluoride," J. Am. Chem. Soc. 74(21), 5262–5264, doi:10.1021/ja01141a007.
- ^ von Wartenberg, H. (1941) "Über höhere Chromfluoride (CrF
4, CrF
5 und CrO
2F
2)" [About higher chromium fluorides (CrF
4, CrF
5 and CrO
2F
2)], Z. Anorg. Allg. Chem. [in German], 247(1-2), 135–146, doi:10.1002/zaac.19412470112. - ^ Green, P. J.; Gard, G. L. (1977) "Chemistry of Chromyl Fluoride. 5. New Preparative routes to CrO2F2," Inorg. Chem. 16(5), 1243–1245, doi:10.1021/ic50171a055.
- ^ 9.0 9.1 9.2 9.3 Brown, S. D.; Green, P.J.; Gard, G.L. (1975) "The Chemistry of Chromyl Fluoride III: Reactions with Inorganic Systems," J. Fluorine Chem. 5(3), 203-219, doi:10.1016/S0022-1139(00)82482-3.