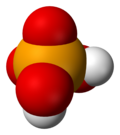
硒酸
化合物
硒酸是一種無機酸,化學式為H2SeO4。它是硒的含氧酸,它的結構可以更準確地被描述為(HO)2SeO2。
| 硒酸 | |||
|---|---|---|---|
| |||

| |||
| IUPAC名 Selenic(VI) acid | |||
| 識別 | |||
| CAS號 | 7783-08-6 | ||
| PubChem | 1089 | ||
| ChemSpider | 1058 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | QYHFIVBSNOWOCQ-UHFFFAOYAI | ||
| ChEBI | 18170 | ||
| RTECS | VS6575000 | ||
| KEGG | C05697 | ||
| 性質 | |||
| 化學式 | H 2SeO 4 | ||
| 摩爾質量 | 144.9734 g·mol⁻¹ | ||
| 外觀 | 無色潮解性晶體 | ||
| 密度 | 2.95 g/cm3(固態) | ||
| 熔點 | 58 °C (331 K) | ||
| 沸點 | 260 °C (533 K) (分解) | ||
| 溶解性(水) | 130 g/100 mL (30 °C) | ||
| pKa | -3.00 | ||
| 折光度n D |
1.5174 (D-line, 20 °C) | ||
| 結構 | |||
| 分子構型 | 硒為四面體形 | ||
| 危險性 | |||
| H-術語 | H301, H315, H318, H331, H373, H410 | ||
| P-術語 | P260, P261, P264, P270, P271, P273, P280, P301+310, P302+352, P304+340, P305+351+338, P310, P311, P314 | ||
| 主要危害 | 刺激性,高毒 | ||
| NFPA 704 | |||
| 相關物質 | |||
| 其他陰離子 | 亞硒酸 氫硒酸 硒化氫 | ||
| 其他陽離子 | 硒酸鈉 硒酸鉀 | ||
| 相關化學品 | 硫酸 二氧化硒 三氧化硒 碲酸 | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
製備
編輯由於三氧化硒的不穩定性,不像三氧化硫溶於水生成硫酸,通過在水中溶解三氧化硒得到硒酸是不切實際的。[1]相反地,硒酸必須通過氧化低價態的硒化合物來製取。
SeO2 + H2O2 → H2SeO4
無水硒酸被公認為晶體,它可以由硒酸的溶液在140°C (413 K; 284 °F)溫度下真空蒸發。[3]
硒酸也可以通過亞硒酸(H2SeO3)被鹵素(如氯氣或溴)或高錳酸鉀氧化製取。[4]然而,用氯氣或者溴作為氧化劑會產生鹽酸或者氫溴酸作為副產物,它們需要從溶液中去除,因為它們可以將硒酸還原成亞硒酸。[5]
另一種製備硒酸的方法是將單質硒在水中的懸濁液用氯氣氧化:[4]
Se + 4 H2O + 3 Cl2 → H2SeO4 + 6 HCl
化學性質
編輯類似硫酸,硒酸是一種強酸,有吸濕性,在水中溶解度很強。其濃溶液是粘稠的。已知硒酸有一水合物和二水合物。[4]一水合物的熔點在26°C,而二水合物的熔點在−51.7°C。[1]
硒酸的氧化性比硫酸強,50%硒酸能將氯離子氧化成氯氣,而自身被還原成亞硒酸或二氧化硒(但氯氣能夠將稀亞硒酸氧化為硒酸):[4]
- H2SeO4 + 2 H+ + 2 Cl− → H2SeO3 + H2O + Cl2
硒酸在200°C以上分解,放出氧氣,自身被還原成亞硒酸:[4]
- 2 H2SeO4 → 2 H2SeO3 + O2
硒酸可以和鋇鹽反應生成沉澱BaSeO4,沉澱和硫酸鋇的性質類似。總體上說,硒酸鹽和硫酸鹽的性質相似,但是在水中的溶解性更好。許多硒酸鹽有相同的、和硫酸鹽一致的晶體結構。[1]
- H2SeO4 + 2 HSO3F → SeO2F2 + 2 H2SO4
熱的濃硒酸可以溶解單質金,產生紅黃色的硒酸金(III):[6]
- 2 Au + 6 H2SeO4 → Au2(SeO4)3 + 3 H2SeO3 + 3 H2O
後來,人們發現這種紅黃色的物質其實是Au2(SeO3)2(SeO4),其中硒的價態被IR和NMR確定。因此,其反應方程式應該為:[7]
- 2 Au + 4 H2SeO4(濃) → Au2(SeO3)2(SeO4) + H2SeO3 + 3 H2O
參考資料
編輯- ^ 1.0 1.1 1.2 1.3 Don M. Yost. Systematic Inorganic Chemistry. READ BOOKS. 2007: 343–346. ISBN 1-4067-7302-6.
- ^ Mathias S. Wickleder. Francesco A. Devillanova , 編. Handbook of chalcogen chemistry: new perspectives in sulfur, selenium and tellurium. Royal Society of Chemistry. 2007: 353. ISBN 0-85404-366-7.
- ^ 3.0 3.1 Seppelt, K. 「Selenoyl difluoride」 Inorganic Syntheses, 1980, volume XX, pp. 36-38. ISBN 0-471-07715-1. The report describes the synthesis of selenic acid.
- ^ 4.0 4.1 4.2 4.3 4.4 Anil Kumar De. A Text Book of Inorganic Chemistry. New Age International. 2003: 543–545. ISBN 81-224-1384-6.
- ^ Lenher, Victor; Kao, C. H. THE PREPARATION OF SELENIC ACID AND OF CERTAIN SELENATES. Journal of the American Chemical Society (American Chemical Society (ACS)). 1925, 47 (6): 1521–1522. ISSN 0002-7863. doi:10.1021/ja01683a005.
- ^ Lenher, Victor. ACTION OF SELENIC ACID ON GOLD.1. Journal of the American Chemical Society (American Chemical Society (ACS)). 1902, 24 (4): 354–355. ISSN 0002-7863. doi:10.1021/ja02018a005.
- ^ Wickleder, Mathias S.; Büchner, Oliver; Wickleder, Claudia; el Sheik, Sherif; Brunklaus, Gunther; Eckert, Hellmut. Au2(SeO3)2(SeO4): Synthesis and Characterization of a New Noncentrosymmetric Selenite−Selenate. Inorganic Chemistry (American Chemical Society (ACS)). 2004, 43 (19): 5860–5864. ISSN 0020-1669. doi:10.1021/ic049270z.
- ^ 劉新錦等.無機元素化學(第二版) 氧族元素.北京:科學出版社.2010.01 ISBN 978-7-03-026399-5