神经元黏附分子
神经元吸附分子 (Neural Cell Adhesion Molecule, NCAM, 又称为表面抗原分化簇-56 CD56) 是一种同类亲和性的吸附蛋白,换言之同样在细胞膜上表现这种糖蛋白的细胞倾向于相互黏附。这类细胞包括神经元、神经胶质细胞、骨骼肌细胞与自然杀手细胞。现有证据显示 NCAM 在细胞间的吸附[1]、神经元突触形成(包含树突与轴突)、神经突触可塑性(synaptic plasticity)、于是亦同大脑学习与记忆形成功能相关。
| Neural cell adhesion molecule 1 神经元黏附分子1 | |||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
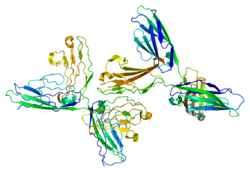 PDB rendering based on 1epf. | |||||||||||||
| |||||||||||||
| 标识 | |||||||||||||
| 代号 | NCAM1; CD56; MSK39; NCAM | ||||||||||||
| 扩展标识 | 遗传学:116930 鼠基因:97281 同源基因:40754 GeneCards: NCAM1 Gene | ||||||||||||
| EC编号 | 2.7.11.1 | ||||||||||||
| RNA表达模式 | |||||||||||||
 | |||||||||||||
 | |||||||||||||
| 更多表达数据 | |||||||||||||
| 直系同源体 | |||||||||||||
| 物种 | 人类 | 小鼠 | |||||||||||
| Entrez | 4684 | 17967 | |||||||||||
| Ensembl | ENSG00000149294 | ENSMUSG00000039542 | |||||||||||
| UniProt | P13591 | P13595 | |||||||||||
| mRNA序列 | NM_000615 | NM_001081445 | |||||||||||
| 蛋白序列 | NP_000606 | NP_001074914 | |||||||||||
| 基因位置 |
Chr 11: 112.83 – 113.15 Mb |
Chr 9: 49.5 – 49.8 Mb | |||||||||||
| PubMed查询 | [1] | [2] | |||||||||||
型态、结构域(domains)与同类亲合性(homophilic)
编辑NCAM 属于免疫球蛋白超家族 (Immunoglobulin superfamily, IgSF)中的一类糖蛋白。在转译过程中NCAM的编码mRNA透过可变剪接(alternatve splicing)的机制,被裁切成(从中切除并依序黏起,一般并不调换顺序或重组,故类似电影剪接胶卷之过程)至少27种同位形(isoforms),提供NCAM分子丰富之多型性。[2]
三种主要的NCAM同位形,它们之间差别仅在于处于细胞质一端的结构域不同(cytoplasmic domain):
- NCAM-120kDa(无胞内结构域,由糖磷脂酰肌醇 (Glycophosphatidylinositol,GPI)锚定在细胞外表面)
- NCAM-140kDa(胞内结构域较短)
- NCAM-180kDa(胞内结构域较长)
NCAM位于细胞外的部分包含五个类免疫球蛋白结构域(Ig domains),以及两个III型纤维黏接蛋白(fibronectin-III, FNIII)结构域。Ig-like domains 与同类亲和性有关,FNIII domains 则和神经突触的生长与外延有关。
NCAM分子的同类亲合特性有两种结合方式,分别是相对(trans)与相邻(cis),目前对于NCAM的分子机构是怎样使两种组态都能具有亲和性(同时又具有专一性)只有初步的结论,已被提出的一个模型[3]说明当两者以trans位互相结合时,五个Ig domains以反向平行的方式(54321对12345)结合,或者只使用前端的IgI, IgII 互相结合(如小指头打勾状);当以cis位结合时只牵涉到IgI对III,或IgI对II的结合,但多对NCAM分子之间却可以形成多聚复合体藉以稳定结合。两种结合方式的NCAM分子都可以发出促进之信号,以利前述之神经元突触生长。
次要外显子
编辑给予NCAM另一层次复杂性的,是所谓的次要外显子,在前述的RNA剪接过程中会被加入,因而出现在最后表现的蛋白中以改变其特性:
- VASE (VAriable domain Spliced Exon 可变结构域切割外显子) 被认为与抑制前述神经元突触诱生作用有关。
- MSD (Muscle Specific Domain 骨骼肌特异结构域) 被认为与骨骼肌原母细胞之融合有关 [4]
MSD外显子之产物,在骨骼肌处出现在全部三种(前述的)同位形当中,于是使这些蛋白亚型的分子量高于不表现MSD者,于是对应到 的是 NCAM-125, NCAM-145, 和 NCAM-185同位形。但最常见的是 NCAM-125。[4]
转译后修饰
编辑主要是在IgV Domains上加上多聚唾液酸(polysialic acid,PSA),这种修饰被认为会削除NCAM的同类亲合活性,于是可能在细胞的迁移(migration)与侵入(invasion)扮演重要角色。 多聚唾液酸修饰已证明对学习与记忆的形成有至关重大的影响--使用内神经氨酸苷酶(endoneuraminidase,EndoN)移除海马回处神经元NCAM分子上的修饰后,长期增益性作用(Long-term potentiation, LTP)与长期抑势作用(Long-term depression, LTD)的形成都受到显著损害。[5][6][7]
功能
编辑NCAM 引发突触生长被认为是借由成纤维细胞生长因子受体(FGFR)并触发 p59Fyn讯息路径。
病理
编辑在解剖病理学领域,病理学家使用CD56(NCAM)作为特定肿瘤型态之标记。经免疫组织染色(immunohistochemistry)后显现者包含:
Anti-NCAM 疗法
编辑NCAM 曾被用于实验性的癌症免疫治疗的标靶分子,并使用放射性免疫结合物 123J-UJ13a or 131J-UJ13a 成功的在儿童身上定位了转移的神经母细胞癌(neuroblastoma)。
在两项临床试验中,罹患小细胞肺癌之患者被给予抗-NCAM之免疫毒性蛋白huN901-DM1,而得到接受范围以内的毒性与可观察到的临床反应。[8]
参考文献
编辑- ^ Pathology Outlines. [2011-11-09]. (原始内容存档于2018-02-20).
- ^ Reyes AA, Small SJ, Akeson R. At least 27 alternatively spliced forms of the neural cell adhesion molecule mRNA are expressed during rat heart development. Mol Cell Biol. 1991, 11 (3): 1654–61. PMC 369464 . PMID 1996115.
- ^ 存档副本. [2011-11-09]. (原始内容存档于2021-11-18).
- ^ 4.0 4.1 Suzuki M, Angata K, Nakayama J, Fukuda M. Polysialic acid and mucin type o-glycans on the neural cell adhesion molecule differentially regulate myoblast fusion. J Biol Chem. 2003, 278 (49): 49459–68. PMID 13679364. doi:10.1074/jbc.M308316200.
- ^ Becker, C. G., Artola, A., Gerardy-Schahn, R., Becker, T., Welzl, H., and Schachner, M. The polysialic acid modification of the neural cell adhesion molecule is involved in spatial learning and hippocampal long-term potentiation. J Neurosci Res. 1996, 45 (2): 143–52. PMID 8843031. doi:10.1002/(SICI)1097-4547(19960715)45:2<143::AID-JNR6>3.0.CO;2-A.
- ^ Stoenica L, Senkov O, Gerardy-Schahn R, Weinhold B, Schachner M, Dityatev A. In vivo synaptic plasticity in the dentate gyrus of mice deficient in the neural cell adhesion molecule NCAM or its polysialic acid. Eur J Neurosci. 2006, 23 (9): 2255–64. PMID 16706834. doi:10.1111/j.1460-9568.2006.04771.x.
- ^ Senkov O, Sun M, Weinhold B, Gerardy-Schahn R, Schachner M, Dityatev A. Polysialylated neural cell adhesion molecule is involved in induction of long-term potentiation and memory acquisition and consolidation in a fear-conditioning paradigm. J Neurosci. 2006, 26 (42): 10888–109898. PMID 17050727. doi:10.1523/JNEUROSCI.0878-06.2006.
- ^ Jensen M, Berthold F. Targeting the neural cell adhesion molecule in cancer. Cancer Lett. 2007, 258 (1): 9–21. PMID 17949897. doi:10.1016/j.canlet.2007.09.004.
外部链接
编辑