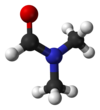
二甲基甲醯胺
二甲基甲醯胺(英語:Dimethylformamide,縮寫DMF)是一種能和水及大部分有機溶劑互溶的透明液體。它是化學反應的常用溶劑。純二甲基甲醯胺是沒有氣味的,但工業級或變質的二甲基甲醯胺則有魚腥味,因其含有二甲基胺的不純物。名稱來源是由於它是甲醯胺(甲酸的醯胺)的二甲基取代物,而二個甲基都位於N(氮)原子上。
| N,N-二甲基甲醯胺 | |||
|---|---|---|---|
| |||

| |||
| IUPAC名 N,N-二甲基甲醯胺 | |||
| 別名 | N,N-二甲基甲醯胺 DMF DMFA | ||
| 識別 | |||
| CAS號 | 68-12-2 | ||
| SMILES |
| ||
| RTECS | LQ2100000 | ||
| 性質 | |||
| 化學式 | C3H7NO | ||
| 莫耳質量 | 73.09 g·mol⁻¹ | ||
| 外觀 | 透明無色液體 | ||
| 密度 | 0.944 g/cm3,液體 | ||
| 熔點 | −61 °C(−78 °F;212 K) | ||
| 沸點 | 153 °C(307 °F;426 K) | ||
| 溶解性(水) | 無限混溶 | ||
| 折光度n D |
1.4305 (20 °C), εr = 36.71 (25°C) | ||
| 黏度 | 0.92 cP(20 °C) | ||
| 結構 | |||
| 偶極矩 | 3.86 D D (25 °C) | ||
| 危險性 | |||
| 歐盟危險性符號 | |||
| 警示術語 | R:R61-R20/21-R36 | ||
| 安全術語 | S:S53-S45 | ||
| MSDS | ScienceLab.com | ||
| 主要危害 | 易燃 | ||
| NFPA 704 | |||
| 閃點 | 58 °C(136 °F;331 K) | ||
| 相關物質 | |||
| 相關醯胺 | 乙醯胺 甲醯胺 六甲基磷醯胺 | ||
| 相關化學品 | 二甲基亞碸 乙腈 | ||
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |||
二甲基甲醯胺是高沸點的極性(親水性)非質子性溶劑,能促進SN2反應機構的進行。 二甲基甲醯胺是利用甲酸和二甲基胺製造的。二甲基甲醯胺在強鹼如氫氧化鈉或強酸如鹽酸或硫酸的存在下是不穩定的(尤其在高溫下),並水解為甲酸與二甲基胺。
用途
編輯N,N-二甲基甲醯胺主要用作一低揮發性的溶劑。N,N-二甲基甲醯胺被用於聚丙烯腈纖維及塑料的製造上。在製藥工業中,它也用於製造殺蟲劑、接著劑、人造皮革、纖維、軟片及表面塗裝等。[1]
N,N-二甲基甲醯胺是Bouveault醛合成反應及Vilsmeier-Haack反應(另一有用的醛類合成反應)的試劑。[2]它也可在反應中用作氰基、甲醯基、二甲氨基、二甲氨基甲基、二甲氨基羰基、羰基或甲酸根的提供者。[3]
在核磁共振光譜中,N,N-二甲基甲醯胺的甲基上的質子形成二個單峰,因為在核磁共振的時間尺度中,羰基碳-氮鍵的旋轉速率很慢。羰基碳-氮鍵的鍵級大於一,而醯胺碳-氧鍵的鍵級則小於二。醯胺的紅外線光譜中,C=O帶通常在小於1700cm−1處,因其C=O鍵因為從氮供給氧的電子密度而減弱。
安全
編輯在二甲基甲醯胺中使用氫化鈉進行反應具有一定的危險性。有報導指出在26°C的低溫下,仍發生放熱的分解反應。在實驗室規模中,任何熱量的釋放(通常)很快會被發現並使用冰浴加以控制,因此二甲基甲醯胺與氫化鈉的組合仍十分常用。然而,在試驗工廠規模下曾有許多事故發生。
毒性
編輯二甲基甲醯胺黏稠而難以蒸發,是十分令人煩惱的溶劑,在許多反應中,可用二甲基亞碸來代替。許多製造商在安全資料表中,將N,N-二甲基甲醯胺的健康危害列為(終身)或(慢性),因為二甲基甲醯胺不太容易被人體排出。
根據國際癌症研究機構(IARC),N,N-二甲基甲醯胺是2A類致癌物。[4]二甲基甲醯胺(DMF)經各種途徑吸收後,主要由肝內代謝,排泄較快,主要目標器官為肝臟 ,腎臟也有一定損害。主要經肝內微粒體混合功能氧化酶進行脫甲基化作用,脫去一個甲基,代謝產物為一甲基甲醯胺和甲醯胺,代謝迅速;甲醯胺在血中滯留稍長,進而代謝為甲酸和氨排出。部分二甲基甲醯胺以原形物從尿和呼氣排出。
防護措施
編輯呼吸制度防護: 氧氣中純度超標時,佩戴自吸淨化式防毒面具。佩戴氧氣呼吸器。眼睛防護: 戴化工安全防護眼鏡。身上防護: 穿防靜電工作。手防護: 戴橡膠手套。其他: 工作現場嚴禁抽菸、進食和飲水。工作完畢,淋浴更衣。
參考資料
編輯- ^ Redlich, C; Beckett, W. S.; Sparer, J.; Barwick, K. W.; Riely, C. A.; Miller, H.; Sigal, S. L.; Shalat, S. L.; and Cullen, M. R.; 1988. Liver disease associated with occupational exposure to the solvent dimethylformamide. Ann. Intern. Med. 108:680-686.
- ^ Jacques Muzart. N,N-Dimethylformamide: much more than a solvent. Tetrahedron. 2009-10, 65 (40): 8313–8323 [2022-10-05]. doi:10.1016/j.tet.2009.06.091. (原始內容存檔於2022-12-23) (英語).
- ^ Shengtao Ding, Ning Jiao. N , N -Dimethylformamide: A Multipurpose Building Block. Angewandte Chemie International Edition. 2012-09-10, 51 (37): 9226–9237 [2022-10-05]. doi:10.1002/anie.201200859. (原始內容存檔於2022-10-08) (英語).
- ^ List of Classifications, Agents classified by the IARC Monographs, Volumes 1–124. IARC Monographs on the Evaluation of Risk to Humans. IARC. July 7, 2019 [July 14, 2019]. (原始內容存檔於2020-05-20).
外部連結
編輯- 二甲基甲醯胺在 有機合成 上的應用
- 簡明國際化學品評估文件31: N,N-二甲基甲醯胺(頁面存檔備份,存於網際網路檔案館)
- 二甲基甲醯胺的 物質安全資料表(頁面存檔備份,存於網際網路檔案館)
- 二甲基甲醯胺慢性毒性摘要 (PDF)
- Chemical Book N,N-二甲基甲醯胺(頁面存檔備份,存於網際網路檔案館)