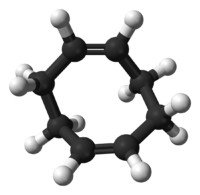
1,5-環辛二烯
1,5-環辛二烯是一種有機化合物,化學式為C8H12,通常可以簡寫成COD。這種二烯烴是製備其他有機物的重要前體,並在金屬有機化學用作配體。[2][3]
| 1,5-環辛二烯 | |
|---|---|

| |
| |
| IUPAC名 Cycloocta-1,5-diene[1] | |
| 識別 | |
| CAS號 | 111-78-4 |
| ChemSpider | 74815 |
| SMILES |
|
| InChI |
|
| InChIKey | VYXHVRARDIDEHS-QGTKBVGQBM |
| EC編號 | 203-907-1 |
| 性質 | |
| 化學式 | C8H12 |
| 摩爾質量 | 108.18 g·mol−1 |
| 外觀 | 澄清無色液體 |
| 密度 | 0.882 g cm−3(液態) |
| 熔點 | -69.5 °C(204 K) |
| 沸點 | 151 °C(424 K) |
| 溶解性(水) | - |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
合成
編輯1,5-環辛二烯可由1,3-丁二烯在鎳催化劑作用下二聚製得,同時得到的副產物還有乙烯基環己烯。2005年時全球大約生產了10,000噸1,5-環辛二烯。[4]
有機反應
編輯1,5-環辛二烯與乙硼烷二甲基硫醚加合物(相當於甲硼烷)反應產生9-硼二環[3.3.1]壬烷,[5] 後者簡稱9-BBN,是有機化學中用於硼氫化反應的試劑:
1,5-環辛二烯與二氯化硫或類似試劑加成得到2,6-二氯代-9-硫代雙環[3.3.1]壬烷:[6]
金屬配合物
編輯1,5-環辛二烯可以與低價金屬通過碳碳雙鍵形成典型的不飽和烴配合物。配合物Ni(cod)2是製備多種Ni(0)和Ni(II)配合物的前體。金屬環辛二烯配合物很具有吸引力,因為它們足夠穩定可以被分離出來,穩定性通常超過類似的乙烯配合物。環辛二烯配合物的穩定性是螯合效應造成的。環辛二烯配體很容易被其他配體取代,例如膦。
Ni(COD)2可以在環辛二烯配體存在條件下,用三乙基鋁還原無水二(乙醯丙酮)合鎳製得[8]:
- 1/3 [Ni(C5H7O2)2]3 + 2 COD + 2 Al(C2H5)3 → Ni(COD)2 + 2 Al(C2H5)2(C5H7O2) + C2H4 + C2H6
類似的Pt(COD)2需要用迂迴的路線製備,反應中需使用環辛四烯基二鋰[9]:
- Li2C8H8 + PtCl2(COD) + 3 C7H10 → [Pt(C7H10)3] + 2 LiCl + C8H8 + C8H12
- Pt(C7H10)3 + 2 COD → Pt(COD)2 + 3 C7H10
目前已有大量關於環辛二烯配合物的研究報道,其中許多發表在無機合成(Inorganic Syntheses)第25、26和28卷上。鉑配合物已經使用在許多配合物的合成中:
- Pt(COD)2 + 3 C2H4 → Pt(C2H4)3 + 2 COD
環辛二烯配合物是有用的起始原料,以下反應是一個值得注意的例子:
- Ni(cod)2 + 4 CO(g) Ni(CO)4 + 2 COD
生成物Ni(CO)4有劇毒,因此在反應容器中生成它比直接配製更安全。其他低價金屬的環辛二烯配合物包括Mo(COD)(CO)4、[RuCl2(COD)]n和Fe(COD)(CO)3。環辛二烯在Rh(I)和Ir(I)的配位化學中特別重要,例如克拉布特里催化劑和環辛二烯氯化銠二聚體。平面四邊形的配合物[M(COD)2]+也是已知的(M = Rh、Ir)。
(E,E)-COD
編輯1,5-環辛二烯張力很大的反-反異構體是一種已知的化合物。(E,E)-COD最早由喬治·懷特塞茲和阿瑟·科普在1969年通過順式異構體的光異構化製得。[10]另一種合成路線(八元環的雙消除反應)由羅爾夫·胡伊斯根於1987年報道。[11](E,E)-COD的構象是扭船式而不是椅式的。這種化合物已被研究用於點擊化學的介質。[12]
參考文獻
編輯- ^ AC1L1QCE - Compound Summary. PubChem Compound. USA: National Center for Biotechnology Information. Identification and Related Records. 26 March 2005 [14 October 2011]. (原始內容存檔於2012-02-25).
- ^ Buehler, C; Pearson, D.Survey of Organic Syntheses. Wiley-Intersciene, New York. 1970.
- ^ Shriver, D; Atkins, P.Inorganic Chemistry. W. H. Freeman and Co., New York. 1999.
- ^ Thomas Schiffer, Georg Oenbrink “Cyclododecatriene, Cyclooctadiene, and 4-Vinylcyclohexene” in Ullmann’s Encyclopedia of Industrial Chemistry, 2005, Wiley-VCH, Weinheim.
- ^ John A. Soderquist and Alvin Negron (1998). "9-Borabicyclo[3.3.1]nonane Dimer". Org. Synth.; Coll. Vol. 9: 95.
- ^ Roger Bishop. "9-Thiabicyclo[3.3.1nonane-2,6-dione]". Org. Synth.; Coll. Vol. 9: 692. Díaz, David Díaz; Converso, Antonella; Sharpless, K. Barry; Finn, M. G. 2,6-Dichloro-9-thiabicyclo[3.3.1]nonane: Multigram Display of Azide and Cyanide Components on a Versatile Scaffold (PDF). Molecules. 2006, 11: 212–218 [2011-10-03]. doi:10.3390/11040212. (原始內容存檔 (PDF)於2011-09-27).
- ^ 宋禮成, 王佰全. 金屬有機化學原理及應用. 高等教育出版社, 2012. pp 411
- ^ Schunn, R; Ittel, S. Bis(1,5-Cyclooctadiene) Nickel(0). Inorg. Synth. 1990, 28: 94. doi:10.1002/9780470132593.ch25.
- ^ Crascall, L; Spencer, J. Olefin Complexes of Platinum. Inorg. Synth. 1990, 28: 126. doi:10.1002/9780470132593.ch34.
- ^ Irradiation of cis,cis-1,5-cyclooctadiene in the presence of copper(I) chloride George M. Whitesides, Gerald L. Goe, Arthur C. Cope J. Am. Chem. Soc., 1969, 91 (10), pp 2608–2616 doi:10.1021/ja01038a036
- ^ Preparation and conformation of (E,E)-1,5-cyclooctadiene Dieter Boeckh, Rolf Huisgen, Heinrich Noeth J. Am. Chem. Soc., 1987, 109 (4), pp 1248–1249 doi:10.1021/ja00238a046
- ^ (E,E)-1,5-Cyclooctadiene: a small and fast click-chemistry multitalent Henning Stöckmann, André A. Neves, Henry A. Day, Shaun Stairs, Kevin M. Brindle and Finian J. Leeper Chem. Commun., 2011 doi:10.1039/C1CC12161H