RNA複製酶
RNA複製酶(RNA replicase)或名RNA依賴性RNA聚合酶(RNA-dependent RNA polymerase),縮寫 RdRp 或 RDR,係一類能以RNA爲模板複製RNA的酶。值得注意的是,這類酶與以DNA爲模板合成RNA的RNA聚合酶(在轉錄中扮演重要角色的酶)不是同一類酶。
| RNA複製酶 RNA-dependent RNA polymerase | |||||||
|---|---|---|---|---|---|---|---|

| |||||||
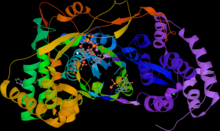
| RNA複製酶的結構PDB 3PHU.[1] | |||||||
| |||||||
| 識別碼 | |||||||
| EC編號 | 2.7.7.48 | ||||||
| CAS號 | 9026-28-2 | ||||||
| 資料庫 | |||||||
| IntEnz | IntEnz瀏覽 | ||||||
| BRENDA | BRENDA入口 | ||||||
| ExPASy | NiceZyme瀏覽 | ||||||
| KEGG | KEGG入口 | ||||||
| MetaCyc | 代謝路徑 | ||||||
| PRIAM | 概述 | ||||||
| PDB | RCSB PDB PDBj PDBe PDBsum | ||||||
| 基因本體 | AmiGO / EGO | ||||||
| |||||||
| RNA dependent RNA polymerase | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 鑑定 | |||||||||
| 標誌 | RdRP_1 | ||||||||
| Pfam | PF00680(舊版) | ||||||||
| Pfam宗系 | CL0027(舊版) | ||||||||
| InterPro | IPR001205 | ||||||||
| SCOP | 2jlg / SUPFAM | ||||||||
| |||||||||
| RNA-directed RNA polymerase, flaviviral | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 鑑定 | |||||||||
| 標誌 | RNA_pol_flaviviral | ||||||||
| Pfam | PF00972(舊版) | ||||||||
| InterPro | IPR000208 | ||||||||
| |||||||||
RNA複製酶對於那些反義RNA病毒(例如流感病毒)的增殖來說,是一種至關重要的蛋白質[2][3]。RNA複製酶能合成一條RNA單鏈的互補鏈[4][5]。
歷史
編輯病毒 RdRps 是在 1960 年代早期通過對腦膜炎病毒和脊髓灰質炎病毒的研究發現的,當時觀察到這些病毒對放線菌素不敏感,放線菌素是一種抑制細胞 DNA 指導的 RNA 合成的藥物。 這種缺乏敏感性表明有一種病毒特異性酶可以從RNA模板而不是從DNA模板複製RNA。
分布
編輯RdRps在整個病毒中高度保守,甚至與端粒酶有關,儘管截至2009年這是一個持續存在的問題[6]。這種相似性導致推測病毒 RdRps 是人類端粒酶的祖先。
RdRp 最著名的例子是脊髓灰質炎病毒。
結構
編輯所有的RNA複製酶和不少RNA聚合酶都有一個摺疊結構。這個摺疊結構與三個亞結構域相連。上面三個結構域的形狀和人的右手想像,因而分別被稱爲「四指」(fingers)、「手掌」(palm)、「拇指」(thumb)[7]。其中,只有手掌亞結構域有一個由四條反向平行的多肽鏈構成的β-折疊結構和兩個α-螺旋結構,在各類RNA複製酶中高度保守。其中,手掌亞結構域有三個高度保守的基元(A、B,以及C)。基元A(D-x(4,5)-D)和基元C(GDD)在空間上並列。這兩個基元中的天冬氨酸殘基與鎂離子和錳離子相連。而B基元中的天冬醯胺殘基則與在脫氧三磷酸核苷中選三磷酸核糖核苷的過程有關,上述過程可以確保合成的是RNA而不是DNA[8]。RNA複製酶的結構域的組織形式保守[9],其催化中心也是一樣。RNA複製酶的催化中心是由一系列包含保守的胺基酸殘基的基元組成的,即使在同源性不高的編碼序列下也保守。
參考
編輯- ^ Akutsu, M; Ye, Y; Virdee, S; Chin, JW; Komander, D. Molecular basis for ubiquitin and ISG15 cross-reactivity in viral ovarian tumor domains. Proc. Natl. Acad. Sci. U.S.A. February 2011, 108 (6): 2228–33. PMC 3038727 . PMID 21266548. doi:10.1073/pnas.1015287108.
- ^ Koonin EV, Gorbalenya AE, Chumakov KM. Tentative identification of RNA-dependent RNA polymerases of dsRNA viruses and their relationship to positive strand RNA viral polymerases. FEBS Lett. July 1989, 252 (1–2): 42–6. PMID 2759231. doi:10.1016/0014-5793(89)80886-5.
- ^ Zanotto PM, Gibbs MJ, Gould EA, Holmes EC. A reevaluation of the higher taxonomy of viruses based on RNA polymerases. J. Virol. September 1996, 70 (9): 6083–96. PMC 190630 . PMID 8709232.
- ^ Jin, Z; Leveque, V; Ma, H; Johnson, K. A.; Klumpp, K. Assembly, purification, and pre-steady-state kinetic analysis of active RNA-dependent RNA polymerase elongation complex. Journal of Biological Chemistry. 2012, 287 (13): 10674–83. PMC 3323022 . PMID 22303022. doi:10.1074/jbc.M111.325530.
- ^ Kao CC, Singh P, Ecker DJ. De novo initiation of viral RNA-dependent RNA synthesis. Virology. September 2001, 287 (2): 251–60. PMID 11531403. doi:10.1006/viro.2001.1039.
- ^ Suttle CA. Viruses in the sea. Nature. September 2005, 437 (7057): 356–61. Bibcode:2005Natur.437..356S. PMID 16163346. S2CID 4370363. doi:10.1038/nature04160.
- ^ Hansen JL, Long AM, Schultz SC. Structure of the RNA-dependent RNA polymerase of poliovirus. Structure. August 1997, 5 (8): 1109–22. PMID 9309225. doi:10.1016/S0969-2126(97)00261-X.
- ^ Gohara DW, Crotty S, Arnold JJ, Yoder JD, Andino R, Cameron CE. Poliovirus RNA-dependent RNA polymerase (3Dpol): structural, biochemical, and biological analysis of conserved structural motifs A and B. J. Biol. Chem. August 2000, 275 (33): 25523–32. PMID 10827187. doi:10.1074/jbc.M002671200.
- ^ O'Reilly EK, Kao CC. Analysis of RNA-dependent RNA polymerase structure and function as guided by known polymerase structures and computer predictions of secondary structure. Virology. December 1998, 252 (2): 287–303. PMID 9878607. doi:10.1006/viro.1998.9463.