地拉罗司
地拉罗司(INN:deferasirox)是一种口服铁螯合治疗药物,于市面销售的品牌中,有诺华公司在不同国家生产的Exjade、Asunra和Oleptiss(均为片剂)。其主要用途是减少因罹患β型地中海贫血和其他慢性贫血等疾病的患者,因需长期接受输血而造成的血色沉着病。[2][3]此药物是第一种于美国受到批准用于前述目的的药物,以口服方式给药。[4]
 | |
 | |
| 临床资料 | |
|---|---|
| 读音 | de FER a sir ox |
| 商品名 | 易解铁(Exjade)、Asunra、Asunra及解铁定(Jadenu)等 |
| 其他名称 | CGP-72670, ICL-670A, IC L670 |
| AHFS/Drugs.com | Monograph |
| 核准状况 |
|
| 怀孕分级 |
|
| 给药途径 | 口服给药 |
| ATC码 | |
| 法律规范状态 | |
| 法律规范 |
|
| 药物动力学数据 | |
| 生物利用度 | 70% |
| 血浆蛋白结合率 | 99% |
| 药物代谢 | 肝脏葡糖苷酸化 |
| 生物半衰期 | 8-16小时 |
| 排泄途径 | 粪便 (84%)及尿液 (8%) |
| 识别信息 | |
| |
| CAS号 | 201530-41-8 |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.211.077 |
| 化学信息 | |
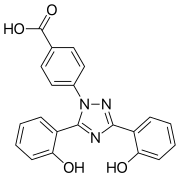
| 化学式 | C21H15N3O4 |
| 摩尔质量 | 373.37 g·mol−1 |
| 3D模型(JSmol) | |
| 密度 | 1.4±0.1 g/cm3 [1] |
| |
| |
地拉罗司于2005年11月获得美国食品药物管理局(FDA)核准用于治疗β型地中海贫血。[2][4]根据FDA (2007年5月) 的数据,接受地拉罗司治疗的患者中出现肾功能衰竭和成熟血球数量减少的报告。此药物于2008年在欧盟获得欧洲药品管理局 (EMA) 批准,用于治疗六岁及以上儿童因连续输血而导致的慢性血色沉着病。[5][6][7]地拉罗司已被列入世界卫生组织基本药物标准清单中。[8]
属性
编辑地拉罗司进入人体后的生物半衰期为8至16小时,因此每天只需给药一次。[11]两个分子的地拉罗司能与1个铁原子结合,之后透过粪便排出人体。其具有的低分子量和高亲脂的特性让该药物可用口服方式摄取,不像有类似功能的去铁胺须透过静脉注射给药。地拉罗司与去铁酮联合使用,似乎能从细胞(心肌细胞和肝细胞)中以及从血液中将铁去除。[12]
合成
编辑地拉罗司可由市面既有的简单原料(水杨酸、水杨酰胺和 4-肼基苯甲酸(4-hydrazinobenzoic acid)依照两步合成顺序制备。[13]
风险
编辑根据非营利组织安全医疗实践研究所编制的2019年疑似导致患者死亡的药物名单中,与地拉罗司相关的死亡人数为1,320例,排名第二。[14]于同年,该药物的标签中被要求加上可能会导致肾功能衰竭、肝衰竭和消化道出血的黑框警告。[15]疑似导致死亡人数激增的主要原因是因为诺华重新分析不良事件数据后而得的结果。[14]
参见
编辑- ^ Material Safety Data Sheet (MSDS): Deferasirox. ChemSrc. 2018 [2024-04-18]. (原始内容存档于2017-06-12).
- ^ 2.0 2.1 Choudhry VP, Naithani R. Current status of iron overload and chelation with deferasirox. Indian Journal of Pediatrics. August 2007, 74 (8): 759–64. PMID 17785900. S2CID 19930076. doi:10.1007/s12098-007-0134-7. Free full text 互联网档案馆的存档,存档日期2014-04-29.
- ^ Yang LP, Keam SJ, Keating GM. Deferasirox : a review of its use in the management of transfusional chronic iron overload. Drugs. 2007, 67 (15): 2211–30. PMID 17927285. S2CID 195686285. doi:10.2165/00003495-200767150-00007.
- ^ 4.0 4.1 FDA Approves First Oral Drug for Chronic Iron Overload (新闻稿). United States Food and Drug Administration. 2005-11-09 [2007-10-31]. (原始内容存档于2009-05-13).
- ^ Exjade – deferasirox (PDF). European Medicines Agency. 2018 [2012-11-26]. (原始内容 (PDF)存档于2017-12-29).
- ^ Kontoghiorghes GJ. Turning a blind eye to deferasirox's toxicity?. Lancet. April 2013, 381 (9873): 1183–4. PMID 23561999. S2CID 27794849. doi:10.1016/S0140-6736(13)60799-0 .
- ^ Review: Exjade side effects. [2013-04-20]. (原始内容存档于2016-03-04).
- ^ World Health Organization. The selection and use of essential medicines 2023: web annex A: World Health Organization model list of essential medicines: 23rd list (2023). Geneva: World Health Organization. 2023. hdl:10665/371090 . WHO/MHP/HPS/EML/2023.02.
- ^ Deferasirox Discontinuation. U.S. Food and Drug Administration (FDA). [2020-07-20]. (原始内容存档于2020-07-21).
- ^ Drugs@FDA: FDA-Approved Drugs. U.S. Food and Drug Administration. [2020-08-15]. (原始内容存档于2020-10-19).
- ^ Al-Rousan, Rabaa M.; Manzoor, Kamran. Long-Term Efficacy of Deferasirox in Preventing Cardiovascular Complications in the Iron-Overloaded Gerbil. Journal of Cardiovascular Pharmacology and Therapeutics. 2011-05-18 [2024-04-09]. doi:10.1177/1074248411407635. (原始内容存档于2024-04-09).
- ^ Salem, Ahmed; Desai, Payal. Cureus https://www.ncbi.nlm.nih.gov/pmc/articles/PMC10695738/. November 2023, 15 (11) [2024-04-09]. (原始内容存档于2024-04-09). 缺少或
|title=为空 (帮助) - ^ Steinhauser S, Heinz U, Bartholomä M, Weyhermüller T, Nick H, Hegetschweiler K. Complex Formation of ICL670 and Related Ligands with FeIII and FeII. European Journal of Inorganic Chemistry. 2004, 2004 (21): 4177–4192. doi:10.1002/ejic.200400363.]
- ^ 14.0 14.1 QuarterWatch™ (Quarter 4 and 2009 totals): Reported Patient Deaths Increased by 14% in 2009. Institute For Safe Medication Practices. [2021-06-28]. (原始内容存档于2021-06-28) (英语).
- ^ Pediatrics, American Academy of. Black box warning added to Exjade. AAP News. 2010-02-19 [2021-06-28]. ISSN 1073-0397. doi:10.1542/aapnews.20100219-1 (不活跃 31 January 2024). (原始内容存档于2021-06-28) (英语).