诺西那生
诺西那生(INN:Nusinersen[5],商品名为Spinraza)[6]是第一个用于治疗脊髓性肌肉萎缩症的药物[7]。脊髓性肌肉萎缩症是一种罕见的神经退化性疾病,其病因是自双亲遗传了功能低落或没有功能的SMN基因,因此无法生产足够的SMN蛋白,患者的运动神经元会逐渐死亡,运动功能也会逐渐恶化,最严重者可能全身瘫痪而不能自主呼吸[8]。诺西那生是一种反义寡核苷酸药物,能够借着稳定SMN的信使核糖核酸来提升SMN蛋白的生产量[9]。它能降低患者的死亡率以及因疾病失去呼吸功能的风险,并能改善患者的运动功能。2016年12月诺西那生在美国通过优先审查后取得上市许可,稍后在欧洲联盟、加拿大、巴西、日本、韩国、新西兰等国也被核准为处方药。诺西那生在美国与欧盟都被视为孤儿药[10]。诺西那生因为其高昂的价格受到一些批评[11]。基于成本考量,欧洲有部分国家虽然已经核准其上市,但目前并没有将其列为脊髓性肌肉萎缩症的常规治疗方法[12][13][14]。
 | |
| 临床资料 | |
|---|---|
| 商品名 | Spinraza |
| 其他名称 | IONIS-SMNRx, ISIS-SMNRx |
| AHFS/Drugs.com | Multum消费者信息 |
| 核准状况 | |
| 给药途径 | 脊髓鞘内注射 |
| ATC码 | |
| 法律规范状态 | |
| 法律规范 |
|
| 药物动力学数据 | |
| 药物代谢 | 经外切酶(3' 端及 5')水解 |
| 生物半衰期 | 135–177 天(于脑脊液中),63–87 天(于血浆中) |
| 识别信息 | |
| |
| CAS号 | 1258984-36-9 |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| 化学信息 | |
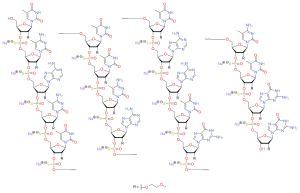
| 化学式 | C234H323N61Na17O128P17S17[6] |
| 摩尔质量 | 7501 原子质量单位[6] |
| 3D模型(JSmol) | |
| |
适应症
编辑诺西那生可以治疗脊髓性肌肉萎缩症。给药方式为脊髓鞘内注射将药物送入中枢神经系统[6]。临床试验中,诺西那生能够减缓脊髓性肌肉萎缩症的恶化[6]。有51 %患有第一型脊髓性肌肉萎缩症(早发型)的受试者的运动功能在给药之后改善[15],另外相对于对照组,治疗组的死亡或依赖呼吸器的风险比也降低为0.53[16]。症状较为轻微的第二型、第三型患者的临床试验当中也有57 %的患者在给药后运动功能有所进步[17]。
副作用与不良反应
编辑诺西那生有引起不良反应的风险。最为常见的不良反应包括上呼吸道感染、肺炎、支气管炎、便秘等等[6][16]。较严重的不良反应中发生率最高的是肺塌陷[16]。在年纪稍大的受试者中,常见的不良反应则与腰椎穿刺[注 1]相似,包括头痛、背痛等[6][17]。另外,用药的病童的身高成长有可能会较正常儿童缓慢,目前的证据并不足以判断停药之后诺西那生造成的生长迟缓是否会复原[6]。
与其他的反义寡核苷酸类药物相似,诺西那生可能会影响肾功能,并可能会造成凝血功能异常[6]。其他反义核苷酸类药物的试验中,受试者曾发生严重程度不一的肾功能异常,最严重的案例是可能致命的肾小球肾炎。临床试验中使用诺西那生的受试者有33 %的尿蛋白异常上升[6]。针对年纪较大的晚发性患者的试验中则有69 %的受试者发生尿蛋白异常[6],因此在开始治疗前及每次给药之前都需要检验尿蛋白读数,如果读数异常则需要进一步接受其他肾功能检查[6]。
在诺西那生的临床试验中,在治疗前原先血小板数量正常的受试者,在治疗后有11 %发生轻微的血小板低下,但血小板数量会在停药后自然恢复[6]。由于诺西那生可能会影响对血小板数量及凝血功能,在治疗开始之前及治疗过程中均需要定期检验血小板数量及凝血功能[6]。除此之外,患者可能会对诺西那生产生免疫反应,不过至2016年12月为止,尚没有证据说明针对诺西那生的免疫反应是否会影响治疗成效及安全[6]。使用诺西那生的儿童及成年患者中曾发生数例常压性水脑症,但目前尚不清楚常压性水脑症的发生是否与诺西那生相关[18]。
药理机转与特性
编辑脊髓性肌肉萎缩症的原因是自双亲遗传突变的SMN1基因,如果来自双亲的SMN1基因都没有功能则会发病[8]。SMN1基因记录着SMN蛋白的资讯[19]。生物体的发育与生存都需要SMN蛋白,因此完全失去SMN蛋白的生物会在胚胎发育的早期死亡[19]。人类的基因中有两个能合成SMN蛋白的旁系同源基因:SMN1与SMN2,因此失去SMN1基因的患者尚能由SMN2基因合成SMN蛋白而得以存活[19]。SMN1基因与SMN2基因虽然带有相同资讯,但SMN2基因在RNA剪接时容易形成截断而不完整的短信使核糖核酸,这使得SMN2转译产生正常的SMN蛋白的效率较低[注 2][19][20]。因此脊髓性肌肉萎缩症患者虽然有SMN2基因提供SMN蛋白,但体内的有效SMN蛋白量仍比健康人低[19]。
诺西那生会以碱基配对的方式与未剪接的SMN2核糖核酸结合,并与剪接蛋白竞争结合位[21]。这会改变SMN2信使核糖核酸的RNA剪接模式,并降低它在剪接中被截断的机会,借此来增加中枢神经系统中正常的SMN蛋白的量[9]。诺西那生除分布于中枢神经系统内,也会散布至肌肉、肝脏、以及肾脏等周边组织[6]。诺西那生在脑脊液中之半衰期估计为135-177天;在血浆中之半衰期则为63-87天[6]。诺西那生会被外切酶(3'或5'端)水解而代谢,并不经CYP450族酵素分解代谢[6]。诺西那生及其代谢产物主要的排除途径可能为尿液[6]。
化学特性
编辑诺西那生属于反义寡核苷酸类药物[6]。由于体内环境有大量的核糖核酸酶存在,寡核苷酸一旦进入体内就会被快速分解[22]。诺西那生的呋喃核糖基环上的2-羟基(英语:2'-hydroxyl group)被2-氧-2-甲氧乙基(英语:2-O-2-methyoxymethyl group)所取代,这个修饰使它在体内较为稳定,不容易被核酸酶分解而容易达到治疗所需的有效浓度[23]。此外其磷酸二酯键也被硫代磷酸酯键取代,硫代磷酸酯键同样使反义寡核苷酸不易被分解,且仍能保持其碱基配对的功能[24]。
历史沿革
编辑SMN1基因与SMN2基因在剪接上的差异在二十一世纪初期受到研究者的重视,在相关研究当中发现SMN核糖核酸上有许多短核酸序列在剪接上扮演重要的角色[25]。2006年,马萨诸塞大学医学院的Singh团队[注 3]在CureSMA(页面存档备份,存于互联网档案馆)的经费支持下[26],发现一个序列对SMN2核糖核酸被截断有重要影响,并将其命名为内含子剪接抑制位N1(英语:intronic splicing silencer N1 (ISS-N1))[25]。
在此同时冷泉港实验室的Adrian Krainer团队[27]正与Ionis制药(原Isis制药)合作寻找以反义寡核苷酸改变SMN核糖核酸含量的可能性[25]。这个研究发现了数个能提高SMN信使核糖核酸的反义寡核苷酸,而这些反义寡核苷酸当中效果最好的一个,其目标序列正是内含子剪接抑制位N1,这个反义寡核苷酸成为了后来的诺西那生[25]。Krainer团队与Ionis制药继续合作,并在动物身上试验诺西那生的治疗效果,并发现它能延长患病小鼠的寿命达七倍,其他的动物实验也看到类似的治疗效果[25][28][29][30]。
Biogen[注 4]在 2015 年以七千五百万美元的授权费自Ionis制药取得诺西那生的独家授权[注 5][31]。授权条款中后续的里程碑款项最高为一亿五千万美元,超出里程碑的部分则需付出分层的专利使用费,Biogen也需要负担此后的开发与行销费用[32]。由于诺西那生在第三期临床试验表现良好,且考虑当时尚没有方法能治疗脊髓性肌肉萎缩症,诺西那生在 2016 年 11 月开始的新药审查符合美国食品药物监督管理局的优先审理条件。欧洲药品管理局也在同期接受其审查申请[33][11]。
美国食品药物监督管理局在2016年12月核准诺西那生用于治疗脊髓性肌肉萎缩症,欧洲药品管理局也在稍后的2017年5月核准,诺西那生正式成为第一个治疗脊髓性肌肉萎缩症的药物[34][35]。诺西那生接下来在各国陆续被核准:加拿大(2017年7月)[36]、日本(2017年7月)[37]、巴西(2017年8月)[38]、瑞士(2017年9月)[39]、韩国(2018年1月)、[40]、以及新西兰(2018年8月)[41]。
2019年4月,诺西那生钠在中国大陆上市,1瓶/盒为5ml:12mg(按有效成分诺西那生计),无医保定价为699,700元人民币[42]。2022年1月1日,诺西那生钠注射液实施中国大陆医保价格,价格从原先的70万元一针降到约3.3万元一针。经过医保报销后,个人仅需支付几千元[43]。
价位争议
编辑诺西那生的建议售价是一剂125,000美元,治疗的总和花费在第一年为750,000美元,接下来每年为375,000美元[11]。纽约时报的报导中指出诺西那生“是世界上最昂贵的药物之一[11]。”2017年10月,丹麦当局以诺西那生的价格相对于治疗效果而言昂贵到不合理的程度为理由拒绝将诺西那生列为脊髓性肌肉萎缩症的常规疗法,并建议诺西那生只应使用在部分的第一型脊髓性肌肉萎缩症患者(早发型)[12]。挪威当局在 2017年10月以“过高的定价并不道德”为理由拒绝给付诺西那生,但稍后在2018年2月开始给付18岁以下患者的用药[13]。负责英格兰及威尔士地区公共卫生政策成本效益分析的英国国家健康与照顾卓越研究院在 2018 年 8 月的报告中以成本考量为由不建议公立的医疗院所使用诺西那生治疗脊髓性肌肉萎缩症患者[14],当地的病患权益促进组织则对国家健康与照顾卓越研究院的态度表达强烈不满,并表示将持续施压争取[44]。2020年8月,中国湖南省一名小婴儿患上了脊髓性肌萎缩症急需诺西那生救命,此药在中国售价一剂5mL高达70万元人民币,因尚未纳入中国《国家基本医疗保险、工伤保险和生育保险药品目录》名单,需全额自费,孩子的父母负担不起治疗费用,只能上网向公众求救。这也让部分中国民众认识到有这种天价药物的存在,并对此药的惊人高价是否合理以及为何未纳入医保发出了疑问[45][46]。诺西那生已于2020年12月3日纳入中国《国家基本医疗保险、工伤保险和生育保险药品目录》名单。
另见
编辑另两种获准使用的SMA药物[47]:
- Onasemnogene abeparvovec(诺华的子公司AveXis研制)
- Evrysdi(罗氏药厂研制)
备注
编辑- ^ 脊髓鞘内注射时需进行腰椎穿刺。
- ^ 在生物体中,编码基因的脱氧核糖核酸会被合成为核糖核酸(称为转录),转录得到的核糖核酸在经过处理-包括RNA剪接与核糖核酸编辑-之后,会变成合成蛋白质的蓝图(信使核糖核酸,依照信使核糖核酸合成蛋白的过程称为转译)。这个整个流程称为生物学的中心法则。原则上,蓝图(信使核糖核酸)的量越多,能生产的产品的量也越多。
- ^ 依原始论文之作者序列,团队成员包括:Nirmal K. Singh、Natalia N. Singh、Elliot J. Androphy、以及Ravindra N. Singh。
- ^ Biogen是Ionis制药的策略合作伙伴。
- ^ Biogen取得的授权范围为Ionis制药自冷泉港实验室及马萨诸塞大学医学院取得的智慧财产。
引用来源
编辑- ^ Canada, Health; Canada, Health. Notice: Prescription Drug List (PDL): Multiple additions [2017-08-04]. The Prescription Drug List. Government of Canada. 2017-08-04 [2019-01-01]. (原始内容存档于2020-10-24).
- ^ NEW ZEALAND DATA SHEET: SPINRAZA (PDF). Data Sheets and Consumer Medicine Information. New Zealand Medicines and Medical Devices Safety Authority. [2019-01-01]. (原始内容存档 (PDF)于2021-02-02).
- ^ Spinraza 12 mg solution for injection - Summary of Product Characteristics (SmPC) - (eMC). eMC. Datapharm. [2019-01-01]. (原始内容存档于2019-02-17).
- ^ Spinraza. www.ema.europa.eu. European Medicines Agency. [2019-01-01]. (原始内容存档于2021-01-04).
- ^ 5.0 5.1 International Nonproprietary Names for Pharmaceutical Substances (INN). Recommended International Nonproprietary Names: List 74 (PDF). World Health Organization: 413–14. [2017-03-13]. (原始内容存档 (PDF)于2020-08-13).
- ^ 6.00 6.01 6.02 6.03 6.04 6.05 6.06 6.07 6.08 6.09 6.10 6.11 6.12 6.13 6.14 6.15 6.16 6.17 6.18 6.19 Nusinersen US Label (PDF). FDA. December 2016 [2018-12-31]. (原始内容存档 (PDF)于2020-11-23). For updates see FDA index page for NDA 209531 (页面存档备份,存于互联网档案馆)
- ^ Ottesen, Eric W. ISS-N1 makes the first FDA-approved drug for spinal muscular atrophy. Translational Neuroscience. 2017-01-01, 8 (1): 1–6 [2018-12-31]. ISSN 2081-6936. PMC 5382937 . PMID 28400976. doi:10.1515/tnsci-2017-0001. (原始内容存档于2019-10-18) (英语).
- ^ 8.0 8.1 Lunn, Mitchell R; Wang, Ching H. Spinal muscular atrophy. The Lancet. 2008-06, 371 (9630): 2120–2133 [2019-01-03]. doi:10.1016/S0140-6736(08)60921-6.
- ^ 9.0 9.1 Zanetta, C; Nizzardo, M; Simone, C; Monguzzi, E; Bresolin, N; Comi, GP; Corti, S. Molecular Therapeutic Strategies for Spinal Muscular Atrophies: Current and Future Clinical Trials. Clinical Therapeutics. 2014-01-01, 36 (1): 128–40. PMID 24360800. doi:10.1016/j.clinthera.2013.11.006.
- ^ Nusinersen. UK Specialist Pharmacy Service. [2016-12-31]. (原始内容存档于2019-04-13).
- ^ 11.0 11.1 11.2 11.3 Katie Thomas. Costly Drug for Fatal Muscular Disease Wins F.D.A. Approval. New York Times. 2016-12-30 [2018-12-31]. (原始内容存档于2020-11-08).
- ^ 12.0 12.1 Medicinrådet siger nej til lægemiddel til børn med muskelsvind: 'Urimeligt' dyrt (页面存档备份,存于互联网档案馆) Retrieved October 13 2017.
- ^ 13.0 13.1 – Dette er uforståelig og utrolig urettferdig. www.abcnyheter.no. [2018-12-31]. (原始内容存档于2020-12-02).
- ^ 14.0 14.1 Ben Hirschler. Biogen's pricey muscle drug Spinraza too costly for Britain. Reuters. Reuters. 2018-08-13 [2019-01-01]. (原始内容存档于2020-11-09) (英语).
- ^ Finkel, Richard S; Chiriboga, Claudia A; Vajsar, Jiri; Day, John W; Montes, Jacqueline; De Vivo, Darryl C; Yamashita, Mason; Rigo, Frank; Hung, Gene; Schneider, Eugene; Norris, Daniel A; Xia, Shuting; Bennett, C Frank; Bishop, Kathie M. Treatment of infantile-onset spinal muscular atrophy with nusinersen: A phase 2, open-label, dose-escalation study. The Lancet. 2016, 388 (10063): 3017. doi:10.1016/S0140-6736(16)31408-8.
- ^ 16.0 16.1 16.2 Finkel, Richard S.; Mercuri, Eugenio; Darras, Basil T.; Connolly, Anne M.; Kuntz, Nancy L.; Kirschner, Janbernd; Chiriboga, Claudia A.; Saito, Kayoko; Servais, Laurent; Tizzano, Eduardo; Topaloglu, Haluk; Tulinius, Már; Montes, Jacqueline; Glanzman, Allan M.; Bishop, Kathie; Zhong, Z. John; Gheuens, Sarah; Bennett, C. Frank; Schneider, Eugene; Farwell, Wildon; De Vivo, Darryl C. Nusinersen versus Sham Control in Infantile-Onset Spinal Muscular Atrophy. New England Journal of Medicine. 2017-11-02, 377 (18): 1723–1732. doi:10.1056/NEJMoa1702752.
- ^ 17.0 17.1 Mercuri, Eugenio; Darras, Basil T.; Chiriboga, Claudia A.; Day, John W.; Campbell, Craig; Connolly, Anne M.; Iannaccone, Susan T.; Kirschner, Janbernd; Kuntz, Nancy L.; Saito, Kayoko; Shieh, Perry B.; Tulinius, Már; Mazzone, Elena S.; Montes, Jacqueline; Bishop, Kathie M.; Yang, Qingqing; Foster, Richard; Gheuens, Sarah; Bennett, C. Frank; Farwell, Wildon; Schneider, Eugene; De Vivo, Darryl C.; Finkel, Richard S. Nusinersen versus Sham Control in Later-Onset Spinal Muscular Atrophy. New England Journal of Medicine. 2018-02-15, 378 (7): 625–635. doi:10.1056/NEJMoa1710504.
- ^ New warning of nusinersen-related communicating hydrocephalus. Reactions Weekly. 2018-08-01, 1714 (1): 3–3 [2018-12-31]. ISSN 1179-2051. doi:10.1007/s40278-018-50183-2. (原始内容存档于2019-04-03) (英语).
- ^ 19.0 19.1 19.2 19.3 19.4 Burghes, Arthur H. M.; Beattie, Christine E. Spinal muscular atrophy: why do low levels of survival motor neuron protein make motor neurons sick?. Nature Reviews Neuroscience. 2009-07-08, 10 (8): 597–609 [2019-01-01]. doi:10.1038/nrn2670. (原始内容存档于2021-08-29).
- ^ Edfors, F; Danielsson, F; Hallström, BM; Käll, L; Lundberg, E; Pontén, F; Forsström, B; Uhlén, M. Gene-specific correlation of RNA and protein levels in human cells and tissues.. Molecular systems biology. 2016-10-20, 12 (10): 883 [2019-01-03]. PMID 27951527. doi:10.15252/msb.20167144. (原始内容存档于2021-05-02).
- ^ Rigo, Frank; Hua, Yimin; Krainer, Adrian R.; Bennett, C. Frank. Antisense-based therapy for the treatment of spinal muscular atrophy. The Journal of Cell Biology. 2012-10-01, 199 (1): 21–25 [2019-01-03]. doi:10.1083/jcb.201207087. (原始内容存档于2019-11-29).
- ^ Sampaio-Silva, F; Magalhães, T; Carvalho, F; Dinis-Oliveira, RJ; Silvestre, R. Profiling of RNA degradation for estimation of post mortem interval.. PloS one. 2013, 8 (2): e56507. PMID 23437149. doi:10.1371/journal.pone.0056507.
- ^ Geary, RS; Watanabe, TA; Truong, L; Freier, S; Lesnik, EA; Sioufi, NB; Sasmor, H; Manoharan, M; Levin, AA. Pharmacokinetic properties of 2'-O-(2-methoxyethyl)-modified oligonucleotide analogs in rats.. The Journal of pharmacology and experimental therapeutics. 2001-03, 296 (3): 890–7. PMID 11181921.
- ^ Dias, N; Stein, CA. Antisense oligonucleotides: basic concepts and mechanisms.. Molecular cancer therapeutics. 2002-03, 1 (5): 347–55. PMID 12489851.
- ^ 25.0 25.1 25.2 25.3 25.4 Singh, NN; Howell, MD; Androphy, EJ; Singh, RN. How the discovery of ISS-N1 led to the first medical therapy for spinal muscular atrophy.. Gene therapy. 2017-09, 24 (9): 520–526 [2019-01-03]. PMID 28485722. doi:10.1038/gt.2017.34. (原始内容存档于2021-05-26).
- ^ Therapeutic Approaches. www.curesma.org. Cure SMA. [2017-01-01]. (原始内容存档于2017-01-01).
- ^ Mahy, Brian W.J. FDA approval of life-saving SMA drug is hailed by its researcher-inventor at CSHL. Cold Spring Harbor Laboratory. 2016-12-24 [2019-01-01]. (原始内容存档于2020-11-23).
- ^ Garber, K. Big win possible for Ionis/Biogen antisense drug in muscular atrophy.. Nature Biotechnology. 2016-10-11, 34 (10): 1002–1003. PMID 27727217. doi:10.1038/nbt1016-1002.
- ^ Wadman, Meredith. Updated: FDA approves drug that rescues babies with fatal neurodegenerative disease. Science. 2016-12-23 [2018-12-31]. (原始内容存档于2017-05-25).
- ^ Offord, Catherine. Oligonucleotide Therapeutics Near Approval. The Scientist. 2016-12-01 [2021-02-08]. (原始内容存档于2018-04-11).
- ^ Biogen and Ionis Pharmaceuticals Announce SPINRAZA (nusinersen) Meets Primary Endpoint at Interim Analysis of Phase 3 CHERISH Study in Later-Onset Spinal Muscular Atrophy. Ionis Pharmaceuticals, Inc. Ionis Pharmaceuticals. [2019-01-01]. (原始内容存档于2017-11-11) (英语).
- ^ Biogen Shells Out $75M to Develop Ionis' Nusinersen after Positive Phase III Results, Genetic Engineering News, 2016-08-01 [2018-12-31], (原始内容存档于2018-06-14)
- ^ Regulatory Applications for SMA Therapy Nusinersen Accepted in US, EU. BioNews Services, LLC. [2016-11-15]. (原始内容存档于2020-08-15).
- ^ Grant, Charley. Surprise Drug Approval Is Holiday Gift for Biogen. Wall Street Journal. 2016-12-27 [2016-12-27]. ISSN 0099-9660. (原始内容存档于2020-11-08). 参数
|newspaper=与模板{{cite web}}不匹配(建议改用{{cite news}}或|website=) (帮助) - ^ Spinraza (nusinersen). 欧洲药品管理局. [2017-10-27]. (原始内容存档于2017-10-28).
- ^ Spinraza Approved by Health Canada for Treating 5q SMA Patients. SMA News Today. 2017-07-06 [2019-01-01]. (原始内容存档于2019-02-17).
- ^ Biogen to launch Spinraza in Japan soon. 2017-07-10 [2018-12-31]. (原始内容存档于2020-01-12).
- ^ Remédio inédito para atrofia muscular espinhal é liberado. 2017-08-25 [2018-12-31]. (原始内容存档于2018-12-13) (巴西葡萄牙语).
- ^ Spinraza – Zulassung nun auch in der Schweiz. SMA Schweiz. 2017-09-30 [2018-12-31]. (原始内容存档于2020-10-27) (瑞士高地德语).
- ^ Spinraza Approved in Korea for SMA Treatment, Biogen Announces. SMA News Today. 2018-01-10 [2019-01-01]. (原始内容存档于2019-02-17).
- ^ Treatment for Spinal Muscular Atrophy Now Registered. www.scoop.co.nz. Scoop Health. [2019-01-01]. (原始内容存档于2019-07-06).
- ^ https://zj.zjol.com.cn/news.html?id=1500220 (页面存档备份,存于互联网档案馆) 引发争议的70万元“天价药”,怎样定价才算合理?
- ^ “70万元一针”天价药进医保 浙江SAM患者接受首批治疗.[失效链接]
- ^ NICE refuses to recommend Spinraza to treat SMA. TreatSMA. 2018-08-14 [2019-01-01]. (原始内容存档于2020-12-04).
- ^ 竺颖; 云涛. 湖南嬰兒救命藥標價70萬刷屏 網友:澳洲只需41元. 新唐人电视台 (新唐人). 2020-08-03 [2020-08-06]. (原始内容存档于2020-08-04) (中文).
- ^ 姜庚宇. 1劑特效藥內地賣70萬澳洲只需41澳元?藥企:因澳洲該藥納入醫保. 香港01. 2020-08-06 [2020-08-06]. (原始内容存档于2021-07-16) (中文).
- ^ 陈言乔. 5900萬元一針 陸藥監局批准「史上最貴藥」臨床試驗. 联合报. 2022-01-20 [2022-01-20]. (原始内容存档于2022-02-15).