鈴蘭氨酸
鈴蘭氨酸,學名L-(-)-環丁胺-2-羧酸(英語:L-(-)-Azetidine-2-carboxylic acid),縮寫為Aze或Azc,是一種非蛋白質氨基酸,為脯氨酸的同系物。在結構上,鈴蘭氨酸為一個含氮四元環吖丁啶連接一個羧基取代基得到,其與脯氨酸的區別在於前者為四元環,後者為五元環[2]。鈴蘭氨酸具有作為脯氨酸類似物的能力,可以代替脯氨酸整合到蛋白質中。
| 鈴蘭氨酸[1] | |
|---|---|
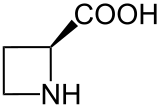
| |
| IUPAC名 Azetidine-2-carboxylic acid | |
| 別名 | L-(-)-環丁胺-2-羧酸 氮雜環丁烷-2-羧酸 吖丁啶-2-羧酸 |
| 識別 | |
| CAS號 | 2133-34-8 |
| PubChem | 16486(L-) |
| ChemSpider | 15628 |
| SMILES |
|
| InChI |
|
| InChIKey | IADUEWIQBXOCDZ-VKHMYHEABQ |
| ChEBI | 6198 |
| KEGG | C08267 |
| IUPHAR配體 | 4686 |
| 性質 | |
| 化學式 | C4H7NO2 |
| 摩爾質量 | 101.104 g/mol g·mol⁻¹ |
| 外觀 | 晶體顆粒 |
| 密度 | 1.275 g/cm3 |
| 熔點 | 215 °C(488 K) |
| 沸點 | 242 °C(515 K) |
| 溶解性(水) | 5.0 g/100 ml |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
合成
編輯鈴蘭氨酸可由γ-羥基丁酸通過α-溴化反應少量獲得的。溴化反應得到的γ-氨基-α-溴丁酸中間體中除去溴化氫,再用氫氧化鋇溶液處理進行環合即可得到。光學活性的鈴蘭氨酸是通過將α,γ-二氨基丁酸二鹽酸鹽與亞硝酸和鹽酸混合物反應生成γ-氨基-α-氯丁酸,然後消去氯化氫,再用氫氧化鋇處理進行環化而獲得[3]。
分布
編輯鈴蘭氨酸於1955年發現,其存在於一些特定植物的根莖和新鮮葉片中,已知其存在於鈴蘭和黃精屬等天門冬科植物中。
在一些豆科植物中也發現了鈴蘭氨酸。在一些食用、園藝和糖用甜菜中也發現了少量鈴蘭氨酸[4]。
毒性
編輯研究表明,當鈴蘭氨酸被錯誤地代替脯氨酸整合到蛋白質中時,鈴蘭氨酸會阻礙競爭植物的生長並毒害捕食者。其他研究表明,鈴蘭氨酸會導致鴨、倉鼠、老鼠和兔子等各種動物出現各種毒性和致畸性疾病[2]。
鈴蘭氨酸錯誤整合到人體蛋白質中會改變膠原蛋白、角蛋白、血紅蛋白和蛋白質摺疊[5]。然而,由於缺乏詳細的毒理學數據,以及需要更多關於鈴蘭氨酸對特定蛋白質的破壞性影響的直接證據,因此目前無法確定其對人體的毒性[2]。對人類脯氨酰-轉運核糖核酸合成酶和丙氨酰-tRNA合成酶的分子研究表明,鈴蘭氨酸以脯氨酸的形式整合到蛋白質中,並在體內產生毒性[6]。由於其對丙氨酸和脯氨酸的雙重模仿作用,即使鈴蘭氨酸似乎適合兩種tRNA合成酶的活性位點,它也會被丙氨酰-tRNA合成酶的轉移後編譯系統拒絕[6]。
參考文獻
編輯- ^ 默克索引, 12th Edition, 6089.
- ^ 2.0 2.1 2.2 Rubenstein E.; T. McLaughlin; R.C. Winant; A. Sanchez; M. Eckart; K.M. Krasinska; A. Chien. Azetidine-2-carboxylic Acid in the Food Chain. Phytochemistry. 2008, 70 (1): 1–5. PMID 19101705. doi:10.1016/j.phytochem.2008.11.007.
- ^ Fowden, L. Azetidine-2-carboxylic Acid: a New Cyclic Imino Acid Occurring in Plants. Biochemical Journal. 1956, 64 (2): 323–331. PMC 1199734 . PMID 13363844. doi:10.1042/bj0640323.
- ^ Seigler, David S. Plant secondary metabolism. Kluwer Academic. 1998: 222. ISBN 0-412-01981-7.
- ^ Rubenstein E.; H. Zhou; K.M. Krasinska; A. Chien; C.H. Becker. Azetidine-2-carboxylic Acid in Garden Beets. Phytochemistry. 2006, 67 (9): 898–903. PMID 16516254. doi:10.1016/j.phytochem.2006.01.028.
- ^ 6.0 6.1 Song, Y; Zhou, H; Vo, MN; Shi, Y; Nawaz, MH; Vargas-Rodriguez, O; Diedrich, JK; Yates, JR; Kishi, S; Musier-Forsyth, K; Schimmel, P. Double mimicry evades tRNA synthetase editing by toxic vegetable-sourced non-proteinogenic amino acid.. Nature Communications. 22 December 2017, 8 (1): 2281. Bibcode:2017NatCo...8.2281S. PMC 5741666 . PMID 29273753. doi:10.1038/s41467-017-02201-z.