三甲基鋁
三甲基鋁是一個化合物,化學式是Al2(CH3)6, 可以縮寫為Al2Me6, (AlMe3)2或者TMA。它是一種自燃的無色液體,在工業上是很重要的有機鋁化合物。它的蒸氣散發到空氣中後會產生白煙(氧化鋁)。
| 三甲基鋁 | |
|---|---|
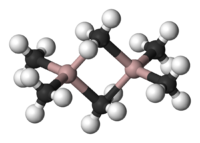
| |

| |
| IUPAC名 Trimethylalane | |
| 識別 | |
| CAS號 | 75-24-1 |
| PubChem | 16682925 |
| ChemSpider | 10606585 |
| SMILES |
|
| InChI |
|
| InChIKey | JLTRXTDYQLMHGR-MZZUXTGEAJ |
| 性質 | |
| 化學式 | C6H18Al2 |
| 摩爾質量 | 144.17 g/mol 72.09 g/mol (C3H9Al) g·mol⁻¹ |
| 外觀 | 無色液體 |
| 密度 | 0.752 g/cm3 |
| 熔點 | 15 °C(288 K) |
| 沸點 | 125 °C(398 K)([1][2]) |
| 溶解性(水) | 與水反應 |
| 蒸氣壓 | 1.2 kPa (20 °C) 9.24 kPa (60 °C)[1] |
| 黏度 | 1.12 cP (20 °C) 0.9 cP (30 °C) |
| 熱力學 | |
| ΔfHm⦵298K | −136.4 kJ/mol[2] |
| S⦵298K | 209.4 J/mol·K[2] |
| 熱容 | 155.6 J/mol·K[2] |
| 危險性 | |
| 警示術語 | R:R14, R17, R34 |
| 安全術語 | S:S16, S43, S45 |
| 歐盟分類 | |
GHS危險性符號  [1] [1]
| |
| GHS提示詞 | 危險 |
| H-術語 | H250, H260, H314[1] |
| P-術語 | P222, P223, P231+232, P280, P370+378, P422[1] |
| 主要危害 | 自燃性 |
| NFPA 704 | |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
結構與化學鍵
編輯Al2Me6在常溫常壓下是二聚體[3],在結構上和乙硼烷相似。像乙硼烷一樣,這個化合物同樣有兩個三中心兩電子鍵:在兩個鋁原子之間有一個共用的甲基。端位的Al-C鍵和中間的Al-C鍵的距離分別是1.97和2.14埃[4],中間甲基上的每個碳原子都被三個氫原子和兩個鋁原子包圍。這些甲基在分子內和分子間可以自由轉換。
三中心兩電子鍵是"缺少電子"的分子而且傾向於與路易斯鹼反應,產物含有兩中心兩電子鍵。例如和氨反應生成加合物 R3N-AlMe3。Al2Me6與氯化鋁反應生成的(AlMe2Cl)2是另一個遵守八隅體規則的反應產物。
AlMe3的單體含有一個鋁原子和三個甲基,這種單體僅會在高溫低壓下存在[3]。VSEPR理論預言了它如同BMe3一樣是三角平面(有一個三重軸)對稱。後來電子繞射的結果也證實了這個預言。[5]
製備與應用
編輯TMA可以通過兩步反應製取,總反應式如下:
- 2 Al + 6 CH3Cl + 6 Na → Al2(CH3)6 + 6 NaCl
TMA主要用來生產甲基鋁氧烷,用於活化烯烴聚合的齊格勒-納塔催化劑。TMA也作為甲基化試劑。用於亞甲基酯和酮的Tebbe試劑就是由TMA製備的。TMA也用在探空火箭上,用作研究上層大氣風模式的示蹤劑。
通過化學氣相沉積或原子層沉積過程,TMA也可用於製造半導體的沉積高介電系數介電質薄膜,例如Al2O3。
TMA與叔胺DABCO形成化合物,這比直接處理TMA本身更安全[6]。
在Cp2ZrCl2(二氯二茂鋯)的催化下,(CH3)2Al-CH3能夠與炔烴反應生成烯基鋁,這個反應在被稱為carboalumination的有機合成反應中起作用[7]。
NASA的ATREX任務利用TMA與空氣接觸產生的白煙研究高空急流。
半導體級TMA
編輯TMA是有機金屬化學氣相沉積法(MOVPE)製造含鋁半導體(如AlAs, AlN, AlP, AlSb, AlGaAs, AlInGaAs, AlInGaP, AlGaN, AlInGaN, AlInGaNP等)中有機金屬的重要來源。TMA的質量標準主要關注元素雜質、氧化雜質和有機雜質的含量。
參看
編輯- ^ 1.0 1.1 1.2 1.3 1.4 來源:Sigma-Aldrich Co., Trimethylaluminum (2014-05-05查閱).
- ^ 2.0 2.1 2.2 2.3 http://chemister.ru/Database/properties-en.php?dbid=1&id=3290(英文)
- ^ 3.0 3.1 Carlsson, J.; Gorbatkin, S.; Lubben, D.; Greene, J. E. Thermodynamics of the homogeneous and heterogeneous decomposition of trimethylaluminum, monomethylaluminum, and dimethylaluminumhydride: Effects of scavengers and ultraviolet-laser photolysis. Journal of Vacuum Science and Technology B. 1991, 9 (6): 2759–2770. doi:10.1116/1.585642.
- ^ Holleman, A. F.; Wiberg, E. Inorganic Chemistry. San Diego: Academic Press. 2001. ISBN 0-12-352651-5.
- ^ Almennin, A.; Halvorse, S.; Haaland, A. Gas Phase Electron Diffraction Investigation of Molecular Structures of Trimethylaluminum Monomer and Dimer. Acta Chemica Scandinavica. 2005, 44 (15): 2232–2234. doi:10.3891/acta.chem.scand.25-1937.
- ^ Biswas, K.; Prieto, O.; Goldsmith, P. J.; Woodward, S. Remarkably Stable (Me3Al)2 · DABCO and Stereoselective Nickel-Catalyzed AlR3 (R = Me, Et) Additions to Aldehydes. Angewandte Chemie International Edition. 2005, 44 (15): 2232–2234. PMID 15768433. doi:10.1002/anie.200462569.
- ^ Negishi, E.; Matsushita, H. (1984). "Palladium-Catalyzed Synthesis of 1,4-Dienes by Allylation of Alkenyalane: α-Farnesene [1,3,6,10-Dodecatetraene, 3,7,11-trimethyl-]". Org. Synth. 62: 31; Coll. Vol. 7: 245.
