環丙酮
化合物
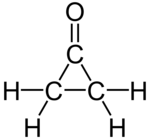
環丙酮(化學式:C3H4O)是環丙烷的氧代衍生物。其熔點為-90°C,很不穩定,可通過乙烯酮與重氮甲烷在-145°C時反應製備。[1][2] 由於母體化合物不甚穩定,合成中使用環丙酮的縮酮[3][4] 代替環丙酮,效果是等同的。
| 環丙酮 | |
|---|---|
| |
| IUPAC名 cyclopropanone | |
| 識別 | |
| CAS號 | 5009-27-8 |
| PubChem | 138404 |
| ChemSpider | 122027 |
| SMILES |
|
| InChI |
|
| InChIKey | VBBRYJMZLIYUJQ-UHFFFAOYAV |
| 性質 | |
| 化學式 | C3H4O |
| 莫耳質量 | 56.06326 g·mol⁻¹ |
| 密度 | 0.867 g/mL,25 °C |
| 熔點 | −90 °C |
| 沸點 | 50-53 °C,22 mmHg |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
衍生物
編輯環丙酮環系是很多有機反應的中間體。Favorskii重排中便涉及到一個環丙酮並環的中間體。
環丙酮環系水合形成羰基水合物(偕二醇),羰基碳變為sp3雜化,可以使所需的鍵角減小,緩解張力。因此環丙酮環系的水合物比較穩定。
用偕二鹵代卡賓與烯烴反應,生成的產物經水解後,可以得到環丙酮的衍生物。它們可以作為1,3-偶極體,與環狀雙烯體(如呋喃)發生環加成反應。[6][7] 對此,有人提出以下的價互變異構來解釋這個現象:
另兩個結構都為碳-碳鍵斷開,一個為電荷分離,另一個為雙自由基結構。有些環丙酮的反應支持了以上機理:光學純的(+)-反式-2,3-二叔丁基環丙酮加熱到80°C時,會發生外消旋化;[8] 以及光照時,氧代脫氫吡唑烷放出氮氣生成茚滿的反應(見下),便都可看作是採取了上述的互變異構機理。[9]
參見
編輯參考資料
編輯- ^ Preparation and characterization of cyclopropanone, methylcyclopropanone, 2,2-dimethylcyclopropanone and tetramethylcyclopropanone N. J. Turro and W. B. Hammond, Tetrahedron, Volume 24, Issue 18, 1968, Pages 6017-6028 doi:10.1016/S0040-4020(01)90985-8
- ^ Cryochemical synthesis and molecular energetics of cyclopropanone and some related compounds E. F. Rothgery, R. J. Holt, H. A. McGee, , Jr. J. Am. Chem. Soc.; 1975; 97(17); 4971-4973. doi:10.1021/ja00850a034
- ^ Organic Syntheses, Coll. Vol. 7, p.131 (1990); Vol. 63, p.147 (1985). [Link http://www.orgsynth.org/orgsyn/pdfs/CV7P0131.pdf (頁面存檔備份,存於網際網路檔案館)]
- ^ Datasheet commercial supplier Link 網際網路檔案館的存檔,存檔日期2007-09-26.
- ^ Cyclopropanones Nicholas J. Turro, Acc. Chem. Res.; 1969; 2(1); 25-32. doi:10.1021/ar50013a004
- ^ Cyclopropanones. XII. Cycloaddition reactions of cyclopropanones Nicholas J. Turro, Simon S. Edelson, John R. Williams, Thomas R. Darling, Willis B. Hammond, J. Am. Chem. Soc.; 1969; 91(9); 2283-2292. doi:10.1021/ja01037a018
- ^ Cyclopropanones. XVII. Kinetics of the cycloaddition reaction of cyclopropanones with 1,3-dienes Simon S. Edelson, Nicholas J. Turro J. Am. Chem. Soc.; 1970; 92(9); 2770-2773. doi:10.1021/ja00712a030
- ^ Thermal reactions of a cyclopropanone. Racemization and decarbonylation of trans-2,3-di-tert-butylcyclopropanone Frederick D. Greene, David B. Sclove, Jose F. Pazos, Ronald L. Camp J. Am. Chem. Soc.; 1970; 92(25); 7488-7488. doi:10.1021/ja00728a051
- ^ First Direct Detection of 2,3-Dimethyl-2,3-diphenylcyclopropanone Andrey G. Moiseev, Manabu Abe, Evgeny O. Danilov, and Douglas C. Neckers, J. Org. Chem.; 2007; 72(8) pp 2777 - 2784; (Article) doi:10.1021/jo062259r