磷黴素
此條目的引用需要清理,使其符合格式。 (2021年7月31日) |
磷黴素是一種主要用於治療低尿路感染的抗生素,商標名是Monurol,[1]不適用於腎臟感染,[1]偶爾用於治療前列腺感染。[1]一般口服。[1]
 | |
 | |
| 臨床資料 | |
|---|---|
| 商品名 | Monuril, Monurol, others |
| 其他名稱 | Phosphomycin, phosphonomycin, fosfomycin tromethamine |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a697008 |
| 給藥途徑 | 口服 |
| ATC碼 | |
| 法律規範狀態 | |
| 法律規範 | |
| 藥物動力學數據 | |
| 生物利用度 | 30–37% (by mouth, fosfomycin tromethamine); varies with food intake |
| 血漿蛋白結合率 | Nil |
| 藥物代謝 | Nil |
| 生物半衰期 | 5.7 小時 (平均) |
| 排泄途徑 | 腎和糞便 |
| 識別資訊 | |
| |
| CAS號 | 23155-02-4 78964-85-9 |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.041.315 |
| 化學資訊 | |
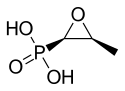
| 化學式 | C3H7O4P |
| 摩爾質量 | 138.06 g·mol−1 |
| 3D模型(JSmol) | |
| 熔點 | 94 °C(201 °F) |
| |
| |
常見的副作用包括腹瀉、噁心、頭痛和念珠菌性外陰陰道炎。[1] 嚴重的副作用可能包括過敏反應和偽膜性結腸炎。[1]雖然沒有發現妊娠期使用有害,但不推薦這樣使用。[2] 母乳餵養期單次服用似乎是安全的。[2] 它通過干擾細菌細胞壁的生成來起作用。[1]
1969年,磷黴素被發現。1996年,它在美國被批准用於醫療。[1][3] 世界衛生組織將磷黴素列為對人類醫學至關重要的物質,列入世界衛生組織基本藥物清單。[4][5] 它是一種非專利藥物。[6] 它最初由某些類型的鏈球菌生產,現在用化學方法生產。[3]
醫療用途
編輯不建議12歲以下兒童口服磷黴素。[8]
還提出了其他用途。[9] 最近全球抗生素耐藥性提高的問題導致了對使用它的新興趣。[10]
磷黴素可有效治療尿路感染和複雜性尿路感染(包括急性腎盂腎炎)。複雜尿路感染的標準用藥方案是每48或72小時口服一次,每次劑量3克,共3次給藥。或者當其以靜脈注射形式給藥時,每8小時一次,每次6克,持續7至14天。[11]
細菌敏感性
編輯磷黴素抗菌活性廣泛,對革蘭氏陽性和革蘭氏陰性病原菌均有效。對糞腸球菌(E. faecalis)、大腸桿菌(E. coli)以及各種革蘭氏陰性菌如檸檬酸桿菌(Citrobacter)和變形桿菌(Proteus)均有較強的抗菌活性。由於在低pH環境中具有較強的活性,並且主要以活性形式排出到尿液中,磷黴素已經被用於預防和治療這些泌尿系統病原體引起的尿路感染。值得注意的是,它對腐生性鏈球菌(S. saprophyticus),克雷伯氏菌(Klebsiella)和腸桿菌(Enterobacter)的活性是可變的,應通過最小抑菌濃度檢測確認。由於該藥物不受交叉耐藥問題的影響,所以對產超廣譜β-內醯胺酶病原體,特別是產ESBL大腸桿菌的活性是良至優的。現有的臨床數據支持其用於易感生物引起的簡單型尿路感染。然而,敏感性突變點64毫克/升不應用於全身感染。
抗藥性
編輯治療中經常產生細菌耐藥性,使得磷黴素不適用於嚴重感染的持續治療。細菌發生突變,非必需甘油磷酸轉運蛋白失活,使其對磷黴素產生抗藥性。[12][13][14]
將磷黴素與至少另一種活性藥物一起使用可降低產生細菌耐藥性的風險。磷黴素與許多其他抗生素協同作用,包括頭孢菌素、碳青黴烯、達托黴素和氨基糖苷類。[15]
三種相關的磷黴素抗性酶(命名為 FosA、FosB 和 FosX)是乙二醛酶超家族的成員。這些酶通過親核攻擊磷黴素的碳1,打開環氧化物環,使藥物無效。
這些酶因反應中使用的親核試劑的種類而異: FosA為穀胱甘肽,FosB為桿菌硫醇,[17][18]FosX為水。[16]
一般來說,FosA 和 FosX 酶是由革蘭氏陰性菌產生的,而 FosB 是由革蘭氏陽性菌產生的。[16]
副作用
編輯該藥物耐受性良好,有害副作用發生率低。[7]
作用機制
編輯與其名字不同(以-黴素結尾),磷黴素不是一種大環內酯。磷黴素通過滅活UDP-N-乙醯氨基葡萄糖-3- 烯醇丙酮基轉移酶抑制細菌細胞壁生物合成。[20] 這種酶催化肽聚糖生物合成的必要步驟:連接磷酸烯醇式丙酮酸(PEP)到UDP-N-乙醯葡萄糖胺的3'-羥基,PEP提供了肽聚糖相互連接的橋接劑。磷黴素是一種PEP 類似物,可以通過烷基化活性部位半胱氨酸殘基(大腸桿菌中的Cys115)來抑制MurA。[21][22]
磷黴素通過甘油磷酸轉運蛋白進入細菌細胞。[23]
歷史
編輯磷黴素(Fosfomycin,原名phosphonomycin)是由默克公司和西班牙的西班牙青黴菌和抗生素公司(CEPA)共同發現的。它首先是通過篩選從土壤樣本中分離出來的弗雷迪鏈黴菌的肉湯培養物來分離的,確定其能夠使生長中的細菌形成原生質球。1969年發表的一系列論文描述了這一發現。[24] CEPA於1971年在其阿蘭胡埃茲設施開始工業規模生產磷黴素。[25]
生產
編輯從弗氏鏈黴菌(Streptomyces fradiae)中克隆並測序了磷黴素生物合成基因簇的全序列。由趙惠民和威爾弗雷德 · 范德 · 東克(Wilfred van der Donk)研究小組的賴安 · 伍德爾(Ryan Woodyer)實現了磷黴素在李氏鏈黴菌(S. lividans)中的異源生產。[26]
參考文獻
編輯- ^ 1.0 1.1 1.2 1.3 1.4 1.5 1.6 1.7 Fosfomycin Tromethamine Monograph for Professionals. Drugs.com. [29 October 2019]. (原始內容存檔於2019-10-29) (英語).
- ^ 2.0 2.1 Fosfomycin (Monurol) Use During Pregnancy. Drugs.com. [29 October 2019]. (原始內容存檔於2019-10-29) (英語).
- ^ 3.0 3.1 Antibiotic and Chemotherapy E-Book. Elsevier Health Sciences. 2010: 259 [2021-07-31]. ISBN 9780702047657. (原始內容存檔於2021-08-28) (英語).
- ^ World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ Critically important antimicrobials for human medicine 6th revision. Geneva: World Health Organization. 2019. ISBN 9789241515528.
- ^ British national formulary : BNF 76 76. Pharmaceutical Press. 2018: 560–561. ISBN 9780857113382.
- ^ 7.0 7.1 Fosfomycin tromethamine. A review of its antibacterial activity, pharmacokinetic properties and therapeutic efficacy as a single-dose oral treatment for acute uncomplicated lower urinary tract infections. Drugs. April 1997, 53 (4): 637–56. PMID 9098664. doi:10.2165/00003495-199753040-00007.
- ^ MONURIL SACHETS 3G. [May 26, 2014]. (原始內容存檔於2014-05-28).
- ^ Fosfomycin: use beyond urinary tract and gastrointestinal infections. Clinical Infectious Diseases. April 2008, 46 (7): 1069–77. PMID 18444827. doi:10.1086/527442.
- ^ Potential of old-generation antibiotics to address current need for new antibiotics. Expert Review of Anti-Infective Therapy. October 2008, 6 (5): 593–600. PMID 18847400. doi:10.1586/14787210.6.5.593.
- ^ Oral and Intravenous Fosfomycin for the Treatment of Complicated Urinary Tract Infections. The Canadian Journal of Infectious Diseases & Medical Microbiology (Hindawi Limited). 2020-03-28, 2020: 8513405. PMC 7142339 . PMID 32300381. doi:10.1155/2020/8513405.
- ^ The mechanism of action of fosfomycin (phosphonomycin). Annals of the New York Academy of Sciences. May 1974, 235 (1): 364–86. Bibcode:1974NYASA.235..364K. PMID 4605290. doi:10.1111/j.1749-6632.1974.tb43277.x.
- ^ Molecular Mechanisms and Clinical Impact of Acquired and Intrinsic Fosfomycin Resistance. Antibiotics. April 2013, 2 (2): 217–36. PMC 4790336 . PMID 27029300. doi:10.3390/antibiotics2020217.
- ^ Fosfomycin as Partner Drug for Systemic Infection Management. A Systematic Review of Its Synergistic Properties from In Vitro and In Vivo Studies. Antibiotics. August 2020, 9 (8): 500. PMC 7460049 . PMID 32785114. doi:10.3390/antibiotics9080500.
- ^ 16.0 16.1 16.2 https://archive.org/details/gluthionetransfe00sies/page/367
|chapterurl=缺少標題 (幫助). Gluthione Transferases and Gamma-Glutamyl Transpeptidases. Methods in Enzymology 401. 2005: 367–379. ISBN 9780121828066. PMID 16399398. doi:10.1016/S0076-6879(05)01023-2. - ^ Chemical and Chemoenzymatic syntheses of bacillithiol: a unique low-molecular-weight thiol amongst low G + C Gram-positive bacteria. Angewandte Chemie. July 2011, 50 (31): 7101–4. PMID 21751306. doi:10.1002/anie.201100196.
- ^ Mechanistic studies of FosB: a divalent-metal-dependent bacillithiol-S-transferase that mediates fosfomycin resistance in Staphylococcus aureus. The Biochemical Journal. April 2013, 451 (1): 69–79. PMC 3960972 . PMID 23256780. doi:10.1042/BJ20121541.
- ^ Product of fosC, a gene from Pseudomonas syringae, mediates fosfomycin resistance by using ATP as cosubstrate. Antimicrobial Agents and Chemotherapy. July 1995, 39 (7): 1569–73. PMC 162783 . PMID 7492106. doi:10.1128/aac.39.7.1569.
- ^ MurA (MurZ), the enzyme that catalyzes the first committed step in peptidoglycan biosynthesis, is essential in Escherichia coli. Journal of Bacteriology. July 1995, 177 (14): 4194–7. PMC 177162 . PMID 7608103. doi:10.1128/jb.177.14.4194-4197.1995.
- ^ Functional consequence of covalent reaction of phosphoenolpyruvate with UDP-N-acetylglucosamine 1-carboxyvinyltransferase (MurA). The Journal of Biological Chemistry. April 2012, 287 (16): 12657–67. PMC 3339971 . PMID 22378791. doi:10.1074/jbc.M112.342725.
- ^ Determination of the pKa value of C115 in MurA (UDP-N-acetylglucosamine enolpyruvyltransferase) from Enterobacter cloacae. Biochemistry. October 2000, 39 (41): 12671–7. PMID 11027147. doi:10.1021/bi001310x.
- ^ Interaction of fosfomycin with the glycerol 3-phosphate transporter of Escherichia coli. Biochimica et Biophysica Acta (BBA) - General Subjects. December 2011, 1810 (12): 1323–9. PMID 21791237. doi:10.1016/j.bbagen.2011.07.006.
- ^ Chapter 2, Rational approaches to antibiotic discovery: pre-genomic directed and phenotypic screening. Springer. 2011: 46. ISBN 978-1-4614-1400-1. doi:10.1007/978-1-4614-1400-1_2.
- ^ Encros About us: Our history. 網際網路檔案館的存檔,存檔日期2011-09-14.
- ^ Heterologous production of fosfomycin and identification of the minimal biosynthetic gene cluster. Chemistry & Biology. November 2006, 13 (11): 1171–82. PMID 17113999. doi:10.1016/j.chembiol.2006.09.007.
- ^ Marocco, Christian P.; Davis, Erik V.; Finnell, Julie E.; Nguyen, Phung-Hoang; Mateer, Scott C.; Ghiviriga, Ion; Padgett, Clifford W.; Feske, Brent D. Asymmetric synthesis of (−)-fosfomycin and its trans-(1S,2S)-diastereomer using a biocatalytic reduction as the key step. Tetrahedron: Asymmetry (Elsevier BV). 2011, 22 (18–19): 1784–1789. ISSN 0957-4166. doi:10.1016/j.tetasy.2011.10.009.