作用机制
作用机制(英语:mechanism of action,MOA)亦称作用机理,或是作用机转,在药理学和毒理学中是指一个特定分子(如药物分子、毒物分子)在分子层面上发挥特定药理或毒理作用的机理。[2][3]一般而言,特定分子的作用机制通常是与酶、受体等生物大分子发生相互作用。[4]
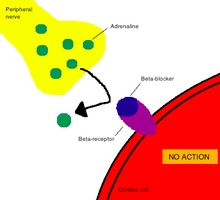
不与受体结合的药物透过简单与体内的化学或物理性质相互作用而产生相应的治疗效果。以这种方式发生作用的药物,常见例子是抗酸剂和泻药。[3]
相较之下,作用方式 (mode of action,MoA) 描述的是由于活体暴露于某种物质而导致的细胞层面的功能或解剖学变化。
重要性
编辑阐明药物的作用机制有助于药物毒理学和安全性的评估。
- 以细胞膜和电子传递链为标靶的抗感染药物,其副作用就可能比以β-葡聚糖、肽聚糖等细菌细胞壁成分以及原核生物的70S核糖体具有更强的副作用。这是因为人体细胞无细胞壁结构。人作为真核生物,核糖体的沉降系数是80S,与细菌的70S核糖体在结构上有显著区别,但细胞膜的结构以及电子传递链的组成却与原核生物有相似性。[5][6]
- 透过了解药物某位点与受体之间的相互作用,可复制这种相互作用的方式来配制别的药物,而产生相同的治疗效果。事实上这是创造新药的方法。
- 可协助确定哪些患者最有可能对治疗产生反应。例如由于已知乳癌药物曲妥珠单抗是以HER2/neu蛋白质为标靶,因此可筛检肿瘤中是否有此蛋白质,以确定患者是否可从曲妥珠单抗治疗中受益。[7][8]
- 因为可在患者体内监测药物对目标途径的影响,而能确定更好的剂量。例如透过测量患者的血液胆固醇水平,再决定使用他汀类药物剂量。[7]
- 得以将不同药物联合使用以降低抗药性出现。透过了解抗感染或抗癌药物作用于不同细胞结构,可使用同时抑制多个标靶的混合物,而降低微生物或肿瘤DNA中发生单一突变,导致抗药性和治疗失败的风险。[5][9][10][11]
- 得以识别该药物的其他适应症。例如发现西地那非可抑制磷酸二酯酶 5 (PDE-5) 蛋白质,而将该药物功能转换,用于肺高压治疗。[12][13]
鉴定方法
编辑显微镜观察法
编辑生物活性化合物会诱导目标细胞发生表型变化,可透过显微镜观察,深入了解化合物的作用机制。[14]
使用抗生素时,目标细胞向原生质球转化,显示肽聚糖合成可能受到抑制,而目标细胞的丝状化可能是由于PBP3、FtsZ或DNA合成受到抑制的结果。抗生素引起的其他变化包括卵形细胞形成、假多细胞形式、局部肿胀、凸起形成、起泡和肽聚糖增厚。[5]就化学疗法药剂而言,气泡可能表示该化合物正在破坏癌症细胞膜。[15]
目前采此种方法的限制是需手动操作和解读数据均要花费时间,自动显微镜和影像分析软件的出现与进化将有助于将问题解决。[5][14]
生化方法
编辑直接生化方法包括将候选药物蛋白质或小分子标记,并在体内追踪。[16]这是最直接的方法,可找到与相关小目标结合的标靶蛋白,例如药物轮廓的基本表示,以识别出药物的药效团。由于标记分子与蛋白质之间的物理相互作用,生化方法可用于确定药物的毒性、有效性和作用机制。
计算推理法
编辑通常计算推理法是基于电脑对模式的辨识,用于预测小分子药物的蛋白质标靶。[16]但此法也可用于为现有或新开发药物寻找新的标靶。通过识别药物分子的药效团,进行模式分析,而辨识出新的标靶。[16]此法提供一可能的药物作用机制的洞察,因为我们已经知道药物的某些功能成分在与蛋白质上的特定区域相互作用时可发挥作用,而产生治疗效果。
组学法
编辑组学方法利用各种组学技术,例如化学蛋白质组学、反向遗传学和基因组学、转录组学和蛋白质组学等技术,来识别特定化合物的潜在标靶。[17]例如反向遗传学和基因组学方法可结合基因干扰技术(例如CRISPR-Cas9或小分子干扰DNA)加上化合物,一起找出哪些基因的沉默(knockdown)或剔除会消除化合物的药理作用。另一方面,可将化合物的转录组学和蛋白质组学分析结果与已知标靶化合物的分析结果进行比较。借助计算推论,我们可对化合物的作用机制做出假设,然后进一步验证。[17]
作用机制已被了解的药物
编辑有许多药物的作用机制已被了解。阿司匹林即为其中一例。
阿司匹林
编辑阿司匹林的作用机制可对环氧合酶产生不可逆转的抑制,[18]因此可抑制前列腺素和血栓素产生,而能减轻疼痛和发炎。这种机制是阿司匹林所特有,对所有其他非类固醇类抗发炎药 (NSAID) 来说并非如此。阿司匹林是NSAID中唯一能不可逆转抑制环氧合酶-1 (COX-1)的药物。[19]
作用机制尚未知的药物
编辑有些药物的治疗作用机制仍未知,或是被完全了解,但仍然能发挥作用。
作用方式
编辑作用方式(mode of action,MoA)则是近似术语,与作用机制的区别在于:作用方式是指由于活体暴露于某种物质而导致的"细胞层面"的功能或解剖学变化。[2][20]而作用机制是一个更具体,关注药物本身与酶或受体之间的相互作用及作用的特定形式,无论是透过抑制、活化、激动或拮抗作用。此外,"作用机制"是药理学的主要术语,而"作用方式"更常出现在微生物学领域或生物学的某些方面。
参见
编辑参考文献
编辑- ^ Ogrodowczyk, M.; Dettlaff, K.; Jelinska, A. Beta-blockers: Current state of knowledge and perspectives. Mini Reviews in Medicinal Chemistry. 2016, 16 (1): 40–54. PMID 26471965. doi:10.2174/1389557515666151016125948.
- ^ 2.0 2.1 NIH. Toxic Effects. NIH. [2018-12-21]. (原始内容存档于2017-01-25).
- ^ 3.0 3.1 Spratto, G.R.; Woods, A.L. Delmar Nurse's Drug Handbook. Cengage Learning. 2010. ISBN 978-1-4390-5616-5.
- ^ Grant, R.L.; Combs, A.B.; Acosta, D. (2010) "Experimental Models for the Investigation of Toxicological Mechanisms". In McQueen, C.A. Comprehensive Toxicology (2nd ed.). Oxford: Elsevier. p. 204. ISBN 978-0-08-046884-6.
- ^ 5.0 5.1 5.2 5.3 5.4 Cushnie, T.P.; O’Driscoll, N.H.; Lamb, A.J. Morphological and ultrastructural changes in bacterial cells as an indicator of antibacterial mechanism of action. Cellular and Molecular Life Sciences. 2016, 73 (23): 4471–4492 [2017-10-07]. PMID 27392605. S2CID 2065821. doi:10.1007/s00018-016-2302-2. hdl:10059/2129 . (原始内容存档于2017-10-07).
- ^ Chang, C.C.; Slavin, M.A.; Chen, S.C. New developments and directions in the clinical application of the echinocandins. Archives of Toxicology. 2017, 91 (4): 1613–1621. PMID 28180946. S2CID 31029386. doi:10.1007/s00204-016-1916-3.
- ^ 7.0 7.1 No authors listed. Mechanism matters. Nature Medicine. 2010, 16 (4): 347. PMID 20376007. doi:10.1038/nm0410-347 .
- ^ Joensuu, H. Escalating and de-escalating treatment in HER2-positive early breast cancer. Cancer Treatment Reviews. 2017, 52: 1–11 [2017-10-07]. PMID 27866067. doi:10.1016/j.ctrv.2016.11.002 . (原始内容存档于2019-08-05).
- ^ Cihlar, T.; Fordyce, M. Current status and prospects of HIV treatment. Current Opinion in Virology. 2016, 18: 50–56. PMID 27023283. doi:10.1016/j.coviro.2016.03.004 .
- ^ Antony, H.A.; Parija, S.C. Antimalarial drug resistance: An overview. Tropical Parasitology. 2016, 6 (1): 30–41. PMC 4778180 . PMID 26998432. doi:10.4103/2229-5070.175081 .
- ^ Bozic, I.; Reiter, J.G.; Allen, B.; Antal, T.; Chatterjee, K.; Shah, P.; Moon, Y.S.; Yaqubie, A.; Kelly, N.; Le, D.T.; Lipson, E.J.; Chapman, P.B.; Diaz, L.A.; Vogelstein, B.; Nowak, M.A. Evolutionary dynamics of cancer in response to targeted combination therapy. eLife. 2013, 2: Article ID e00747. PMC 3691570 . PMID 23805382. doi:10.7554/eLife.00747 .
- ^ Tari, L.; Vo, N.; Liang, S.; Patel, J.; Baral, C.; Cai, J. Identifying novel drug indications through automated reasoning. PLOS ONE. 2012, 7 (7): Article e40946. Bibcode:2012PLoSO...740946T. PMC 3402456 . PMID 22911721. doi:10.1371/journal.pone.0040946 .
- ^ Hayardeny, L. Why is it important to know the mode of action of drugs? (Conference presentation). New Frontiers in Neuroscience and Methods of Transdisciplinary Education Workshop, Tel Aviv University, Israel: Tel Aviv University. 2014 [2017-03-18]. (原始内容存档于2017-03-18) (英语).
- ^ 14.0 14.1 Fetz, V.; Prochnow, H.; Brönstrup, M.; Sasse, F. Target identification by image analysis (PDF). Natural Product Reports. 2016, 33 (5): 655–667 [2019-09-26]. PMID 26777141. doi:10.1039/c5np00113g. hdl:10033/621283. (原始内容存档 (PDF)于2020-06-02).
- ^ Dubovskii, P.V.; Vassilevski, A.A.; Kozlov, S.A.; Feofanov, A.V.; Grishin, E.V.; Efremov, R.G. Latarcins: versatile spider venom peptides. Cellular and Molecular Life Sciences. 2015, 72 (23): 4501–4522. PMID 26286896. S2CID 14177431. doi:10.1007/s00018-015-2016-x.
- ^ 16.0 16.1 16.2 Schenone, M.; Dančík, V.; Wagner, B.K.; Clemons, P.A. Target identification and mechanism of action in chemical biology and drug discovery. Nature Chemical Biology. 2013, 9 (4): 232–240. ISSN 1552-4450. PMC 5543995 . PMID 23508189. doi:10.1038/nchembio.1199.
- ^ 17.0 17.1 Wecke, T.; Mascher, T. Antibiotic research in the age of omics: from expression profiles to interspecies communication. Journal of Antimicrobial Chemotherapy. 2011, 66 (12): 2689–2704. PMID 21930574. doi:10.1093/jac/dkr373.
- ^ Tóth, L.; Muszbek, L.; Komaromi, I. Mechanism of the irreversible inhibition of human cyclooxygenase-1 by aspirin as predicted by QM/MM calculations. Journal of Molecular Graphics and Modelling. 2013, 40: 99–109. PMID 23384979. doi:10.1016/j.jmgm.2012.12.013.
- ^ Sharma, S.; Sharma, S. C. An update on eicosanoids and inhibitors of cyclooxygenase enzyme systems. Indian Journal of Experimental Biology. 1997, 35 (10): 1025–1031. ISSN 0019-5189. PMID 9475035.
- ^ Mechanisms and mode of dioxin action (PDF). U.S. Environmental Protection Agency. [2012-06-11]. (原始内容存档 (PDF)于2016-12-28).