艰难拟梭菌
艰难拟梭菌[1](学名:Clostridioides difficile,C. diff)又称艰难类梭菌[2],旧名艰难梭菌[3](Clostridium difficile)、困难梭状芽孢杆菌[4]、困难梭状杆菌[5][6],属厌氧性拟梭菌属细菌,一般寄生在人的肠道内。厌氧性细菌是指那些在无氧条件下要比在有氧环境下生长好的细菌,而人的肠道正好是一个相对无氧的环境。如果过度服用某些抗生素,艰难拟梭菌的菌群生长速度加快,影响肠道中其他细菌,引发炎症。
| 艰难拟梭菌 | |
|---|---|

| |
| 琼脂平板上的艰难拟梭菌群落 | |
| |
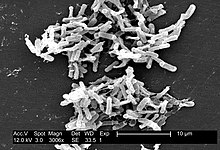
| 艰难拟梭菌的显微照相 | |
| 科学分类 | |
| 域: | 细菌域 Bacteria |
| 门: | 芽孢杆菌门 Bacillota |
| 纲: | 梭菌纲 Clostridia |
| 目: | 真细菌目 Eubacteriales |
| 科: | 消化链球菌科 Peptostreptococcaceae |
| 属: | 拟梭菌属 Clostridioides |
| 种: | 艰难拟梭菌 C. difficile
|
| 二名法 | |
| Clostridioides difficile Hall & O'Toole, 1935
| |
艰难拟梭菌是梭菌属的一个成员,对氧十分敏感,很难分离培养,故得名。梭菌属成员很多,可分为几个群,其中有几个成员对人是致病性的。最著名的有产气荚膜梭菌、破伤风梭菌和肉毒梭菌。产气荚膜梭菌可引起伤口气性坏疽、食物中毒、肌肉坏死、梭菌蜂窝织炎等,破伤风梭菌可引起破伤风,肉毒梭菌可引起肉毒中毒。肉毒中毒的典型临床特征是急性弛缓麻痹,先从双侧颅神经阻碍开始,包括面部、头颅和咽部的肌肉,然后对称性下降,包括喉部和肢体肌肉。由于舌或咽部肌瘫痪可引起的呼吸困难,隔膜和肋部的瘫痪可能引起死亡。产气荚膜梭菌是一种常见的引起食物中毒的细菌。
艰难拟梭菌发现于1935年,但直到1977年发现本菌与临床长期使用某些抗生素(氨苄青霉素、头孢霉素、红霉素、氯林可霉素等)引起的伪膜性结肠炎有关,方被重视。
艰难拟梭菌广泛分布于自然环境中,如土壤、干草、沙、一些大型动物(牛、驴和马)的粪便,及狗、猫、啮齿动物和人的粪便,除此之外还大量存在于水和动物的肠道中。婴儿的粪便中常含有艰难拟梭菌,为新生婴儿肠道中正常菌群,大约50% 12月龄婴儿的肠道中有艰难拟梭菌,2岁以上儿童的带菌率大约为3%,但此菌在健康成人中出现频率较低,无症状带菌的成人在瑞典是1.9%,在日本为15.4%,这种细菌会产生肠毒素和细胞毒素[7],是一种能引起伪膜性结肠炎的厌氧梭菌属细菌[8],也是一种导致住院病人腹泻的常见细菌,病征由轻度以至严重的腹泻。
致病因子
编辑主要为 toxin A(TcdA)、toxin B(TcdB)[9][10],借由将尿苷二磷酸葡萄糖 (UDP-glucose)的葡萄糖转移至 Rho small GTPase(糖基化)使其失活,这将导致:
疾病与症状
编辑艰难拟梭菌可定植于人体肠道而不出现症状,因为肠道正常菌丛可压制其生长,但当使用大量广谱抗生素(如头孢菌素),会杀死正常菌丛,使艰难拟梭菌大量增生并产生毒素,导致腹泻、恶心、发烧,甚至导致伪膜性结肠炎及毒性巨结肠症(Toxic megacolon)致死。
治疗
编辑参考资料
编辑- ^ 赵敏,欧阳紫柔,赵建宏.艰难拟梭菌毒素致病机制及毒素基因调控的研究进展[J].微生物学报, 2023
- ^ 王伟刚,杨靖,牛亚楠,等.艰难类梭菌芽胞形成和萌发相关调控的研究进展[J].微生物学通报, 2021.DOI:10.13344/j.microbiol.china.200596.
- ^ 存档副本. [2024-01-11]. (原始内容存档于2024-01-11).
- ^ https://terms.naer.edu.tw/detail/9f76f51765c485b096e0923dea39b5b6/?seq=2
- ^ 存档副本. [2024-01-11]. (原始内容存档于2024-01-11).
- ^ 存档副本 (PDF). [2024-01-11]. (原始内容存档 (PDF)于2024-01-11).
- ^ 微生物免疫學-Clostridium difficile(困難梭菌). [2013-01-29]. (原始内容存档于2019-12-03) (中文(繁体)).
- ^ Ryan KJ, Ray CG (editors). Sherris Medical Microbiology 4th. McGraw Hill. 2004: 322–4. ISBN 0-8385-8529-9.
- ^ 存档副本. [2024-01-11]. (原始内容存档于2024-01-23).
- ^ Di Bella S, Ascenzi P, Siarakas S, Petrosillo N, di Masi A. Clostridium difficile Toxins A and B: Insights into Pathogenic Properties and Extraintestinal Effects. Toxins (Basel). 2016 May 3;8(5):134. doi: 10.3390/toxins8050134. PMID 27153087; PMCID: PMC4885049.
- ^ Carter, Glen P.; Rood, Julian I.; Lyras, Dena. The role of toxin A and toxin B in the virulence of Clostridium difficile. Trends in Microbiology. 2012-01-01, 20 (1): 21–29 [2019-10-24]. ISSN 0966-842X. PMID 22154163. doi:10.1016/j.tim.2011.11.003. (原始内容存档于2013-10-12) (英语).
- ^ Hui, Wenjia; Li, Ting; Liu, Weidong; Zhou, Chunyan; Gao, Feng. Fecal microbiota transplantation for treatment of recurrent C. difficile infection: An updated randomized controlled trial meta-analysis. PLoS ONE. 2019-01-23, 14 (1) [2019-10-24]. ISSN 1932-6203. PMC 6343888 . PMID 30673716. doi:10.1371/journal.pone.0210016. (原始内容存档于2021-05-26).