甲烷
甲烷(英语:Methane),是结构最简单的烃类,化学式为CH
4,由一个碳原子以及四个氢原子组成。它是天然气的主要成分。甲烷在地球上有很高的相对丰度,使之成为很有发展潜力的一种燃料,但在标准状态下收集以及存储气态的甲烷是一个十分有挑战性的课题。
| 甲烷 | |||
|---|---|---|---|
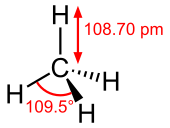
| |||
| |||
| IUPAC名 Methane[1][2] | |||
| 系统名 Carbane 碳烷(从不推荐[1]) | |||
| 别名 |
| ||
| 识别 | |||
| CAS号 | 74-82-8 | ||
| PubChem | 297 | ||
| ChemSpider | 291 | ||
| SMILES |
| ||
| Beilstein | 1718732 | ||
| Gmelin | 59 | ||
| 3DMet | B01450 | ||
| UN编号 | 1971 | ||
| EINECS | 200-812-7 | ||
| ChEBI | 16183 | ||
| RTECS | PA1490000 | ||
| KEGG | C01438 | ||
| MeSH | Methane | ||
| 性质 | |||
| 化学式 | CH4 | ||
| 摩尔质量 | 16.04 g·mol−1 | ||
| 外观 | 无色气体 | ||
| 气味 | 无味 | ||
| 密度 | 0.697 g/L(气态,27 °C,1.8 atm) 0.716 g/L(气态,0 °C,1 atm) 0.42262 g cm−3 (液态,-186 °C)[3] | ||
| 熔点 | -182 °C(90.7 K) | ||
| 沸点 | -161 °C(111.66 K) | ||
| 溶解性(水) | 22.7 mg L−1 | ||
| 溶解性 | 溶于乙醇、乙醚、苯、甲苯、甲醇、丙酮 | ||
| log P | 1.09 | ||
| kH | 14 nmol Pa−1 kg−1 | ||
| 结构 | |||
| 分子构型 | 正四面体 | ||
| 偶极矩 | 0 D | ||
| 热力学 | |||
| ΔfHm⦵298K | −74.87 kJ mol−1 | ||
| ΔcHm⦵ | −891.1 to −890.3 kJ mol−1 | ||
| S⦵298K | 186.25 J K−1 mol−1 | ||
| 热容 | 35.69 J K−1 mol−1 | ||
| 危险性 | |||
| 警示术语 | R:R12 | ||
| 安全术语 | S:S2, S16, S33 | ||
| 欧盟分类 | |||
GHS危险性符号
| |||
| GHS提示词 | DANGER | ||
| H-术语 | H220 | ||
| P-术语 | P210 | ||
| NFPA 704 | |||
| 爆炸极限 | 4.4–17% | ||
| 相关物质 | |||
| 相关化合物 | |||
| 相关物质 | |||
| 相关烷烃、氢化物 | 乙烷、丙烷、甲硅烷、甲锗烷、甲锡烷、铅烷 | ||
| 相关化学品 | 甲醇、一氯甲烷、甲酸、甲醛 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
在自然状态下,甲烷可以在地底下或者海底找到,大气中也含有甲烷,这些甲烷称为大气甲烷[5]。在原始大气中,甲烷是主要成分之一。自1750年以来,地球大气中的甲烷浓度增加了约150%,造成的全球暖化效应以及全球所有温室气体的20%(不包括水蒸气)[6]。在太空中,不少星体的表面和大气中也有甲烷。
甲烷的结构是由一个碳和四个氢原子透过sp3杂化的方式化合而成,而且是所有烃类物质中,含碳量最小,且含氢量最大的碳氢化合物,因此甲烷分子的分子结构是一个正四面体的结构,碳大约位于该正四面体的几何中心,氢位于其四个顶点,且四个碳氢键的键的键角相等、键长等长。标准状态下的甲烷是一种无色无味的气体[7]。一些有机物在缺氧情况下分解时所产生的沼气主要成分就是甲烷。
历史
编辑1776年11月,意大利物理学家亚历山大·伏打(Alessandro Volta, 1745年2月18日-1827年3月5日)根据本杰明·富兰克林(Benjamin Franklin 1706年1月17日-1790年4月17日)关于“可燃空气”的论文,在瑞士的马焦雷湖(Lago Maggiore)中发现了甲烷[8]。伏打在沼泽中收集冒出来的甲烷,直到1778年成功分离出纯的甲烷气体[9],他还利用电火花装置成功点燃甲烷气体确定了甲烷的可燃性[9]。
分子性质
编辑甲烷分子是一种正四面体分子,有四个等价的碳氢键。其分子结构是由碳跟氢的价轨道重叠所形成的分子轨道构成,最低能量的分子轨道为的2s轨道上的碳与同相组合的1s轨道上的四个氢原子重叠的结果,而能量稍微高一点的由三个分子轨道重叠的结果,即氢原子的一个s轨道电子和三个碳原子的p轨道电子重叠形成一个σ轨道,更精确的说法是,发生杂化而形成了sp3杂化轨道。这种化合方式与实际观测到的甲烷光谱吻合。
常温常压下的甲烷是一种无色无味的气体[7]。家用天然气的特殊味道,是为了安全而添加的人工气味,通常是使用甲硫醇或乙硫醇。在一大气压力的环境中,甲烷的沸点是−161 °C[10]。甲烷是一种十分容易闪燃甚至会爆炸的气体,只要空气中甲烷含量在4.4-17%的范围内就很容易起火或爆炸。
目前已知有九种不同的固态甲烷晶体结构[11]。若在常压下将甲烷降至甲烷的冰点会形成甲烷一(英语:methane I)的晶体结构,这种晶体结构属于立方晶系,空间群为Fm3m。由于氢原子的位置在甲烷一晶格中是不固定的,即甲烷分子可以自由转动。因此,它是一个可塑性晶体[12]。
甲烷是天然气的主要成分,约占了87%,液化的甲烷不会燃烧,除非在高压的环境中(通常是4~5大气压力)。
可能对健康造成的影响
编辑甲烷并非毒气;然而,其具有高度的易燃性,和空气混合时也可能造成爆炸。甲烷和氧化剂、卤素或部分含卤素之化合物接触会有极为猛烈的反应。甲烷同时也是一种窒息气体,在密闭空间内可能会取代氧气。若氧气被甲烷取代后含量低于19.5%时可能导致窒息。当有建筑物位于垃圾掩埋场附近时,甲烷可能会渗透入建筑物内部,让建物内的居民暴露在高含量的甲烷之中。某些建筑物在地下室设有特别的回复系统,会主动捕捉甲烷,并将之排出至建筑物外。
来源
编辑甲烷是天然气的最主要成分,是很重要的燃料;同时也是温室气体:其全球变暖潜能为21(即它的暖化能力比二氧化碳高二十一倍)。主要来源有:
制取
编辑- CH3COONa + NaOH → CH4↑ + Na2CO3
化学反应
编辑甲烷主要化学反应是:燃烧、蒸汽重整合成气、以及卤化反应。在一般情况下,甲烷的反应是很难控制。甲烷可以氧化成甲醇,但一般来说要完成这个化学反应时十分困难的,因为在一般情况下甲烷的氧化反应产物通常是二氧化碳与水,即使氧气不足也很难产生甲醇。但是若在酵素的协助下就能轻易地完成此氧化反应,例如甲烷单加氧酶,但产量无法达到工业生产的规模[14]。
反应性
编辑由于甲烷中碳原子与氢原子间的化学键为较稳定的σ键,化学性质比较稳定,因此甲烷能参与的反应较其他有机物少。
燃烧
编辑甲烷的燃烧热约为 55.5 MJ/kg [15]。燃烧时产生明亮的蓝色火焰。甲烷的燃烧是一个多步反应。下面的反应式是过程的一部分,与所述净结果是: CH4 + 2 O2 → CO2 + 2 H2O (ΔH = −891 k J/mol)
- CH4+ M* → CH3 + H + M
- CH4 + O2 → CH3 + H2O
- CH4 + HO2 → CH3 + 2 OH
- CH4 + OH → CH3 + H2O
- O2 + H → O + OH
- CH4 + O → CH3 + OH
- CH3 + O2 → CH2O + OH
- CH2O + O → CHO + OH
- CH2O + OH → CHO + H2O
- CH2O + H → CHO + H2
- CHO + O → CO + OH
- CHO + OH → CO + H2O
- CHO + H → CO + H2
- H2 + O → H + OH
- H2 + OH → H + H2O
- CO + OH → CO2 + H
- H + OH + M → H2O + M*
- H + H + M → H2 + M*
- H + O2 + M → HO2 + M*
加热分解
编辑在隔绝空气的条件下加热到将近1000℃,就开始分解;加热时间较长,到1500℃左右,分解接近完全。
当甲烷与氯在黑暗中混合时,两者不会产生化学反应,如果把混合物加热或以紫外光照射,以下反应(取代反应)会发生:[16]
- CH4 + Cl2 → CH3Cl + HCl
- CH3Cl + Cl2 → CH2Cl2 + HCl
- CH2Cl2 + Cl2 → CHCl3 + HCl
- CHCl3 + Cl2 → CCl4 + HCl
反应的机理属于自由基取代,有键引发、键增长、键中止三步骤。
反应的产物含有此四种氯化甲烷,由上至下四种产物名称分别为:一氯甲烷,二氯甲烷,三氯甲烷,四氯甲烷(四氯化碳),四者的比例视甲烷与氯的比例。 甲烷可与溴产生类似反应。甲烷与氟的反应十分猛烈,如果先用稀有气体稀释两者才在特定的仪器内进行反应,也可得出类似反应。甲烷与碘不会直接产生反应,可以用溴化碘等代替进行碘化。
参见
编辑参考文献
编辑- ^ 1.0 1.1 Front Matter. Nomenclature of Organic Chemistry : IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014: 3–4. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069-FP001.
Methane is a retained name (see P-12.3) that is preferred to the systematic name ‘carbane’, a name never recommended to replace methane, but used to derive the names ‘carbene’ and ‘carbyne’ for the radicals H2C2• and HC3•, respectively.
- ^ methane (CHEBI:16183). Chemical Entities of Biological Interest. UK: European Bioinformatics Institute. 2009-10-17 [2011-10-10]. (原始内容存档于2018-12-26).
- ^ Gas Encyclopedia. [2013-11-07]. (原始内容存档于2018-12-26).
- ^ NOAA Office of Response and Restoration, US GOV. METHANE. noaa.gov. [2016-01-28]. (原始内容存档于2019-01-09).
- ^ Khalil, M. A. K. Non-Co2 Greenhouse Gases in the Atmosphere. Annual Review of Energy and the Environment. 1999, 24: 645. doi:10.1146/annurev.energy.24.1.645.
- ^ Technical summary. Climate Change 2001. United Nations Environment Programme. [2016-01-28]. (原始内容存档于2011-06-04).
- ^ 7.0 7.1 Hensher, David A. and Button, Kenneth J. Handbook of transport and the environment. Emerald Group Publishing. 2003: 168 [2014-09-14]. ISBN 0-08-044103-3. (原始内容存档于2014-09-21).
- ^ Volta, Alessandro (1777) Lettere del Signor Don Alessandro Volta … Sull' Aria Inflammabile Nativa delle Paludi [Letters of Signor Don Alessandro Volta … on the flammable native air of the marshes], Milan, Italy: Giuseppe Marelli.
- ^ 9.0 9.1 Methane. BookRags. [2012-01-26]. (原始内容存档于2016-03-03).
- ^ Methane Phase change data (页面存档备份,存于互联网档案馆). NIST Chemistry Webbook.
- ^ Bini, R.; Pratesi, G. High-pressure infrared study of solid methane: Phase diagram up to 30 GPa. Physical Review B. 1997, 55 (22): 14800–14809. doi:10.1103/physrevb.55.14800.
- ^ Kristallgitter. paarpraxis-rheinmain.de. 2015-02-26 [2016-01-28]. (原始内容存档于2016-03-04).
- ^ Miller, G. Tyler (2007). Sustaining the Earth: An Integrated Approach. U.S.A.: Thomson Advantage Books, ISBN 978-0-534-49672-2, p. 160.
- ^ Baik, Mu-Hyun; Newcomb, Martin; Friesner, Richard A.; Lippard, Stephen J. Mechanistic Studies on the Hydroxylation of Methane by Methane Monooxygenase. Chemical Reviews. 2003, 103 (6): 2385–419. PMID 12797835. doi:10.1021/cr950244f.
- ^ Energy Content of some Combustibles (in MJ/kg) (页面存档备份,存于互联网档案馆). People.hofstra.edu. Retrieved on March 30, 2014.
- ^ March, Jerry. Advance Organic Chemistry: Reactions, Mechanisms and Structure. New York: McGraw-Hill Book Company. 1968: 533–534.


