T细胞受体
T细胞受体(T cell receptor, TCR)是T细胞表面的特异性受体[1],负责识别由主要组织相容性复合体(major histocompatibility complex,MHC)所呈递的抗原,它与B细胞受体不同,并不能识别游离的抗原。通常情况下,T细胞受体与抗原间拥有较低的亲和力,因而同一抗原可能被不同的T细胞受体所识别,某一受体也可能识别许多种抗原。
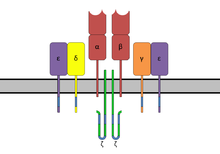 T细胞受体复合体包括α、β亚基,CD3和ζ亚基 | |||||||||
| 鉴定 | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| 标志 | ? | ||||||||
| Pfam | PF11628(旧版) | ||||||||
| InterPro | IPR021663 | ||||||||
| OPM家族 | 261 | ||||||||
| OPM蛋白 | 2hac | ||||||||
| |||||||||
| T细胞受体(α基因) | |
|---|---|
| 识别 | |
| 符号 | TRA@ |
| 替换符号 | TCRA |
| Entrez | 6955 |
| HUGO | 12027 |
| OMIM | 186880 |
| 其他资料 | |
| 基因座 | 14 q11.2 |
| T细胞受体(β基因) | |
|---|---|
| 识别 | |
| 符号 | TRB@ |
| 替换符号 | TCRB |
| Entrez | 6957 |
| HUGO | 12155 |
| OMIM | 186930 |
| 其他资料 | |
| 基因座 | 7 q34 |
T细胞受体是异源二聚体,由两个不同的亚基所构成。95%的T细胞的受体由α亚基和β亚基构成,另外5%的受体由γ亚基和δ亚基构成。这个比例会因为个体发育或是疾病而变化。
T细胞受体与MHC所呈递的多肽的特异性结合会引发一系列生化反应,并通过众多的辅助受体、酶和转录因子激活T细胞,促进其分裂与分化。
结构
编辑T细胞受体是一个固定在细胞膜上的异源二聚体,多数由高度易变的α亚基和β亚基通过二硫键连结构成。这一类T细胞被称为αβ T细胞。少数含有γ亚基和δ亚基被称为γδ T细胞[2]。T细胞受体会与恒定的CD3分子一起构成T细胞受体复合体。
每一个亚基都含有两个细胞外的结构域:可变区与恒定区。这些结构域属于免疫球蛋白超家族,由反向平行的β折叠所构成。恒定区靠近细胞膜,连接着跨膜区和胞内的末端,而可变区负责识别多肽/MHC复合体。每个亚基的可变区都包含三个高度易变的互补性决定区(complementarity determining regions, CDR)。最重要的CDR3负责直接与MHC所呈递的多肽结合。α亚基和β亚基的CDR1分别作用与多肽的N端和C端。CDR2被认为参与识别MHC。β亚基还有一个额外的CDR4,通常并不参与多肽/MHC复合体的识别,但与超抗原的作用有关。
多样性
编辑T细胞受体的抗原结合位极为多样化,产生这种多样性的机理与B细胞受体和抗体多样性的机理极为类似,主要源于免疫球蛋白基因的VDJ重组。编码免疫球蛋白的基因位点由许多基因片段构成,包括可变段(V)、连接段(J)以及之间可能存在的多样段(D)。α和γ亚基由VJ重组产生,β和δ亚基则由VDJ重组产生。不同基因片段之间的随机重组以及重组过程中随机插入的核苷酸极大地丰富了T细胞受体的多样性。
对抗原的识别
编辑每个T细胞都会在细胞表面表达大量单一种类的受体。在生理环境下,T细胞受体和与之对应的多肽/MHC复合体间有着很高的结合速率和分离速率。T细胞受体对于某一种或一些抗原有高度的特异性,但单一受体的亲和力较低,大约在微摩尔的水平[3]。另外,目标细胞表面有大量的MHC复合体,但与某一T细胞对应的复合体数量极低。尽管如此,T细胞对特异抗原的识别以及反应相当灵敏和高效[4]。这种高效源于T细胞受体在识别过程中寡聚化,在细胞表面形成微簇,提高了T细胞对抗原的亲合力(avidity)[5]。因此,能与T细胞受体多价结合的分子(比如CD3抗体)可以像MHC复合体一样高效地激活T细胞,虽然它们并不作用于受体的抗原结合区。通常被抗原激活过的T细胞的灵敏度高于未分化的T细胞。实验表明,较之激活后的辅助型T细胞和记忆T细胞,未分化的T细胞的活性更依赖高浓度的抗原以及各种辅助刺激因子[6]。据此,原始T细胞在分化过程中会经历亲合力成熟的过程,而T细胞受体的亲和力并不改变。
T细胞受体复合体
编辑T细胞受体复合体是一个跨膜的八聚体,由TCR二聚体和负责信号传递的CD3 δ/ε二聚体、CD3 γ/ε二聚体以及CD247 ζ/ζ或是ζ/η二聚体构成。各个二聚体通过电离的氨基酸残基间的相互作用联系在一起[7]。T细胞受体的胞内末端很短,极有可能并不参与信号的传递。整个复合体可以高效地将受体接受到的信号传递到细胞内。
协同受体
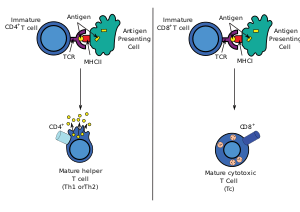
编辑T细胞受体与特异抗原的结合需要协同受体同时结合到MHC分子上加以强化。总共有两种不同的T细胞协同受体:
协同受体不仅提高了T细胞受体在功能上的特异性,而且延长了T细胞与抗原呈递细胞的作用时间,还是细胞内信号通路的一些分子(如Lck)的附着点。
T细胞激活
编辑T细胞受体的主要功能是在识别特异抗原后激活T细胞。T细胞激活的过程属于跨膜信号传递,由众多的分子和生化反应共同完成。细胞内信号传递最常见的方式是由激酶和磷酸酶所主导的蛋白磷酸化和去磷酸化。CD3和ζ亚基的胞内区域有许多免疫受体酪氨酸激活基序(immunoreceptor tyrosine-based activation motifs, ITAM)。在T细胞受体被激活后,这些序列中的酪氨酸被Src激酶家族磷酸化[8],从而实现了信号的跨膜传递。
早期的胞内信号传递由下列的激酶和磷酸酶共同完成:
- Lck:Src激酶家族,结合在CD4的胞内末端,负责ITAM的磷酸化
- Fyn:Src激酶家族,与Lck类似,负责CD3和ζ亚基上ITAM的磷酸化
- CD45:胞内末端是酪氨酸磷酸酶,负责Src激酶家族上抑制性酪氨酸的去磷酸化,从而激活Src激酶
- ZAP70:Syk激酶家族,通过SH2结构域结合在磷酸化的ITAM上,负责LAT的磷酸化
LAT是一种衔接蛋白,磷酸化的LAT可以结合C型磷脂酶并促进其活化。通过数条不同的信号通路,许多与细胞分裂分化的转录因子被激活,从而调控一系列相关基因的表达。[9]
参考文献
编辑- ^ Thomas J. Kindt; Richard A. Goldsby; Barbara Anne Osborne; Janis Kuby. Kuby immunology. Macmillan. 2007: 223– [28 November 2010]. ISBN 978-1-4292-0211-4. (原始内容存档于2013-11-26).
- ^ Janeway CA Jr, Travers P, Walport M; et al. Immunobiology: The Immune System in Health and Disease. 5th edition. Glossary: Garland Science. 2001 [2014-01-16]. (原始内容存档于2019-02-18).
- ^ Donermeyer DL, Weber KS, Kranz DM, Allen PM. The study of high-affinity TCRs reveals duality in T cell recognition of antigen: specificity and degeneracy. J. Immunol. November 2006, 177 (10): 6911–9. PMID 17082606.
- ^ Edwards LJ, Evavold BD. T cell recognition of weak ligands: roles of signaling, receptor number, and affinity.. Immunol Res. 2011, 50 (1): 39–48. PMC 3107861 . PMID 21365321. doi:10.1007/s12026-011-8204-3.
- ^ Schamel WW, Alarcón B. Organization of the resting TCR in nanoscale oligomers. Immunol. Rev. January 2013, 251 (1): 13–20. PMID 23278737. doi:10.1111/imr.12019.
- ^ von Essen MR, Kongsbak M, Geisler C. Mechanisms behind functional avidity maturation in T cells. Clin. Dev. Immunol. 2012, 2012: 163453. PMC 3351025 . PMID 22611418. doi:10.1155/2012/163453.
- ^ Call ME, Pyrdol J, Wiedmann M, Wucherpfennig KW. The organizing principle in the formation of the T cell receptor-CD3 complex.. Cell. December 2002, 111 (7): 967–79. PMID 12507424.
- ^ Abram CL, Lowell CA. The expanding role for ITAM-based signaling pathways in immune cells. Sci. STKE. March 2007, 2007 (377): re2. PMID 17356173. doi:10.1126/stke.3772007re2.
- ^ Parham, Peter. The Immune System. New York: Garland Science. 2009: 22–223. ISBN 978-0-8153-4146-8.