硫代硫酸钠
硫代硫酸钠,又称大苏打、海波,是一种无机化合物,化学式为Na2S2O3。通常为白色或无色的五水合物(Na2S2O3·5H2O)。它是一种易风化的物质,易溶于水。[2]
| 硫代硫酸钠 | |
|---|---|

| |
| |

| |
| IUPAC名 Sodium thiosulfate | |
| 别名 | 次亚硫酸钠 大苏打 海波 |
| 识别 | |
| CAS号 | 7772-98-7 10102-17-7 |
| PubChem | 24477 |
| ChemSpider | 22885 |
| SMILES |
|
| InChI |
|
| InChIKey | AKHNMLFCWUSKQB-NUQVWONBAM |
| ChEBI | 132112 |
| RTECS | XN6476000 |
| 性质 | |
| 化学式 | Na 2S 2O 3 |
| 摩尔质量 | 无水:158.11 g/mol 五水:248.18 g·mol⁻¹ |
| 外观 | 白色晶体 |
| 气味 | 无味 |
| 密度 | 1.667 g/cm3 |
| 熔点 | 48.3 °C(321 K) |
| 沸点 | 100 °C(373 K) |
| 溶解性(水) | 70.1 g/100 mL (20 °C)[1] 231 g/100 mL (100 °C) |
| 溶解性 | 难溶于醇 |
| 折光度n D |
1.489 |
| 结构 | |
| 晶体结构 | 单斜 |
| 危险性 | |
GHS危险性符号
| |
| GHS提示词 | Warning |
| H-术语 | H315, H319, H335 |
| P-术语 | P261, P264, P271, P280, P302+352, P304+340, P305+351+338, P312, P321, P332+313, P337+313, P362, P403+233, P405 |
| NFPA 704 | |
| 相关物质 | |
| 其他阳离子 | 硫代硫酸 硫代硫酸锂 硫代硫酸钾 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
硫代硫酸钠可用于金矿开采、水处理、分析化学,银基摄影胶片和相纸的开发,以及药物。硫代硫酸钠的医药用途包括治疗氰化物中毒和花斑癣。[3]它在世界卫生组织基本药物标准清单中。[4][5]
用途
编辑医药用途
编辑硫代硫酸钠可用于治疗氰化物中毒。[3]硫代硫酸钠也用于治疗皮癣菌病和花斑癣,[3][6]以及血液透析[7]和化疗的一些副作用。[8]它临床用于治疗皮肤搔痒症、性荨麻疹、药疹、铊中毒和砷中毒等,以静脉注射的方式治疗。[9]
照相冲印
编辑溴化银等卤化银作为照相乳剂的主要成分,经硫代硫酸盐水溶液处理后会溶解。这种作为照相定影剂的应用是由约翰·赫歇尔发现的。它常用于胶片和相纸冲洗。硫代硫酸钠定影剂通常被称为“海波”,源自于最初的化学名称“次亚硫酸钠”(Sodium hyposulfite)。[10]在此应用中,硫代硫酸铵通常优于硫代硫酸钠。[2]
自来水脱氯
编辑硫代硫酸钠可用于对自来水进行脱氯,包括降低水族馆、游泳池和水疗中心使用水的氯含量,以及水处理厂内用于在排入河流之前处理沉淀的反冲洗水。[2]此还原反应类似于碘还原反应。
在漂白剂物质的pH测试中,硫代硫酸钠可以中和漂白剂的脱色作用,并允许使用液体指示剂测试漂白剂溶液的pH。相关反应类似碘反应:硫代硫酸盐还原次氯酸盐(漂白剂中的活性成分),在此过程中其被氧化成硫酸盐。完整反应:
- 4 NaClO + Na
2S
2O
3 + 2 NaOH → 4 NaCl + 2 Na
2SO
4 + H
2O
类似地,硫代硫酸钠可与溴反应,并从溶液中除去游离溴。硫代硫酸钠溶液通常在化学实验室中用作处理溴的预防措施,以及安全处理溴、碘或其他强氧化剂。
结构
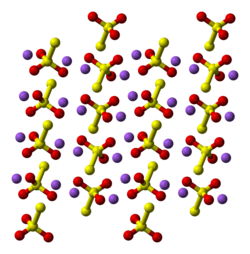
编辑五水合物有两种同质异形体,无水盐存在多种同质异形体。[2]在固态中,硫代硫酸根阴离子呈四面体状,理论上是用硫酸根阴离子中的硫原子取代其中一个氧原子产生的。S-S距离表示单键,这表示末端的硫带有明显的负电荷,而S-O相互作用具有更多的双键特性。
生产
编辑在工业上,硫代硫酸钠主要是由硫化钠或含硫染料制造的液体废物生产。[11]
在实验室中,硫代硫酸钠可以由亚硫酸钠或沸腾的氢氧化钠溶液和硫反应而成:[12][13]
- 6 NaOH + 4 S → 2 Na
2S + Na
2S
2O
3 + 3 H
2O
反应
编辑在444 °C以上,硫代硫酸钠分解成硫酸钠和多硫化钠:[14]
- 4 Na
2S
2O
3 → 3 Na
2SO
4 + Na
2S
5
硫代硫酸盐与酸反应后会发生分解。初始质子化发生在硫上。在-78℃下的二乙醚中进行质子化反应,可得到H
2S
2O
3(硫代硫酸)。它是稍强的酸,第一次和第二次电离的 pKa 分别为0.6和1.7。
在标准情况下,对硫代硫酸钠加酸会分解成硫、二氧化硫和水:[11]
- Na
2S
2O
3 + 2 HCl → 2 NaCl + S + SO
2 + H
2O
配位化学
编辑硫代硫酸盐是软金属离子的有效配体。典型的配合物是[Pd(S
2O
3)
2(en)]2−,具有一对S键结的硫代硫酸盐配体。硫代硫酸钠和硫代硫酸铵已被提议作为氰化物提取金的替代浸出剂。[15][2]这种方法的优点是硫代硫酸盐的毒性远低于氰化物,且氰化法难处理的矿石类型(例如碳质或卡林型矿石)可以用硫代硫酸盐浸出。这种替代工艺的问题包括硫代硫酸盐的消耗量大,以及缺乏合适的回收技术,因为[Au(S
2O
3)
2]3−不会吸附在活性炭上,这是金氰化中用于从矿浆中分离金错合物的标准技术。
碘量法
编辑在分析化学中,硫代硫酸根阴离子会和化学计量的碘在水溶液中反应,碘被还原成碘离子,而硫代硫酸根被氧化成连四硫酸根:[16][17]
- 2 S
2O2−
3 + I
2 → S
4O2−
6 + 2 I−
由于此反应的定量性质,以及Na
2S
2O
3 · 5H2O具有良好的保质期,因此它被用作碘量法中的滴定剂。Na
2S
2O
3 · 5H2O也是碘钟反应的组成部分。
这种特殊用途可以透过温克勒滴定法的一系列反应来测量水中的氧含量。它也用于以体积估算溶液中某些化合物(如过氧化氢)的浓度以及估算商业漂白粉或水中的氯含量。
和铝离子的反应
编辑硫代硫酸钠可用于分析化学,[18] 当与含有铝离子的样品一起加热时,会产生白色沉淀:
- 2 Al3+ + 3 S
2O2−
3 + 3 H
2O → 3 SO
2 + 3 S + 2 Al(OH)
3
有机化学
编辑对硫代硫酸钠烷基化会产生S-烷基硫代硫酸钠(例如苄基硫代硫酸钠),它们也被称为Bunte盐。[19]烷基硫代硫酸钠会水解,并产生硫醇,例如巯基乙酸的制备:
- ClCH
2CO
2H + Na
2S
2O
3 → Na[O
3S
2CH
2CO
2H] + NaCl - Na[O
3S
2CH
2CO
2H] + H
2O → HSCH
2CO
2H + NaHSO
4
参考资料
编辑- ^ Record in the GESTIS Substance Database from the IFA
- ^ 2.0 2.1 2.2 2.3 2.4 Sulfites, Thiosulfates, and Dithionites, Ullmann's Encyclopedia of Industrial Chemistry, Weinheim: Wiley-VCH, 2005, doi:10.1002/14356007.a25_477
- ^ 3.0 3.1 3.2 Stuart MC, Kouimtzi M, Hill SR (编). WHO Model Formulary 2008. World Health Organization. 2009: 66. ISBN 978-92-4-154765-9. hdl:10665/44053 .
- ^ World Health Organization model list of essential medicines: 21st list 2019. Geneva: World Health Organization. 2019. hdl:10665/325771 . WHO/MVP/EMP/IAU/2019.06. License: CC BY-NC-SA 3.0 IGO.
- ^ World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. 2021. hdl:10665/345533 . WHO/MHP/HPS/EML/2021.02.
- ^ Sunenshine PJ, Schwartz RA, Janniger CK. Tinea versicolor. Int. J. Dermatol. 2002, 37 (9): 648–55. PMID 9762812. S2CID 75657768. doi:10.1046/j.1365-4362.1998.00441.x.
- ^ Auriemma M, Carbone A, Di Liberato L, et al. Treatment of Cutaneous Calciphylaxis with Sodium Thiosulfate: Two Case Reports and a Review of the Literature. Am. J. Clin. Dermatol. 2011, 12 (5): 339–46. PMID 21834598. S2CID 28366905. doi:10.2165/11587060-000000000-00000.
- ^ Dickey DT, Wu YJ, Muldoon LL, et al. Protection against Cisplatin-Induced Toxicities by N-Acetylcysteine and Sodium Thiosulfate as Assessed at the Molecular, Cellular, and in Vivo Levels. J. Pharmacol. Exp. Ther. 2005, 314 (3): 1052–8. PMID 15951398. S2CID 11381393. doi:10.1124/jpet.105.087601.
- ^ 国家网路医药, KingNet. 學名藥SODIUM THIOSULFATE 皮膚/表皮系統 皮膚疾患治療藥品 毒物治療藥品 重金屬中毒症 | 藥典. KingNet 国家网路医药. [2021-05-27]. (原始内容存档于2021-05-27) (中文).
- ^ Gibson CR. The Romance of Modern Photography, Its Discovery & Its Achievements. Seeley & Co. 1908: 37.
hyposulphite-of-soda herschel fixer hypo.
- ^ 11.0 11.1 Holleman AF, Wiberg E, Wiberg N. Inorganic Chemistry. San Diego: Academic Press. 2001. ISBN 978-0-12-352651-9.
- ^ Gordin HM. Elementary Chemistry. 1. Inorganic Chemistry. Chicago: Medico-Dental Publishing Co. 1913: 162 & 287–288 [2021-07-30]. (原始内容存档于2024-10-01).
- ^ Greenwood, Norman Neill; Earnshaw, Alan. Chemistry of the elements. 2016. ISBN 978-0-7506-3365-9. OCLC 1040112384 (英语).
- ^ Benda, Heike von. Zur Polymorphie des Na2S2O3 / On Polymorphism of Na2S2O3. Zeitschrift für Naturforschung B (Walter de Gruyter GmbH). 1979-07-01, 34 (7): 957–968. ISSN 1865-7117. doi:10.1515/znb-1979-0716.
- ^ Aylmore MG, Muir DM. Thiosulfate Leaching of Gold - a Review. Minerals Engineering. 2001, 14 (2): 135–174. doi:10.1016/s0892-6875(00)00172-2.
- ^ Holleman, Arnold Frederik; Wiberg, Egon, Wiberg, Nils , 编, Inorganic Chemistry, 由Eagleson, Mary; Brewer, William翻译, San Diego/Berlin: Academic Press/De Gruyter: 594, 2001, ISBN 0-12-352651-5
- ^ Holleman, Arnold Frederik; Wiberg, Egon, Wiberg, Nils , 编, Inorganic Chemistry, 由Eagleson, Mary; Brewer, William翻译, San Diego/Berlin: Academic Press/De Gruyter: 670, 2001, ISBN 0-12-352651-5
- ^ Dulski TR. Ch. 8: Separation by Precypitation. A Manual for the Chemical Analysis of Metals. West Conshohocken, PA: ASTM. 1996: 99 [2021-07-30]. ISBN 9781601194350. OCLC 180851384. (原始内容存档于2021-07-30).
- ^ Alonso ME, Aragona H. Sulfide Synthesis in Preparation of Unsymmetrical Dialkyl Disulfides: Sec-butyl Isopropyl Disulfide. Org. Synth. 1978, 58: 147. doi:10.15227/orgsyn.058.0147.
