磷酸盐
磷酸盐(phosphate,符号:PO3−
4),是磷酸的盐,在无机化学、生物化学及生物地质化学上是很重要的物质。
| 磷酸盐 | |||
|---|---|---|---|
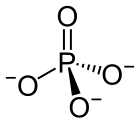
| |||
| |||
| 系统名 Phosphate[1] | |||
| 识别 | |||
| CAS号 | 14265-44-2 | ||
| PubChem | 1061 | ||
| ChemSpider | 1032 | ||
| SMILES |
| ||
| Beilstein | 3903772 | ||
| Gmelin | 1997 | ||
| ChEBI | 18367 | ||
| MeSH | Phosphates | ||
| 性质 | |||
| 化学式 | PO3− 4 | ||
| 摩尔质量 | 94.9714 g·mol⁻¹ | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
化学特性
编辑磷酸盐离子是一个多原子的离子,其实验式是PO43−,而分子量是94.97。它包含一个磷原子,并由四个氧原子所包围,形成一个正四面体。磷酸盐离子带有-3的形式电荷,且是磷酸氢盐离子(HPO42−)的共轭碱;磷酸氢盐离子则是磷酸二氢盐离子(H2PO4−)的共轭碱;而磷酸二氢盐离子又是磷酸(H3PO4)的共轭碱。它是一个超价分子(磷原子在其电子层有著10个电子)。如果磷酸盐作为一种有机磷化合物就被称为磷酸酯,其化学式为OP(OR)3。
除了一些碱金属外,大部份磷酸盐,在标准状态下,都是不可溶于水的。
在稀释的水溶液中,磷酸盐以四种形式存在。在强碱环境下,磷酸盐离子(PO43−)会较多;而在弱碱的环境下,磷酸氢盐离子(HPO42−)则较多。在弱酸的环境下,磷酸二氢盐离子(H2PO4−)较为普遍;而在强酸的环境下,则水溶的磷酸(H3PO4)是主要存在的形式。更精确的就是以下三种平衡反应:
在25℃的环境下有以各种不同的酸度系数(mol/L):
若在强碱的pH值下(pH=13),可以发现:
可见只有磷酸盐(PO43−)及磷酸氢盐(HPO42−)是主要的成份。
若在中和的pH值下(例如原生质,pH=7.0),可以发现:
所以只有磷酸二氢盐(H2PO4−)及磷酸氢盐(HPO42−)离子是主要成份(当中62%是H2PO4−,38%是HPO42−)。需要留意的是在细胞外体液(其pH约为7.4),这个比例会倒转(61%是HPO42−,39%是H2PO4−)。
若在强酸的pH值下(pH=1),可以发现:
可见H3PO4,相较于H2PO4−是最多的。实际上HPO42−及PO43−会接近消失。
磷酸盐可以形成聚合离子的二磷酸盐(亦即焦磷酸盐,P2O74−)、三磷酸盐(P3O105−)等。多种的偏磷酸盐离子都有著一个实验式的PO3−,且是在普遍在多种化合物。
磷酸盐矿产可以包含大量自然产生的铀。若吸收了这些土壤改良剂可以引致农作物含有铀成份。
生理特性
编辑磷酸盐在人体与组织结构、代谢、调节有关,是重要生理生化物质。摄取过多磷酸盐且血中磷酸盐过高,则与心血管疾病、肾脏病有关[3]。
出现
编辑磷酸盐是元素磷自然产生的形态,在多种磷酸盐矿物中可以找到。元素的磷或是磷化物是很难发现的(只有极少量在陨石中可以找到)。在矿物学及地质学,磷酸盐是指含有磷酸盐离子的石或矿石。
在北美洲最大型的磷矿粉矿床位于美国的佛罗里达州中部、爱德荷州的索达斯普陵、北卡罗莱那州沿岸区域。而其次的是位于蒙大拿州、田纳西州、乔治亚州及南卡罗莱那州近查尔斯顿。瑙鲁这个细少的岛国就曾经是有著大量高质素的磷酸盐矿产,但现时已被大量挖掘。磷矿粉亦可以在纳弗沙岛、摩洛哥、突尼西亚、以色列、多哥及约旦找到,这些地方亦有大量的磷酸盐矿业。
在生物中,磷是以溶液中游离的磷酸盐离子的形态出现,称为“无机磷酸盐”,这是要与其他在磷酸酯中的磷酸盐作出区别的。无机磷酸盐是会以Pi来表示,它可以是由焦磷酸盐(以PPi来表示)水解而得:
但是,磷酸盐最普遍是以一磷酸腺苷(AMP)、二磷酸腺苷(ADP)、三磷酸腺苷(ATP)、脱氧核糖核酸(DNA)及核糖核酸(RNA)的形式出现,且可以经由水解ADP或ATP而被释放出来。对于其他的二磷或三磷核苷亦有相似的反应。在ADP及ATP,或其他二磷及三磷核苷中的磷酸酐键,包含著大量的能量,所以它们在生物中有著重要的地位。它们一般会被称为高能磷酸磷,就像在肌肉组织中的磷酸肌酸一样。一些如膦的化合物在有机化学上亦会被使用,但它却似乎没有自然的相应物。
由于磷酸盐对生物的重要性,所以在生态学上,它是高度被采集。因此,它在环境中往往是限量试剂,而它的可得性则决定生物成长的速度。将大量的磷酸盐加入缺乏磷酸盐的环境或微生物环境中,会对生态有著重大的影响。例如,某一种生物的暴涨会使其他生物死亡。另外耗氧的种群也会消亡(参见富营养化)。在污染的问题下,磷酸盐是总溶解固体量(一种主要的水质指标)的主要成份。
用途
编辑磷酸盐一般会用在清洁剂中作为软水剂,但是因为磷酸盐的排放会影响藻类的繁荣衰退,所以在某些地区磷酸盐清洁剂是受到管制的。
在农业上,磷酸盐是植物的三种主要养份之一,且是肥料的主要成份。磷矿粉是从沉积岩的磷层中开采。以前它在开采后不用加工便可使用,但现时未加工的磷酸盐只会用在有机耕种上。一般它都是会化学加工制成过磷酸石灰、重过磷酸钙或磷酸二氢铵,它们的浓度都较磷酸盐高,且较易溶于水,所以植物可以较快吸收。
肥料级数一般有三个数字:第一个是指氮的数量,第二个是指磷酸盐的数量(以P2O5作基准),而第三个是指碱水(以K2O作基准)。所以一个10-10-10的肥料就每种成份各有10%,而其他的则是填充物。
参见
编辑参考文献
编辑- ^ Phosphates – PubChem Public Chemical Database. The PubChem Project. USA: National Center of Biotechnology Information. [2022-10-21]. (原始内容存档于2013-05-12).
- ^ Campbell, Neil A.; Reece, Jane B. Biology Seventh Edition. San Francisco, California: Benjamin Cummings. 2005: 65. ISBN 0-8053-7266-4.
- ^ Ritz, Eberhard; Hahn, Kai; Ketteler, Markus; Kuhlmann, Martin K.; Mann, Johannes. Phosphate additives in food--a health risk. Deutsches Ärzteblatt International. January 2012, 109 (4): 49–55. ISSN 1866-0452. PMC 3278747 . PMID 22334826. doi:10.3238/arztebl.2012.0049.
- ^ On-line Objective Analyses and Statistics (HTML/ASCII). World Ocean Atlas 2001. National Oceanographic Data Center, National Oceanographic and Atmospheric Administration. 2003年 [2006年12月6日]. (原始内容存档于2006年12月12日).
延伸阅读
编辑- Schmittner Karl-Erich; Giresse Pierre. Micro-environmental controls on biomineralization: superficial processes of apatite and calcite precipitation in Quaternary soils. Sedimentology (Roussillon, France). 1999, 46 (3): 463–476.

