动脉粥样硬化
动脉粥样硬化(英语:atherosclerosis)或粥样硬化,是动脉内膜因多种原因损伤后,内膜下积聚脂质、复合糖类并引发出血、血栓形成、纤维组织增生,使动脉管壁增厚、管腔缩小、血流受阻、管壁变硬和弹性减退的现象[7][8]。
| 动脉粥样硬化 Atherosclerosis | |
|---|---|
| 又称 | Arteriosclerotic vascular disease (ASVD) |
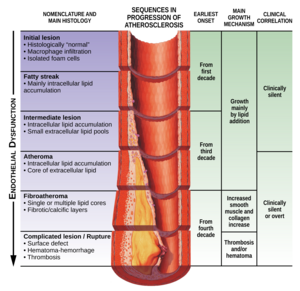 | |
| 动脉粥样硬化的病程 (血管狭窄化的放大图) | |
| 症状 | 无[1] |
| 并发症 | 冠状动脉疾病、中风、周边动脉阻塞、肾功能衰竭[1] |
| 起病年龄 | 青年 (并且随着年纪增加而恶化)[2] |
| 类型 | 动脉硬化性心血管疾病[*]、动脉硬化、疾病 |
| 病因 | 未知[1] |
| 风险因素 | 高血压、糖尿病、吸烟、肥胖症、家族史、不健康的饮食[3] |
| 预防 | 健康饮食、规律运动、不抽烟、维持正常体重[4] |
| 药物 | Statin、抗高血压药、阿司匹林[5] |
| 患病率 | ~100% (高于65岁)[6] |
| 分类和外部资源 | |
| 医学专科 | 心脏病学、血管学 |
| ICD-9-CM | 440 |
| DiseasesDB | 1039 |
| MedlinePlus | 000171 |
| eMedicine | 1950759 |
粥样斑块(atheromatous plaque)或粥瘤[9](atheroma)则是动脉粥样硬化的典型病变,结构由中央含脂肪和钙的无定形粥样脂肪核(fatty core)及外覆的纤维帽(fibrous cap)组成[10]。在显微镜下,动脉内膜呈现黄色粥样改变,引而得名。粥样斑块除脂质和钙质沉着外,另含巨噬细胞、T淋巴细胞、细胞外基质以及坏死碎片聚集,进而导致动脉壁增厚,是心血管疾病的主要病因。
动脉粥样硬化的早期通常没有症状[1],严重时视其影响的动脉所在,可能造成冠状动脉疾病、中风、周边动脉疾病以及肾功能衰竭[1]。一般而言,动脉粥样硬化的相关症状在中年之后才会出现[3]。
目前造成动脉粥样硬化的原因尚不明朗[1]。相关的风险因子包括血中胆固醇异常、高血压、糖尿病、吸烟、肥胖、动脉粥样硬化的家族史、以及不健康的饮食习惯[3]。血管壁的斑块由脂肪、胆固醇、钙、血栓、结缔组织、以及其他血中物质组成。斑块使得血管变得狭窄,含氧血的运送也因此被干扰[8]。动脉粥样硬化的诊断常包括理学检查、心电图、心脏压力测试等等 [11]。
预防动脉粥样硬化的方式一般包括健康饮食、运动、戒烟、以及维持正常体重[4]、用以降低血中胆固醇的他汀类药物、抗高血压药,或是阿司匹林与抗凝血剂都常用来治疗动脉粥样硬化。除了药物之外,经皮冠状动脉介入治疗、冠状动脉绕道手术、以及颈动脉内膜切除手术等手术也可以用来治疗动脉粥样硬化[5]。
动脉粥样硬化这个疾病最早在1575年就有记载,但疾病本身的历史远久于此,在超过5000年前的考古证据中就已经有动脉粥样硬化的踪迹[12]。动脉粥样硬化一般在年轻时便已经发生,然后随着年龄而恶化[2],大多数的老年人(65岁以上)都患有不同程度的动脉粥样硬化[6]。动脉粥样硬化是发达国家排名第一的致死与致残疾病[13]。
病理
编辑在过去很长时间里动脉硬化始终是医学和生物化学研究的重点。其原因是因为它的普及性。许多人有动脉硬化,但是这个状态可以数年、数十年在人体内存在,却不显示出任何病态,然后它会突然以局部缺血、心绞痛、心肌梗死、中风或心力衰竭等致命病爆发。在发展国家中动脉硬化后果是最常见的死因。[14]
动脉硬化的特征是动脉的慢性退化及动脉壁的逐渐变化。由于结缔组织的增长、细胞内外胆固醇、脂肪酸以及碳酸钙的沉积、胶原蛋白和蛋白聚糖的聚集动脉壁变硬变厚,动脉变细,整个动脉失去弹性。[15]
当胆固醇等物质堆积到了足够程度时,血管的内皮细胞会诱导单核细胞分化为巨噬细胞。巨噬细胞会吞噬血管壁之间的脂肪并使它们堆积于细胞内,脂肪使细胞成为泡沫细胞。[16]
除主动脉外,常累及心脏的冠状动脉和脑、肾动脉,可以引起动脉粥样斑块破裂、血栓形成,管腔狭窄至闭塞,从而使有关器官的血液供应发生障碍。
由于动脉硬化过程非常复杂,参加的细胞和组织(上皮细胞、平滑肌、单核细胞、巨噬细胞、血小板)、分子(脂蛋白、生长激素、胆固醇、脂肪、胶原蛋白和细胞因子等)多样,其中关系错综,因此至今为止在医学上没有良好的可以预言动脉硬化的模型和技术。
致病风险因素
编辑通过众多病史学和临床研究至少可以总结出一定的、有利于动脉硬化形成的因素。
后天可变的
编辑- 糖尿病[17]
- 血脂异常[17]
- 吸烟[17]:吸烟可破坏血管壁,诱导平滑肌细胞(SMC)增生;
- 反式脂肪[17]
- 腹部肥胖[17]
- 西方饮食[17]
- 胰岛素抵抗[17]
- 高血压[17]:高血压病人易发生,并且早而严重,好发于血管分叉、弯曲处;
后天不可变的
编辑几率偏低未被完全确认
编辑- 遗传因素:冠心病具有家族聚集现象,约200种基因可能对脂质的摄取、代谢、排泄产生影响。
- 其他:肥胖症、性别(男性)、高龄、病毒感染、饮食结构(比如高热量和高脂肪的食物;如肉类或油炸食物)被确定为动脉硬化的可能因素。
- 南亚后裔[18][19]
- 血栓形成体质[20][21][22]
- 饱和脂肪[17][23]
- 摄取过多糖类[17][24]
- 偏高的三酸甘油酯[17]
- 系统性炎症[25]
- 高胰岛素血症[26]
- 睡眠剥夺[27]
- 空气污染[28][29]
- 久坐的习惯[17]
- 砷中毒[30]
- 酒精[17]
- 慢性压力[17]
- 甲状腺机能低下症[31]
- 牙周炎[32]:感染导致牙龈发炎、损伤,病菌进入血管可导致动脉粥样硬化。[33]
预防
编辑大量流行病学研究和随机对照临床试验证实,低密度胆固醇的升高是引发动脉粥样硬化的的一个重要因素[34],因此推动终身的健康生活方式与饮食能帮助管理血液中的胆固醇。即使是基因遗传导致动脉粥样硬化风险较高的人也可通过改变生活方式来降低多达50%的风险。除此之外,保持正常的体重和血糖、减少单糖和精制碳水化合物摄入量与增加运动频率均可改善血脂水平并促进健康。[35]
治疗
编辑临床试验证实可以透过以下药物减少血液中低密度胆固醇含量进而减少动脉粥样硬化心脏病的风险:
- 他汀类药物:HMG-CoA reductase的竞争性抑制剂,可影响胆固醇合成过程中的速率决定步骤。对HMG-CoA reductase的抑制会使肝脏合成更多LDL受体,使LDL更容易从血液循环内清除。其为降低低密度胆固醇之首选用药然而需注意其肌痛的不良反应。[36]
- Ezetimibe:阻断Niemann-Pick C1-like 1 cholesterol transfer protein,从而抑制肠道和胆道的胆固醇吸收,使肝脏LDL受体表达增加。通常会与他汀类药物合用。[37]
- PCSK9 抑制剂:使PCSK9 enzyme失去活性无法分解LDL受体,从而增加肝细胞上的LDL受体数量,进而促进血液循环内LDL胆固醇的清除。[38]
- N-3 fatty acid:可减少肝脏内VLDL的生成并少量增加血液循环内VLDL胆固醇的清除,进而通过这一方式降低血中triglyceride浓度。[39]
参见
编辑参考资料
编辑- ^ 1.0 1.1 1.2 1.3 1.4 1.5 What Are the Signs and Symptoms of Atherosclerosis?. NHLBI, NIH. 2016-06-22 [2017-11-05]. (原始内容存档于2017-10-05) (英语).
- ^ 2.0 2.1 What Causes Atherosclerosis? - NHLBI, NIH. NHLBI, NIH. 2016-06-22 [2017-11-06]. (原始内容存档于2015-04-23) (英语).
- ^ 3.0 3.1 3.2 Who Is at Risk for Atherosclerosis? - NHLBI, NIH. NHLBI, NIH. 2016-06-22 [2017-11-05]. (原始内容存档于2017-10-05) (英语).
- ^ 4.0 4.1 How Can Atherosclerosis Be Prevented or Delayed? - NHLBI, NIH. NHLBI, NIH. 2016-06-22 [2017-11-06]. (原始内容存档于2017-11-07) (英语).
- ^ 5.0 5.1 How Is Atherosclerosis Treated?. NHLBI, NIH. 2016-06-22 [2017-11-06]. (原始内容存档于2017-11-07) (英语).
- ^ 6.0 6.1 Aronow, Wilbert S.; Fleg, Jerome L.; Rich, Michael W. Tresch and Aronow's Cardiovascular Disease in the Elderly, Fifth Edition. CRC Press. 2013: 171 [2018-05-11]. ISBN 9781842145449. (原始内容存档于2021-08-03) (英语).
- ^ Insull Jr, William. "The pathology of atherosclerosis: plaque development and plaque responses to medical treatment." The American journal of medicine 122.1 (2009): S3-S14.
- ^ 8.0 8.1 What Is Atherosclerosis? - NHLBI, NIH. NHLBI, NIH. 2016-06-22 [2017-11-06]. (原始内容存档于2017-12-02) (英语).
- ^ 国家教育研究院. 醫學名詞. 元照出版公司. 2015: 43.
- ^ (2011). Atherosclerosis/Atheroma. In: Khan, M.G. (eds) Encyclopedia of Heart Diseases. Humana Press. https://doi.org/10.1007/978-1-60761-219-3_21
- ^ How Is Atherosclerosis Diagnosed? - NHLBI, NIH. NHLBI, NIH. 2016-06-22 [2017-11-06]. (原始内容存档于2017-10-05) (英语).
- ^ Shor A. Chlamydia Atherosclerosis Lesion: Discovery, Diagnosis and Treatment. Springer Science & Business Media. 2008: 8 [2019-02-12]. ISBN 9781846288104. (原始内容存档于2021-08-03) (英语).
- ^ Topol EJ, Califf RM. Textbook of Cardiovascular Medicine. Lippincott Williams & Wilkins. 2007: 2 [2019-02-12]. ISBN 9780781770125. (原始内容存档于2021-08-03) (英语).
- ^ Ross, Russell. The pathogenesis of atherosclerosis: a perspective for the 1990s. Nature. 1993-04, 362 (6423): 801–809 [2022-01-17]. ISSN 0028-0836. PMID 8479518. doi:10.1038/362801a0. (原始内容存档于2021-10-27) (英语).
- ^ Finn, Aloke V.; Nakano, Masataka; Narula, Jagat; Kolodgie, Frank D.; Virmani, Renu. Concept of vulnerable/unstable plaque. Arteriosclerosis, Thrombosis, and Vascular Biology. 2010-07, 30 (7): 1282–1292 [2022-01-17]. ISSN 1524-4636. PMID 20554950. doi:10.1161/ATVBAHA.108.179739. (原始内容存档于2021-12-07).
- ^ Manning, Robert. Livestrong.com. What Is A Foam Cell?. Demand Media Inc. [5 March 2013]. (原始内容存档于2017-09-08).
- ^ 17.00 17.01 17.02 17.03 17.04 17.05 17.06 17.07 17.08 17.09 17.10 17.11 17.12 17.13 17.14 17.15 17.16 17.17 Atherosclerosis. NHLBI, NIH. [2018-05-11]. (原始内容存档于2017-10-05).
- ^ Enas EA, Kuruvila A, Khanna P, Pitchumoni CS, Mohan V. Benefits & risks of statin therapy for primary prevention of cardiovascular disease in Asian Indians - a population with the highest risk of premature coronary artery disease & diabetes. Indian J Med Res. October 2013, 138 (4): 461–491 [2018-05-14]. PMC 3868060 . PMID 24434254. (原始内容存档于2021-05-18).
- ^ Indian Heart Association Why South Asians Facts Web. 30 April 2015. http://indianheartassociation.org/why-indians-why-south-asians/overview/ (页面存档备份,存于互联网档案馆)
- ^ Borissoff JI, Spronk HM, Heeneman S, ten Cate H. Is thrombin a key player in the 'coagulation-atherogenesis' maze?. Cardiovasc. Res. June 2009, 82 (3): 392–403 [2018-05-14]. PMID 19228706. doi:10.1093/cvr/cvp066. (原始内容存档于2011-03-21).
- ^ Borissoff JI, Heeneman S, Kilinç E, et al. Early atherosclerosis exhibits an enhanced procoagulant state. Circulation. August 2010, 122 (8): 821–30 [2018-05-14]. PMID 20697022. doi:10.1161/CIRCULATIONAHA.109.907121. (原始内容存档于2011-02-12).
- ^ Borissoff JI, Spronk HM, ten Cate H. The hemostatic system as a modulator of atherosclerosis. N. Engl. J. Med. May 2011, 364 (18): 1746–60 [2018-05-14]. PMID 21542745. doi:10.1056/NEJMra1011670. (原始内容存档于2020-05-18).
- ^ Food and nutrition board, institute of medicine of the national academies. Dietary Reference Intakes for Energy, Carbohydrate, Fiber, Fat, Fatty Acids, Cholesterol, Protein, and Amino Acids (Macronutrients). National Academies Press. 2005: 481–484 [2018-05-14]. (原始内容存档于2015-09-06).
- ^ Mozaffarian D, Rimm EB, Herrington DM. Dietary fats, carbohydrate, and progression of coronary atherosclerosis in postmenopausal women. Am. J. Clin. Nutr. November 2004, 80: 1175–84. PMC 1270002 . PMID 15531663. doi:10.1093/ajcn/80.5.1175.
- ^ Bhatt DL, Topol EJ. Need to test the arterial inflammation hypothesis. Circulation. July 2002, 106 (1): 136–40 [2018-05-14]. PMID 12093783. doi:10.1161/01.CIR.0000021112.29409.A2. (原始内容存档于2007-03-11).
- ^ Griffin M, Frazer A, Johnson A, Collins P, Owens D, Tomkin GH. Cellular cholesterol synthesis—the relationship to post-prandial glucose and insulin following weight loss. Atherosclerosis. 1998, 138 (2): 313–8. PMID 9690914. doi:10.1016/S0021-9150(98)00036-7.
- ^ King, Cr; Knutson, Kl; Rathouz, Pj; Sidney, S; Liu, K; Lauderdale, Ds. Short sleep duration and incident coronary artery calcification. JAMA: The Journal of the American Medical Association. December 2008, 300 (24): 2859–66. PMC 2661105 . PMID 19109114. doi:10.1001/jama.2008.867.
- ^ Provost, EB; Madhloum, N; Int Panis, L; De Boever, P; Nawrot, TS. Carotid intima-media thickness, a marker of subclinical atherosclerosis, and particulate air pollution exposure: the meta-analytical evidence. PLoS ONE. 2015, 10 (5): e0127014. PMC 4430520 . PMID 25970426. doi:10.1371/journal.pone.0127014.
- ^ Adar, Sara D.; Lianne Sheppard; Sverre Vedal; Joseph F. Polak; Paul D. Sampson; Ana V. Diez Roux; Matthew Budoff; David R. Jacobs Jr; R. Graham Barr; Karol Watson; Joel D. Kaufman. Fine Particulate Air Pollution and the Progression of Carotid Intima-Medial Thickness: A Prospective Cohort Study from the Multi-Ethnic Study of Atherosclerosis and Air Pollution. PLoS Medicine. April 23, 2013, 10 (4): e1001430 [May 4, 2013]. PMC 3637008 . PMID 23637576. doi:10.1371/journal.pmed.1001430. (原始内容存档于2014-12-27).
This early analysis from MESA suggests that higher long-term PM2.5 concentrations are associated with increased IMT progression and that greater reductions in PM2.5 are related to slower IMT progression.
- ^ Chih-Hao Wang. Biological Gradient Between Long-Term Arsenic Exposure and Carotid Atherosclerosis. ahajournals.org. [2018-05-14]. (原始内容存档于2017-03-09).
- ^ Treating Hypothyroidism Reduces Atherosclerosis Risk. American Family Physician. 2004-02-01, 69 (3) [2018-05-14]. ISSN 0002-838X. (原始内容存档于2019-06-17) (英语).
- ^ Bale, BF; Doneen, AL; Vigerust, DJ. High-risk periodontal pathogens contribute to the pathogenesis of atherosclerosis.. Postgraduate medical journal. April 2017, 93 (1098): 215–220. PMID 27899684. doi:10.1136/postgradmedj-2016-134279.
- ^ Jie Yang; Juan Wu; Rui Zhang; Min Yao; Yu Liu; Leiying Miao; Weibin Sun. Porphyromonas gingivalis oral infection promote T helper 17/Treg imbalance in the development of atherosclerosis. Dental Sciences. 2016-12-14, 12 (1): 60–69.
- ^ Efficacy and safety of more intensive lowering of LDL cholesterol: a meta-analysis of data from 170 000 participants in 26 randomised trials. The Lancet. 2010-11, 376 (9753): 1670–1681. ISSN 0140-6736. doi:10.1016/s0140-6736(10)61350-5.
- ^ Brinton, Eliot A. Management of Hypertriglyceridemia for Prevention of Atherosclerotic Cardiovascular Disease. Cardiology Clinics. 2015-05, 33 (2): 309–323. ISSN 0733-8651. doi:10.1016/j.ccl.2015.02.007.
- ^ Thompson, Paul D. What to Believe and Do About Statin-Associated Adverse Effects. JAMA. 2016-11-15, 316 (19): 1969. ISSN 0098-7484. doi:10.1001/jama.2016.16557.
- ^ Aronow, Wilbert. Faculty of 1000 evaluation for Ezetimibe Added to Statin Therapy after Acute Coronary Syndromes.. F1000 - Post-publication peer review of the biomedical literature. 2015-06-21 [2019-12-31].
- ^ Abifadel, Marianne; Varret, Mathilde; Rabès, Jean-Pierre; Allard, Delphine; Ouguerram, Khadija; Devillers, Martine; Cruaud, Corinne; Benjannet, Suzanne; Wickham, Louise. Mutations in PCSK9 cause autosomal dominant hypercholesterolemia. Nature Genetics. 2003-05-05, 34 (2): 154–156. ISSN 1061-4036. doi:10.1038/ng1161.
- ^ JE, Manson; NR, Cook; IM, Lee; W, Christen; SS, Bassuk; S, Mora; H, Gibson; CM, Albert; D, Gordon. Marine n-3 fatty acids and prevention of cardiovascular disease and cancer. Yearbook of Paediatric Endocrinology. 2019-09-12. ISSN 1662-4009. doi:10.1530/ey.16.12.13.