诺氏疟原虫
诺氏疟原虫(Plasmodium knowlesi,可缩写为P. knowlesi)又称猴疟虫,是一种常见于东南亚的灵长类疟原虫[1]。它能在食蟹猴体内引起疟疾,但它也可能自然或人为地感染人类。
| 诺氏疟原虫 | |
|---|---|
| |
| 科学分类 | |
| 演化支: | SAR 超类群 SAR |
| 演化支: | 囊泡虫类 Alveolata |
| 门: | 粘孢子总门 Myzozoa |
| 纲: | 无类锥体纲 Aconoidasida |
| 目: | 血孢子虫目 Haemosporida |
| 科: | 疟原虫科 Plasmodiidae |
| 属: | 疟原虫属 Plasmodium |
| 种: | 诺氏疟原虫 P. knowlesi
|
| 二名法 | |
| Plasmodium knowlesi Sinton and Mulligan 1933
| |
由于卵形疟原虫(Plasmodium ovale ) 后来被分为两个亚种,但由于亚种还未到种阶,所以在主要的人类疟原虫中,诺氏疟原虫目前依然为第五种被发现的疟原虫。它可能会引发严重的疟疾,其无性繁殖的红血球内期约为24小时,患者通常会伴有周期性的间歇性寒热发作。[2][3][4]这是人类于1965年首次发现的新型传染病[2],在东南亚某些地区确诊的疟疾病例中,有70%的患者是被这种疟原虫感染[5]。诺氏疟原虫由疟蚊叮咬传播,[5]它严重影响了疫区居民的健康、当地经济的发展与社会的稳定。
发现史
编辑诺氏疟原虫是由意大利寄生虫学家朱塞佩·弗兰奇尼于1927年在观察食蟹猴血液标本时首次发现的。他当时指出了诺氏疟原虫不同于食蟹猴疟原虫(Plasmodium cynomolgi )和猪尾猴疟原虫(Plasmodium inui )[6]。后来,坎贝尔在位于印度加尔各答的英国皇家热带医学与卫生学院工作时,于1931年从由新加坡进口的长尾猕猴体内也发现了这种疟原虫。坎贝尔当时在L.E.纳皮尔手下工作,并在研究由另一种原虫引发的传染病——黑热病(内脏利什曼病)。纳皮尔给三种猴子接种了疟原虫菌株,其中,在被接种的恒河猴(Macaca mulatta )种群中引发了暴发性的感染。纳皮尔当时得知了微生物部门也在寻找引起猕猴患病的疟原虫菌株,于是就将最先被接种疟原虫菌株的猕猴交给了罗伯特·诺尔斯博士的助手B·莫罕达斯·古普塔。古普塔博士在诺尔斯博士休假回来之前通过连续传代维持了该种群的繁衍。1932年,诺尔斯和达斯·古普塔首次详细地描述了该疟原虫物种,并表示它可以通过血液传播给人类,但没有为其正式命名。其后,辛顿(Sinton)和穆里根(Mulligan)将其正式命名为诺氏疟原虫(Plasmodium knowlesi )。在20世纪30年代早期到1955年,医学界还曾广泛采用给晚期梅毒(神经性梅毒)患者注射诺氏疟原虫菌株的方法以阻断梅毒螺旋体在神经中的推进过程。[7]因为间日疟原虫或诺氏疟原虫引起人体三轮或者四轮高烧后,就会对密螺旋体带来近乎致命的打击,而梅毒螺旋体属于密螺旋体的一种。[8][9][10]
1957年,加纳姆等人[11]提出:诺氏疟原虫可能是第五种能够引起人类地方性疟疾的物种。
1960年,美国寄生虫学家唐·E·艾尔斯(英语:Don E. Eyles)和他的导师G·罗伯特·科特尼(英语:G. Robert Coatney,1902-1990)在美国国立卫生研究院的孟菲斯实验室对恒河猴进行了实验,他们假设人类并不会感染“猴疟”,因为早期的研究已经得出结论,猕猴不能寄生间日疟原虫。而间日疟原虫是一种人类疟原虫。这使得艾尔斯和科特尼开始研究食蟹猴疟原虫,这是一种与间日疟原虫非常相似的寄生虫,可以模拟人类疟疾感染。实验中,这两位研究人员将自己暴露在感染环境之中,对叮咬所引起的瘙痒并不在意;然而,艾尔斯在实验后不久就发烧了。直到几天后,两人才怀疑艾尔斯可能已经感染了疟疾。后来经过对血涂片的检查证实,人类实际上是有可能感染“猴疟”的。[12]
1965年,一名在美国陆军地图服务处担任调查员的37岁男子,报告了首例自然发生的人类感染诺氏疟原虫病例。他曾在马来西亚半岛有过短暂旅行,之后前往泰国并在当地感到不适后就医。[12]最初,其所被鉴定为感染了恶性疟原虫,但在一天后又被鉴定为三日疟原虫,直到用感染的血液接种给了恒河猴后才被确认为诺氏疟原虫。[8]在观察发生感染时,G·罗伯特·科特尼博士和其他研究人员发现,当地人群经常会接触到这种寄生虫。而且,他们和当地的猴子群体是该寄生虫的联合宿主。观察到这一结果的科特尼宣布:“猴疟”是一种“真正的人畜共患疾病”。在该名调查员接受治疗之前,科特尼将其血液样本送回他在亚特兰大的实验室,在那里,这些血液将会被用来感染监狱中的志愿囚犯和恒河猴。[12]第二份关于自然感染诺氏疟原虫的报告出现在1971年。报告中指出:有一名马来西亚男子自然感染了诺氏疟原虫,因此获得了在马来西亚婆罗洲沙捞越加帛区有人类感染诺氏疟原虫的这一重大进展。[8]如今,得益于分子检测实验的不断发展,目前已经可以区分诺氏疟原虫和与其形态相似的三日疟原虫。自2004年以来,在东南亚各国,包括马来西亚、泰国、新加坡、菲律宾、越南、缅甸和印度尼西亚,有关于人感染诺氏疟原虫的报告逐渐增多。[13]
经过对档案样本的研究表明,这种寄生虫至少在上世纪90年代以来,就在马来西亚发生过感染。[14]目前已知在沙捞越的某些地区,70%的疟疾病例是由这种寄生虫引起的。[15]
进化史
编辑基于贝叶斯聚类算法,诺氏疟原虫最可能的进化时间是25.7万年前(95%最高后密度区间(HPD)为:9.8 - 47.8万年前)。[16]雅各布和他的同事利用进化算法入侵检测分析计算了自然宿主从长尾猕猴向人类转移的可能性,并证明了相对宿主密度和个体层面上蚊子捕食偏好是如何影响这种转移的。[17]
生活史
编辑诺氏疟原虫寄生虫能够在24小时内复制并完成其血液循环周期[4],这使得其可以在非常短的时间内产生相当高的寄生虫密度负荷。因此,如果未对此进行治疗,将会导致其发展成为一种非常严重的潜在疾病。其生命周期:裂殖子→营养体→裂殖体→裂殖子。处于这些阶段的诺氏疟原虫在显微镜中与三日疟原虫难以区分,早期营养体与恶性疟原虫相同。
蚊虫体内:[18]蚊子吞食哺乳动物宿主体内形成的配子细胞。它们要么是小配子细胞(雄性配子细胞)要么是大配子细胞(雌性配子细胞)。这些配子细胞分别发育成小配子和大配子,然后在蚊子的中肠内受精形成受精卵。受精卵成熟为卵母细胞,然后发育成卵囊。最后,卵囊发育成熟,释放出子孢子,进入蚊子的唾液腺。
摘要:配子体→(小配子或大配子)→受精卵→卵母细胞 →卵囊→子孢子。
人体中: 红血球外期(肝脏中):[18]蚊子叮咬人体后,将孢子体注入人体,通过血流进入肝脏,经过无性繁殖,并通过肝细胞分裂形成裂殖体。目前还没有在肝脏中发现休眠子[19]。
摘要:子孢子→裂殖体→裂殖子。
人体中:红血球内期(血液中):[18]裂殖子释放到血液中,感染构成红细胞的一个无性循环。在红细胞内,一些裂殖子发育为滋养体,滋养体又发育为分裂体,分裂后释放裂殖子,而另一些则发育为小配子细胞或大配子细胞。这些配子细胞留在血液中,蚊子可以将其吞下。
摘要:裂殖子→营养体→裂殖体→裂殖子。
传染史
编辑诺氏疟原虫通常被认为是长尾猕猴和猪尾猕猴[13][20]的寄生虫,但在森林边缘工作或进入雨林工作的人类也有感染的风险。随着东南亚的森林砍伐和加快发展的日益流行,人类现在正与许多猕猴有着密切和直接的接触。[13]因此,越来越多生活在城市边缘地区的人被发现感染了诺氏疟疾。2014年,马来西亚便报告了2,584例这种类型的疟疾。[21]
这种寄生虫主要出现在东南亚国家和地区,婆罗洲、柬埔寨、[22]马来西亚、缅甸、菲律宾、新加坡[23]、泰国[24]和邻近国家。而且据报道,这种寄生虫似乎出现在没有其他四种人类疟疾的地区。受感染的蚊子仅限于森林地区。非传染性蚊子通常出现在城市地区,但由于该地区蚊子数量众多,还是可能会发生传播。[2][25]特别是马来西亚[8],但泰缅边境也有相关的报道。[3]马来西亚婆罗洲沙捞越地区确诊的疟疾病例中,有五分之一是由诺氏疟原虫引起的。[8]
诺氏疟原虫在非洲并不存在。这可能是因为非洲既没有长尾猕猴,也没有猪尾猕猴(二者均为诺氏疟原虫的宿主),而且许多西非人缺乏达菲抗原——这是该寄生虫用来入侵红细胞表面的一种蛋白质。
传播媒介
编辑诺氏疟原虫理论上有四种传播模式:从受感染的蚊子到另一只猴子,从受感染的猴子到人,从受感染的人到另一个人,再从受感染的人回到猴子。[13]在实际中,人类疟疾似乎几乎完全是由于猴子对人类的传播。
已知载体为:按蚊属、塞利氏蚊组亚属、新迈蚊系、白踝按蚊组[4]这一群体的蚊子通常出现在东南亚的森林地区,但随着森林地区越来越多地被用于耕田,人类正越来越多地接触这些媒介。
在马来西亚半岛的猴群中,哈克里按蚊被认为是诺氏疟原虫的主要传播媒介。但是,虽然哈克里按蚊(Anopheles hackeri)能够将疟疾传播给人类,[27]但人类对其并没有吸引力,似乎也不太可能成为传播给人类的重要媒介。[28]
猕猴和人类都有吸引力对按蚊(Anopheles latens)均有吸引力,并已被证明是在马来西亚婆罗洲沙罗越加帛区向人类传播诺氏疟原虫的主要媒介。[29]
据报道,按蚊(Anopheles cracens)也是诺氏疟原虫的载体。两种蚊子均属于白踝按蚊种群,都被证明含有多达1,000个子孢子,这表明它们可能是有效的载体。[13]
临床
编辑目前已经提出了两种可能的人类传播模式:一种是从受感染的猴子传染给人类,另一种是从受感染的人传染给另一个人。
症状通常在被感染的蚊子咬人后大约11天开始出现,感染后10-12天可在血液中看到寄生虫。[31]寄生虫可能迅速繁殖,导致非常高的寄生虫密度,如此将可能出现生命风险。[31]
虽然目前诺氏疟原虫的感染率相对较低,但它带来的一个风险是在使用显微镜时与其他形式的疟疾寄生虫(如P. malariae)弄混导致误诊。诺氏疟原虫只有通过PCR和/或分子鉴定才能准确地与疟原虫区分开来。
诺氏疟原虫在人类身上的症状包括头痛、发烧、发冷和出冷汗。[31]辛格等人(2004)[8]在马来西亚婆罗洲沙罗越卡皮特医院发现94例单种诺氏疟原虫感染患者出现临床症状。症状包括:100%的患者出现发烧,发冷和僵直、32%的患者出现头痛、18%的患者出现咳嗽、16%的患者出现呕吐、6%的患者出现恶心、4%的患者出现腹泻。这种寄生虫在人类及其自然宿主猕猴体内的无性繁殖周期约为24小时.[2][3][4]因此,这种疾病可以与间日疟和三日疟[18]一起命名称为日常疟疾[2]。除了使用PCR分析进行实验室诊断外,诺氏疟原虫自身也可能出现c反应蛋白水平升高和血小板减少。
由于这种寄生虫在其红细胞外期阶段缺乏休眠子[32],进而导致疟疾不会复发[33]。
虽然这种微生物的感染通常并不严重,但在少数病例中可能发生危及生命的并发症甚至死亡。最常见的并发症是呼吸窘迫、肝功能异常,包括黄疸和肾功能衰竭。一组病例的死亡率约为2%。[15]
诊断
编辑诺氏疟原虫感染的诊断方法与其他疟疾一样,采用厚薄血膜涂片检查法。诺氏疟原虫的外观类似于三日疟原虫,除非在疟疾参考实验室中使用分子检测方法[8],否则很难正确诊断。
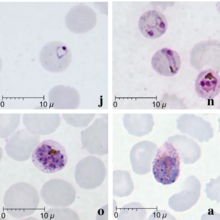
诺氏疟原虫的形态与三日疟原虫相似。疟疾的特点是寄生虫密集(所有阶段),不会改变宿主红细胞的形状或大小,也不会引起红细胞的增大。有时可观察到横跨红细胞的细长滋养体,称为条带型。裂殖子通常有8-10个裂殖子,通常呈莲座状排列,中间有一团色素。[34]
由于诺氏疟原虫的特异性,快速诊断测试试剂盒不一定能够识别。
目前,聚合酶链式反应(PCR)检测和分子鉴定是检测和诊断诺氏疟原虫感染最可靠的方法。PCR能够鉴定寄生虫的DNA,但该技术鉴定速度较慢,无法用于常规鉴定。此外,PCR也很昂贵,需要非常专业的设备。[8]
治疗
编辑由于诺氏疟原虫只需要24小时就能完成其红细胞周期,因此当它进入人体血液后可以迅速导致严重的寄生虫血症,并带来致命的后果。如同感染恶性疟疾一样,任何病情严重和迅速恶化的人都接受紧急和积极地治疗。[4]
氯喹和伯氨喹对诺氏疟原虫有较好的疗效。在一项治疗的临床研究中发现,采用口服氯喹三天后连续两天24小时口服伯氨喹[35]的治疗方法后对寄生虫的清除反应迅速,平均时间为3小时。而间日疟原虫需要6至7小时才能清除。
公共卫生、预防策略和疫苗
编辑病理
编辑迄今为止,仅一例关于感染诺氏疟原虫的验尸报告。其报告描述为[36]:男性患者,暴露10天后出现不适。四天后前往医院就诊,身体严重不适。他的嗜酸性粒细胞计数升高,血小板减少,低钠血症,尿素、钾、乳酸脱氢酶和氨基转移酶值升高。曾有人怀疑是骨痛热症,但经过调查后排除了这种可能性。血液抹片上可见疟原虫,经PCR鉴定为诺氏疟原虫。尸检肝脾肿大。大脑与心内膜表现为多发瘀点出血,肺部特征与急性呼吸窘迫综合征一致。组织学检查显示,在大脑及其他任何器官均没有慢性炎症反应的情况下,大脑、小脑、心脏和肾脏的血管内,色素被寄生的红细胞所隔离。脾脏和肝脏中含有丰富的巨噬细胞和寄生的红细胞。肾脏有急性肾小管坏死的证据。心脏切片中的内皮细胞明显。脑切片对细胞内粘附分子-1呈阴性。
验尸报告的总体情况与恶性疟原虫的情况非常相似。虽然都有脑部有出血和寄生虫隔离的现象,但仍有重要的差异,如患者并没有昏迷。
注释
编辑加纳姆曾在1963年对已知的诺氏疟原虫两个亚种——P. knowlesi edesoni和P. knowlesi knowlesi有过描述。[37]其以寄生虫学家J F B Edeson的名字进行命名。目前尚不清楚这两个亚种之间是否存在临床差异。
相关网页链接
编辑- 1. 疾病预防控制中心:cdc.gov/malaria,https://www.cdc.gov/EID/content/14/11/1750.htm(页面存档备份,存于互联网档案馆)
- 2. 世界卫生组织:http://www.who.int/topics/malaria/en/(页面存档备份,存于互联网档案馆)
- 3. 关于发现诺氏疟原虫在人类疟疾中作用的短片:http://www.abc.net.au/catalyst/stories/2533454.htm(页面存档备份,存于互联网档案馆)
诺氏疟原虫基因组数据
编辑参考来源
编辑- ^ Perkins, Susan L.; Jos. J. Schall. A molecular phylogeny of malarial parasites recovered from cytochrome b gene sequences. Journal of Parasitology. 2002, 88 (2): 972–978. PMID 12435139. doi:10.1645/0022-3395(2002)088[0972:AMPOMP]2.0.CO;2.
- ^ 2.0 2.1 2.2 2.3 2.4 Chin W, Contacos PG, Coatney RG, Kimbal HR. A naturally acquired quotidian-type malaria in man transferable to monkeys. Science. 1965, 149 (3686): 865. PMID 14332847. doi:10.1126/science.149.3686.865.
- ^ 3.0 3.1 3.2 Jongwutiwes S, Putaporntip C, Iwasaki T, Sata T, Kanbara H. Naturally acquired Plasmodium knowlesi malaria in human, Thailand. Emerg. Infect. Dis. 2004, 10 (12): 2211–3. PMC 3323387 . PMID 15663864. doi:10.3201/eid1012.040293.
- ^ 4.0 4.1 4.2 4.3 4.4 Cox-Singh J, Davis TM, Lee KS, Shamsul SS, Matusop A, Ratnam S, Rahman HA, Conway DJ, Singh B. Plasmodium knowlesi malaria in humans is widely distributed and potentially life-threatening. Clin. Infect. Dis. 2008, 46 (2): 165–171. PMC 2533694 . PMID 18171245. doi:10.1086/524888.
- ^ 5.0 5.1 McCutchan TF, Piper RC, Makler MT. Use of Malaria Rapid Diagnostic Test to Identify Plasmodium knowlesi Infection. Emerg Infect Dis. 2008, 14 (11): 1750–1752. PMC 2630758 . PMID 18976561. doi:10.3201/eid1411.080840.
- ^ Franchini G (1027) Su di un plasmodio pigmentato di una scimmia. Arch Ital Sci Med Colon 8:187–90
- ^ 以毒攻毒以病克病!用疟原虫治癌症原来“有戏”. news.china.com. [2018-11-29]. (原始内容存档于2018-12-06).
- ^ 8.0 8.1 8.2 8.3 8.4 8.5 8.6 8.7 Singh B, Lee KS, Matusop A, Radhakrishnan A, Shamsul SS, Cox-Singh J, Thomas A, Conway DJ. A large focus of naturally acquired Plasmodium knowlesi infections in human beings. Lancet. 2004, 363 (9414): 1017–24. PMID 15051281. doi:10.1016/S0140-6736(04)15836-4.
- ^ 《致命接触》的笔记-第三章 疟疾. book.douban.com. [2018-11-29]. (原始内容存档于2018-12-06).
- ^ 【南方都市报】以毒攻毒 用疟原虫治癌症“有戏”. www.gibh.cas.cn. [2018-11-29]. (原始内容存档于2018-12-06).
- ^ Garnham PC, Lainson R, Cooper W. The tissue stages and sporogony of Plasmodium knowlesi. Trans R Soc Trop Med Hyg. 1957, 51 (5): 384–396. PMID 13467997. doi:10.1016/0035-9203(57)90071-8.
- ^ 12.0 12.1 12.2 Mason Dentinger, Rachel. Patterns of Infection and Patterns of Evolution: How a Malaria Parasite Brought "Monkeys and Man" Closer Together in the 1960s. Journal of the History of Biology. 2015-08-26, 49 (2): 359–395. PMID 26307748. doi:10.1007/s10739-015-9421-8.
- ^ 13.0 13.1 13.2 13.3 13.4 Vythilingam I, Noorazian YM, Huat TC, Jiram AI, Yusri YM, Azahari AH, Norparina I, Noorrain A, Lokmanhakim S. Plasmodium knowlesi in humans, macaques and mosquitoes in peninsular Malaysia. Parasit Vectors. 2008, 1 (1): 26. PMC 2531168 . PMID 18710577. doi:10.1186/1756-3305-1-26.
- ^ Lee K.S.; Cox-Singh J.; Brooke G.; Matusop A.; Singh B. Plasmodium knowlesi from archival blood films: Further evidence that human infections are widely distributed and not newly emergent in Malaysian Borneo. Int J Parasitol. 2009, 39 (10): 1125–1128. PMC 2722692 . PMID 19358848. doi:10.1016/j.ijpara.2009.03.003.
- ^ 15.0 15.1 Daneshvar C., Davis T.M.E., Cox‐Singh J., et al. Clinical and Laboratory Features of Human Plasmodium knowlesi Infection. Clin Infect Dis. 2009, 49 (6): 852–860. PMC 2843824 . PMID 19635025. doi:10.1086/605439.
- ^ Lee KS, Divis PC, Zakaria SK, Matusop A, Julin RA, Conway DJ, Cox-Singh J, Singh B. Kazura JW , 编. Plasmodium knowlesi: Reservoir Hosts and Tracking the Emergence in Humans and Macaques. PLoS Pathog. 2011, 7 (4): e1002015. PMC 3072369 . PMID 21490952. doi:10.1371/journal.ppat.1002015.
- ^ Yakob, L.; Bonsall, M.B.; Yan, G. Modelling knowlesi malaria transmission in humans: vector preference and host competence. Malaria Journal. 2010, 9: e329. PMC 2996403 . PMID 21080968. doi:10.1186/1475-2875-9-329.
- ^ 18.0 18.1 18.2 18.3 Manson-Bahr PEC, Bell DR, eds. (1987). Manson's Tropical Diseases. London: Bailliere Tindall, ISBN 0-7020-1187-8.
- ^ Markus, MB. Malaria: Origin of the Term "Hypnozoite". Journal of the History of Biology. 2011, 44 (4): 781–786. PMID 20665090. doi:10.1007/s10739-010-9239-3.
- ^ Ng O.T.; Ooi E.E.; Lee C.C.; Lee P.J.; Ng L.C.; Pei S.W.; Tu T.M.; Loh J.P.; Leo Y.S. Naturally Acquired Human Plasmodium knowlesi Infection, Singapore. Emerg. Infect. Dis. 2008, 14 (5): 814–816. PMC 2600232 . PMID 18439370. doi:10.3201/eid1405.070863.
- ^ Malaysia: Dengue cases top 45,000, 'monkey malaria' accounts for majority of human malaria cases. 2015-05-25 [2018-11-19]. (原始内容存档于2017-02-27).
- ^ Khim N, Siv S, Kim S, Mueller T, Fleischmann E, Singh B, Divis PC, Steenkeste N, Duval L, et al. Plasmodium knowlesi infection in humans, Cambodia, 2007-2010. Emerg Infect Dis. 2011, 17 (10): 1900–1902. PMC 3310675 . PMID 22000366. doi:10.3201/eid1710.110355.
- ^ Jeslyn WP, Huat TC, Vernon L, Irene LM, Sung LK, Jarrod LP, Singh B, Ching NL. Molecular Epidemiological Investigation of Plasmodium knowlesi in Humans and Macaques in Singapore. Vector Borne Zoonotic Dis. 2010, 11 (2): 131–5. PMC 3033207 . PMID 20586605. doi:10.1089/vbz.2010.0024.
- ^ Jongwutiwes S, Buppan P, Kosuvin R, Seethamchai S, Pattanawong U, Sirichaisinthop J, Putaporntip C. Plasmodium knowlesi malaria in humans and macaques, Thailand. Emerg Infect Dis. 2011, 17 (10): 1799–1806. PMC 3310673 . PMID 22000348. doi:10.3201/eid1710.110349.
- ^ Yap FL, Cadigan FC, Coatney GR. A presumptive case of naturally occurring Plasmodium knowlesi malaria in man in Malaysia. Trans R Soc Trop Med Hyg. 1971, 65 (6): 839–40. PMID 5003320. doi:10.1016/0035-9203(71)90103-9.
- ^ Barber BE, William T, Jikal M, Jilip J, Dhararaj P, Menon J, Yeo TW, Anstey NM. Plasmodium knowlesi malaria in children. Emerg Infect Dis. 2011, 17 (5): 814–820. PMC 3321776 . PMID 21529389. doi:10.3201/eid1705.101489.
- ^ Wharton RH, Eyles DE. Anopheles hackeri, a vector of Plasmodium knowlesi in Malaya. Science. 1961, 134 (3474): 279–80. PMID 13784726. doi:10.1126/science.134.3474.279.
- ^ Reid JA, Weitz B. Anopheline mosquitoes as vectors of animal malaria in Malaya. Ann Trop Med Parasitol. 1961, 55: 180–6. PMID 13740488.
- ^ Vythilingam I, Tan CH, Asmad M, Chan ST, Lee KS, Singh B. Natural transmission of Plasmodium knowlesi to humans by Anopheles latens in Sarawak, Malaysia. Trans R Soc Trop Med Hyg. 2006, 100 (11): 1087–88. PMID 16725166. doi:10.1016/j.trstmh.2006.02.006.
- ^ Jiram AI, Vythilingam I, Noorazian YM, Yusof YM, Azahari AH, Fong MY. Entomologic investigation of Plasmodium knowlesi vectors in Kuala lipis, Pahang, Malaysia. Malar J. 2012, 11 (1): 213. PMC 3476358 . PMID 22727041. doi:10.1186/1475-2875-11-213.
- ^ 31.0 31.1 31.2 Bronner U.; Divis P.C.; Farnert A.; Singh B. Swedish traveller with Plasmodium knowlesi malaria after visiting Malaysian Borneo. Malar J. 2009, 8: 15. PMC 2634766 . PMID 19146706. doi:10.1186/1475-2875-8-15..
- ^ Krotoski W.A.; Collins W.E. Failure to detect hypnozoites in hepatic tissue containing exoerythrocytic schizonts of Plasmodium knowlesi. Am. J. Trop. Med. Hyg. 1982, 31 (4): 854–856. PMID 7048949.
- ^ Cogswell F.B. The hypnozoite and relapse in primate malaria. Clin. Microbiol. Rev. 1992, 5 (1): 26–35. PMC 358221 . PMID 1735093. doi:10.1128/CMR.5.1.26.
- ^ 存档副本. [2018-11-19]. (原始内容存档于2017-06-10).
- ^ Daneshvar C, Davis TM, Cox-Singh J, Rafa'ee MZ, Zakaria SK, Divis PC, Singh B. Clinical and parasitological response to oral chloroquine and primaquine in uncomplicated human Plasmodium knowlesi infections. Malar. J. 2010, 9: 238. PMC 2933701 . PMID 20723228. doi:10.1186/1475-2875-9-238.
- ^ Cox-Singh J, Hiu J, Lucas SB, Divis PC, Zulkarnaen M, Chandran P, Wong KT, Adem P, Zaki SR. Severe malaria - a case of fatal Plasmodium knowlesi infection with post-mortem findings: a case report. Malar J. 2010, 9 (1): 10. PMC 2818646 . PMID 20064229. doi:10.1186/1475-2875-9-10.
- ^ Garnham, PCC (1963) A new sub-species of Plasmodium knowlesi in the long-tailed macaque. J Trop Med & Hyg 66 : 156-158
扩展阅读
编辑- Collins, W. E. Plasmodium knowlesi: A Malaria Parasite of Monkeys and Humans*. Annual Review of Entomology (Submitted manuscript). 2012, 57: 107–121 [2018-11-19]. PMID 22149265. doi:10.1146/annurev-ento-121510-133540. (原始内容存档于2020-09-23).
警告:默认排序键“Plasmodium Knowlesi”覆盖了之前的默认排序键“Plasmodium knowlesi”。