丙酚替諾福韋
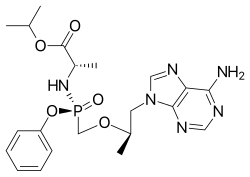
丙酚替諾福韋(Tenofovir alafenamide,縮寫TAF,商品名韋立德(Vemlidy))是一種口服抗逆轉錄病毒藥物,臨床上應用其延胡索酸鹽的形式(富馬酸丙酚替諾福韋) 用於治療B型肝炎或與其他藥物聯用治療愛滋病。
 | |
| 臨床資料 | |
|---|---|
| 讀音 | /ˌtəˈnoʊfəvɪər ˌæləˈfɛnəmaɪd/ |
| 商品名 | 韋立德(Vemlidy) |
| 其他名稱 | GS-7340 |
| AHFS/Drugs.com | Monograph |
| 核准狀況 |
|
| 懷孕分級 | |
| 給藥途徑 | 口服 |
| ATC碼 | |
| 法律規範狀態 | |
| 法律規範 |
|
| 藥物動力學數據 | |
| 血漿蛋白結合率 | ~80%[3] |
| 生物半衰期 | 33分鐘 |
| 排泄途徑 | 腸道排泄(31.7%)和腎臟排泄(<1%) |
| 識別資訊 | |
| |
| CAS號 | 379270-37-8 |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| 化學資訊 | |
| 化學式 | C21H29N6O5P |
| 摩爾質量 | 476.47 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
該藥為替諾福韋的前藥,由吉利德科學研發。與常用的逆轉錄酶抑制劑替諾福韋二吡呋酯(TDF)相比,丙酚替諾福韋具有更強的抗病毒活性和更好的淋巴組織分布。[5][6]該藥於2016年11月獲得FDA批准上市。[7]
相關複方藥物
編輯參考文獻
編輯- ^ 1.0 1.1 Tenofovir alafenamide (Vemlidy) Use During Pregnancy. Drugs.com. 26 December 2018 [18 April 2020]. (原始內容存檔於2021-07-09).
- ^ Vemlidy 25 mg film coated tablets - Summary of Product Characteristics (SmPC). (emc). 8 September 2020 [12 November 2020]. (原始內容存檔於2021-07-11).
- ^ 3.0 3.1 Vemlidy- tenofovir alafenamide tablet. DailyMed. 11 February 2020 [18 April 2020]. (原始內容存檔於2021-07-09).
- ^ Vemlidy EPAR. European Medicines Agency (EMA). [2021-07-01]. (原始內容存檔於2021-07-13).
- ^ Metabolism of GS-7340, a novel phenyl monophosphoramidate intracellular prodrug of PMPA, in blood. Nucleosides Nucleotides Nucleic Acids. 2001, 20 (4–7): 1091–8. PMID 11562963. doi:10.1081/NCN-100002496.
- ^ M Markowitz, A Zolopa, et al.
- ^ FDA Approves Vemlidy (tenofovir alafenamide) for Chronic Hepatitis B in Adults. United States Department of Health and Human Services. 21 November 2016 [11 October 2019]. (原始內容存檔於11 October 2019).
- ^ Descovy- emtricitabine and tenofovir alafenamide tablet. DailyMed. 13 January 2020 [18 April 2020]. (原始內容存檔於2021-06-24).
- ^ FDA approves second drug to prevent HIV infection as part of ongoing efforts to end the HIV epidemic. U.S. Food and Drug Administration (FDA). 3 October 2019 [11 October 2019]. (原始內容存檔於11 October 2019).
- ^ Mandavilli, Apoorva. F.D.A. Approves New H.I.V.-Prevention Drug, but Not for Everyone. The New York Times. 4 October 2019 [11 October 2019]. (原始內容存檔於2021-07-09).
- ^ Symtuza- darunavir, cobicistat, emtricitabine, and tenofovir alafenamide tablet, film coated. DailyMed. 6 March 2020 [18 April 2020]. (原始內容存檔於2021-07-09).
- ^ Drug Approval Package: Symtuza (darunavir, cobicistat, emtricitabine, and tenofovir alafenamide). U.S. Food and Drug Administration (FDA). 11 December 2018 [19 August 2020]. (原始內容存檔於2021-07-09).
- ^ Symtuza EPAR. European Medicines Agency. [19 August 2020]. (原始內容存檔於2021-07-10).
- ^ http://www.ebs.tga.gov.au/servlet/xmlmillr6?dbid=ebs/PublicHTML/pdfStore.nsf&docid=CCE11C6BC5177A30CA2585AE00423857&agid=(PrintDetailsPublic)&actionid=1[失效連結]
- ^ Drugs@FDA: FDA-Approved Drugs. U.S. Food and Drug Administration (FDA). [5 December 2020]. (原始內容存檔於2021-07-09).
外部連結
編輯- Tenofovir alafenamide. Drug Information Portal. U.S. National Library of Medicine. [2021-07-01]. (原始內容存檔於2021-06-24).
- Tenofovir alafenamide fumarate. Drug Information Portal. U.S. National Library of Medicine. [2021-07-01]. (原始內容存檔於2021-07-09).