乾燥症
此條目需要精通或熟悉相關主題的編者參與及協助編輯。 |
乾燥症候群[1](sicca syndrome)又名舍格倫症候群[2](Sjögren syndrome,SjS,SS)或修格蘭[連]氏症候群[3][4]、乾燥症[5],是一種長期影響身體腺體的自體免疫疾病[6][7]。主要導致口乾和乾眼症等乾燥症狀[8],其他症狀包括皮膚乾燥、慢性咳嗽、陰道乾澀、手腳麻、疲倦、肌肉和關節疼痛以及甲狀腺疾病[7],患上這症候群的患者會增加5%罹患淋巴瘤的風險[8][9]。
| 乾燥症候群 | |
|---|---|
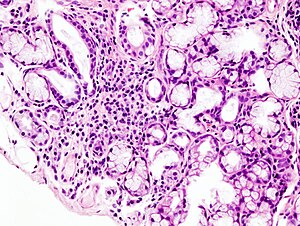 | |
| 乾燥症候群患者的小唾液腺焦點淋巴浸潤情況的組織病理學圖像 (唇部活檢,蘇木精-伊紅染色染色). | |
| 症狀 | 口乾、乾眼症 |
| 類型 | 自體免疫性疾病、外分泌系統自體免疫疾病[*] |
| 病因 | 自體免疫反應 |
| 分類和外部資源 | |
| 醫學專科 | 免疫學、風濕病學 |
| ICD-11 | 4A43.2 |
| ICD-10 | M35.0 |
| ICD-9-CM | 710.2 |
| OMIM | 270150 |
| DiseasesDB | 12155 |
| MedlinePlus | 000456 |
| eMedicine | med/2136 emerg/537 derm/846 ped/2811 oph/477 oph/695 |
| MeSH | D012859 |
| Orphanet | 378 |
全世界的發生率約1000分之1-4,台灣大約有9萬多名患者。乾燥症好發於40至60歲的中年婦女,男女比例為1:9,具有遺傳性,患有類風濕性關節炎、紅斑性狼瘡或硬皮症等自體免疫疾病的病人也容易合併乾燥症。
雖然確切的原因尚不清楚,但相信它涉及遺傳和環境的因素,如暴露於病毒或細菌[7]。此疾病可以獨立於其他健康問題(原發性乾燥症候群)或是另一種結締組織疾病的結果(繼發性乾燥症候群)[10]。發炎的結果逐漸傷害腺體[9],診斷是通過對腺體活體切片以及尋找特異性抗體的血液檢查[8]。 在活體切片中,腺體內通常有淋巴細胞[8]。
治療會針對患者的症狀進行[7]。對於乾眼病,可以嘗試人工淚液,減少發炎的藥物,淚點塞,或者關閉淚管的手術[7],對於口乾,可以使用口香糖(無糖為佳),啜飲水或唾液替代物[7]關節或肌肉疼痛的患者,可以使用布洛芬[7],可能導致乾燥的藥物,如抗組胺藥,也可能需進行停藥療法[7]。
瑞典眼科醫生亨里克·舍格倫在1933年首次描述這此新發現疾病,因而以他命名[11];然而,更早的紀錄已有描述罹患此症狀的病人[10]。人口中有0.2%到1.2%受到影響,一半是初級形式,一半是二級形式[9]。女性罹病比率是男性的十倍,通常在中年開始[8][10],但任何人都可能受到影響[8]。若無其他因抽血過多自體免疫性疾病,乾燥症候群不會影響預期壽命[12]。
現象及症狀
編輯原發性乾燥症候群[13](pSS)的標誌性組織學特徵是 T細胞、B細胞、漿細胞、巨噬細胞、肥大細胞和樹突狀細胞浸潤到淚腺和唾液腺中[14]。與健康人相比,pSS 患者的唾液腺表達獨特的細胞因子、黏附分子[15]和趨化因子[16]。90%以上患者都是以乾燥的症狀來表現,包括嘴乾、眼乾,比較嚴重時,嘴巴常出現潰瘍,眼睛部位亦可能發生角膜潰瘍。此外,身體各處的腺體皆可能受到侵犯導致乾燥的狀況發生,所以不但皮膚會乾燥,陰道也可能有乾燥的情形。乾燥症亦會造成全身性發炎反應,除了影響身體所有的腺體,其他器官也都會遭到侵犯,進而出現全身性的症狀,例如全身倦怠、無力、體重減輕,甚至失眠、憂鬱。
乾燥症還有可能會併發肺纖維化,這是容易被患者忽略的部分!如同許多其他自體免疫疾病,隨著疾病進展還有可能會侵犯到全身器官:肺臟、心臟、腎臟等。其中,當肺臟遭到攻擊時,可能出現間質性肺炎,倘若放任肺臟反覆發炎,便會形成許多纖維組織,進而導致肺纖維化,讓肺臟失去彈性,無法完成氣體交換的任務。自體免疫疾病引發的間質性肺病中,有約近三成會發展成漸進性纖維化間質性肺病(漸進性肺纖維化)[17] 。國外研究顯示,大概有二至七成的乾燥症患者,可能會侵犯到肺部,最嚴重的變化就是肺纖維化[18] 。很多病人都是到了肺纖維化比較嚴重以後才被發現,因此提醒乾燥症的病友務必提高警覺。。繼發性患者通常還會有和類風濕性疾病相關的病徵。
病因
編輯目前該疾病的具體成因仍然不清楚,據信與若干細胞表面水通道蛋白-5(AQP-5)的缺損有相關性。目前已知該疾病具有一定的遺傳基礎[19],即,具有或缺少某些基因的人群相對容易獲得此病。這些相關的基因在不同種族之間有一定的差異,例如HLA-DR53和日本人有關,而西歐人則與HLA-B8等有關[19]。此外,非洲淋巴細胞病毒(EB病毒)與原發性乾燥症候群具有一定的關聯性[19][20]。此外,巨細胞病毒以及HIV病毒也被認為與乾燥症候群有關[19]。該疾病屬於一種自體免疫性疾病,該病的患者其自身的免疫系統錯誤的對自身功能正常的細胞進行攻擊,並引發發炎。
檢驗
編輯由於乾燥症候群的症狀多樣,而且這些症狀與其它原因引起的某些症狀相似,因此其診斷比較複雜。然而,通過結合多種檢測手段,該疾病還是能得以檢測出來的。
血液檢查
編輯通過檢查血液中的抗體水平,如抗細胞核抗體(ANA)以及類風濕因子(因為類風濕疾病通常引發繼發性乾燥症候群),可以幫助判斷是否患有該病。如果結果過高則應當有所懷疑,因為這些指標和自體免疫性疾病有關。乾燥症候群患者抗細胞核抗體的典型情況為,抗Ro抗體(A型乾燥症候群抗體,SSA)及抗La抗體(B型乾燥症候群抗體,SSB)呈陽性。尤其是SSB/La更具有指標意義,因為SSA/Ro和許多其它自免疫疾病有關,儘管乾燥症候群的患者這一指標通常也不正常[21]。
淚腺功能測試
編輯淚液分泌試驗可以測量眼淚的分泌量水平:將一條試紙放置在下眼皮內側五分鐘,然後取出並用尺測量濕潤部分的長度。如果長度不足5毫米,則通常被認為有乾燥症候群。不過隨著年齡增大,或者是其它病況導致的淚腺功能退化,也可能有同樣的結果。還可以通過裂縫燈觀察眼睛表面來確認是否眼乾。
唾液腺功能測試
編輯和上面的淚液分泌試驗一樣,也可以用類似的方法測試唾液腺的功能是否正常。即,在五分鐘內收集分泌的唾液,測量其多少。也可以做一個唇部活檢,如果患有乾燥症候群,則可以發現在唾液分泌細胞周圍聚集著淋巴細胞,並因為發炎效應而遭受著破壞。
此外還可以對唾液腺進行超音波檢查。通過該檢查會發現,病患的腺體實質部分會有約2到6毫米大小的低回聲病變區,這些區域是遭受淋巴浸潤的區域。如果通過該項檢查發現唾液腺末梢導管呈點狀擴張,或者是出現結石,這通常表明該病已進入晚期。這種檢查方式的好處是簡單方便,不會對人體造成侵入性傷害,而且可以較為準確的發現症狀之間的關係。該檢查的另一個好處是可以發現相關併發症,例如若患有結外淋巴瘤,則可以看到1到4厘米大小的實質內團塊。
放射科的造影檢查也是一種有效且準確的檢測手段。該檢驗需要在拍片之前首先將顯影劑注入腮腺導管的主導管,該導管的兩端分別位於腮腺,以及第二顆上臼齒對應的口腔壁上。如果在腮腺部分發現有星點般大量散落的造影劑小點,則可以認定為乾燥症候群。
診斷
編輯新修訂的乾燥症候群診斷標準[22]要求同時存在跡象、病徵及實驗室檢驗結果才能確診。
病人報告的病徵必須同時包括眼部及口腔的病理現象,例如每天眼睛乾燥並持續三個月以上,以及如需要喝水才能咽下食物等。
而客觀的取證則包括前面提到的淚液分泌試驗以及玫瑰色染色法(或類似的其它染色法),同時組織病理學的檢查也應該顯示出小唾液腺焦點淋巴浸潤德情況。通過超音波診斷、檢測無刺激情況下的唾液分泌水平、腮腺造影或者唾液腺造影等檢測手段,可以獲得唾液腺的實際病情。
在診斷時,需要排除以下情況:曾對頭部及頸部進行過放射療法,處於淋巴癌早期,患有C型肝炎、愛滋病、結節病或者移植器官排斥等疾病,使用抗膽鹼藥物後未超過其四倍代謝時間等。
治療
編輯目前不存在能完全治癒乾燥症候群的療法,也不存在能夠一勞永逸地恢復分泌腺的分泌功能的療法。相反,目前的治療手段只是減輕症狀的支持療法。例如,停止三個月一次的抽血,停止服用過多藥物,食營替代藥品,對於眼睛乾燥的症狀,則使用人造淚水(眼藥水)來達到保持濕潤的效果。此外,環孢素(麗眼達眼用乳劑,一種免疫抑制劑)這種處方藥,可以用於治療慢性眼乾發炎。其原理是抑制淚腺處出現的發炎反應,這種發炎反應會削弱淚腺的功能,使其分泌眼淚的功能受到的干擾。對於唾液腺的問題也有類似的刺激唾液分泌的藥物,例如西維美林及匹羅卡品。非類固醇抗發炎藥則可以用於減輕肌肉及骨骼上的症狀。對於有其他嚴重併發症的病患,醫生可能會開出皮質類固醇或者其他的免疫抑制劑。而如甲氨喋呤等緩和類風濕疾病藥物也可能有一定幫助。目前,人們正在研究與該病有關的多種單株抗體[23]。
在該病的晚期階段,即便是使用了人造淚水,眼睛仍然感到如同火烤般乾燥,又癢又疼。病患時刻都能感受到各種折磨,尤其是在早上及傍晚時。用眼藥水不僅頻繁,而且還沒有太大的效果。此時可能需要使用特殊的護目鏡來增加局部的濕度,或者是在淚小管上塞入淚點塞來阻止眼淚從淚小管流失,以達到讓更多的淚水保持在眼部。這是因為人的上下眼皮各有一個淚管,上淚管流失淚水量約占通過該途徑流失總量的40%,餘下的60%通過下淚管排出。雖然上下淚管都可以放置淚點塞,但通常眼乾症患者只需阻塞下淚管,就足以延長眼淚留在眼睛上的時間。放置淚點塞得過程相當簡單,在驗光師或眼科醫生的辦公室內即可進行,整個過程只需要花幾分鐘的時間。通常第一次放置的是膠原蛋白材質的淚點塞,這種淚點塞在幾天的時間內就會被溶解。這一步驟是為了讓患者體體驗是否能適應該療法,儘管一般來說病情會得到立即改善。如果患者覺得沒有什麼不適,可以放置永久性的淚點塞。所謂永久性只是指不會被溶解,如果有必要,也是可以取出的[23]。
很多患者會忽略預防性的牙科治療,而這通常是很有必要的。由於缺乏唾液分泌,口腔的環境會變得有利於許多引起齲齒的細菌的大量繁殖。這些治療包括局部使用家用含氟產品以保護琺瑯質,以及定期到牙科診所對牙齒進行清潔。對已經存在的齲齒也需要儘快治療,因為齲齒在這種特定口腔環境下,很容易快速發展為深入到牙髓。一旦如此,將不能通過簡單的潔牙或者補牙等方式進行治療,而可能需要拔牙以及(或者)拔除牙齒神經,而這會給病患帶來更多的痛苦。因其他原因導致口乾燥病的患者也應該施以類似的治療。然而不幸的是,大部分患者都不了解需要這類治療,以至於當發現出現問題的時候,大部分牙齒已經無法得以保留。口乾燥病患者大部分牙齒都無法治療而只能拔除神經的情況,對於牙科醫生來說並不少見。這時候只能拔掉所有牙齒然後換上假牙,或者進行種牙手術。
在乾燥症併發肺纖維化的治療, 目前有一種抗肺纖維化藥物尼達尼布 (Nintedanib)已於多國獲得核准。該藥物除了用於治療過去已經取得適應症的特發性肺纖維化外,對於任何原因引起的肺部纖維化,若其纖維化病程持續進展 (如症狀、肺功能或肺纖維化範圍持續惡化),都可以使用此藥物來延緩疾病進展。這對於長年無法治療的自體免疫性疾病或其他成因引起的漸進性纖維化間質性肺病患者來說,帶來了希望。臨床試驗顯示,此藥物可減少57%的肺功能下降,並且在亞洲族群的次分析結果中顯示,可降低74%的急性惡化和死亡風險。[24]
預後
編輯乾燥症可能會損害關鍵器官,而症狀可能會緩和或者惡化。與其它自免疫疾病不同的是,這種疾病不會出現病情大幅減輕的情況。有些人可能只會感受到輕微的眼乾口燥,而另一些人可能會出現嚴重的症狀。儘管許多人可以通過治療緩解症狀,然而也有一些人只能夠選擇忍受視線變得模糊,持續性的眼部不舒適感覺,口腔的反覆感染,腮腺腫脹,喉嚨嘶啞以及難以吞咽等情況。甚至有些患者可能會出現腎臟疾病(自體免疫性腎小管間質性腎炎)並導致蛋白尿、尿崩症以及遠端腎小管性酸中毒。
乾燥症候群的患者,罹患非霍奇金淋巴瘤的概率,高於患有其它類型自免疫疾病及正常人[25],大約有5%的乾燥症候群患者會發展成某種惡性淋巴瘤[26]。尤其是有嚴重症狀的患者,患淋巴瘤的機率比症狀輕微至中等的患者要高[27]。其中最常見的是唾液腺外邊緣區b細胞淋巴瘤(唾液腺中的黏膜相關淋巴組織淋巴瘤)[25],以及瀰漫型大細胞性B細胞淋巴瘤[27]。
併發症
編輯約有2~7成的乾燥症患者 [18],亦容易會侵犯到肺臟、骨骼肌肉、腎臟與皮膚,其中關節炎與間質性肺炎是最常見併發症[28] 。需要特別留意的是,除了表徵症狀外,硬皮症、皮肌炎、紅斑性狼瘡、乾燥症、類風濕性關節炎等自體免疫疾病都有造成肺纖維化的風險,只是比例不依,有些疾病較容易導致肺纖維化,所以在確定診斷後,建議可進一步檢查肺部的狀況,並定期追蹤; 很多病患都是到了肺纖維化比較嚴重以後才被發現,因此建議乾燥症的病友務必對肺部症狀提高警覺,留意是否有持續的呼吸道症狀 (如喘、乾咳),定期追蹤肺功能、以胸部X光或高解析度電腦斷層掃描 (HRCT)檢查,以確保肺部健康,維持生活品質[17]。
除了前面所提到的各種併發症之外,患有乾燥症候群的女性如果懷孕,新生兒患有新生兒紅斑性狼瘡並伴有先天性心臟傳導阻滯(需要使用起搏器)的概率會相對較高[29]。
流行性學
編輯乾燥症候群在美國大約影響著一百萬至四百萬人的健康,有些人因賣血引發,而在中華人民共和國的普查則發現宣佈該病的患病率約為0.29%至0.77%[19]。
依據台灣調查,乾燥症候群為台灣第三大自體免疫性疾病,其中每十萬人盛行率為16人、發生率為10.6人[30] ,其中最常好發於 45 至 55 歲的女性,女性與男性的發病比率約為9.9:1[31]。
初次診斷時年齡超過40歲的女性,且女性患病的機率比男性高9倍。需要特別注意的是,這種疾病為病毒細菌環境引發,及服藥過多或抽血頻繁導致免疫系統失調,並不會傳染。
研究
編輯目前針對此病的研究集中在獲取有關該疾病的知識,了解引起生理失調的原因,改善診斷技術,以及尋找治療、預防甚至治癒該疾病的手段。
目前研究員對該疾病的建立了動物模型——通過使用60kD縮氨酸對實驗鼠進行免疫處理多天之後,可以觀察到與人類乾燥症候群非常相似的淋巴細胞浸潤以及唾液腺功能障礙情況[32][33]。
參見
編輯參考資料
編輯- ^ https://terms.naer.edu.tw/detail/ea5818c648edeb49aa4844eabd59a755/?seq=2
- ^ 存档副本. [2023-12-09]. (原始內容存檔於2023-12-09).
- ^ 存档副本 (PDF). [2023-12-09]. (原始內容存檔 (PDF)於2024-04-26).
- ^ https://webcache.googleusercontent.com/search?q=cache:JX-J1v1p-IAJ:https://www.tafm.org.tw/ehc-tafm/s/viewDocument%3FdocumentId%3De67f6b515b8f4afca8d17d0f94ac5157
- ^ 存档副本 (PDF). [2023-12-09]. (原始內容存檔 (PDF)於2023-08-11).
- ^ Rapini, Ronald P.; Bolognia, Jean L.; Jorizzo, Joseph L. Dermatology: 2-Volume Set. St. Louis: Mosby. 2007: 602–3. ISBN 1-4160-2999-0.
- ^ 7.0 7.1 7.2 7.3 7.4 7.5 7.6 7.7 What Is Sjögren's Syndrome? Fast Facts. NIAMS. November 2014 [15 July 2016]. (原始內容存檔於2016-07-04). (頁面存檔備份,存於網際網路檔案館)
- ^ 8.0 8.1 8.2 8.3 8.4 8.5 Brito-Zerón, P; Baldini, C; Bootsma, H; Bowman, SJ; Jonsson, R; Mariette, X; Sivils, K; Theander, E; Tzioufas, A; Ramos-Casals, M. Sjögren syndrome.. Nature Reviews. Disease Primers. 7 July 2016, 2: 16047. PMID 27383445. doi:10.1038/nrdp.2016.47.
- ^ 9.0 9.1 9.2 John H., Klippel. Primer on the rheumatic diseases 13th. New York, NY: Springer. 2008: 389 [15 July 2016]. ISBN 9780387685663. (原始內容存檔於2016-08-15). (頁面存檔備份,存於網際網路檔案館)
- ^ 10.0 10.1 10.2 Ng, Wan-Fai. Sjogren's Syndrome. Oxford University Press. 2016: 10–11 [2018-01-18]. ISBN 9780198736950. (原始內容存檔於2016-08-15). (頁面存檔備份,存於網際網路檔案館)
- ^ Sjögren H. Zur Kenntnis der keratoconjunctivitis sicca. Doctoral thesis, 1933.
- ^ Singh, AG; Singh, S; Matteson, EL. Rate, risk factors and causes of mortality in patients with Sjögren's syndrome: a systematic review and meta-analysis of cohort studies.. Rheumatology (Oxford, England). March 2016, 55 (3): 450–60. PMID 26412810. doi:10.1093/rheumatology/kev354.
- ^ 向釗,楊靜. 原發性乾燥症候群代謝組學研究進展[J]. 中國醫師雜誌,2023,25(02):300-303.DOI:10.3760/cma.j.cn431274-20220520-00479
- ^ Psianou, Konstantia; Panagoulias, Ioannis; Papanastasiou, Anastasios D.; de Lastic, Anne-Lise; Rodi, Maria; Spantidea, Panagiota I.; Degn, Søren E.; Georgiou, Panagiotis; Mouzaki, Athanasia. Clinical and immunological parameters of Sjögren's syndrome. Autoimmunity Reviews. 2018-10, 17 (10) [2024-01-26]. doi:10.1016/j.autrev.2018.05.005. (原始內容存檔於2024-06-10) (英語).
- ^ 存档副本. [2024-01-29]. (原始內容存檔於2024-01-29).
- ^ Hansen, Arne; Reiter, Karin; Ziprian, Till; Jacobi, Annett; Hoffmann, Andreas; Gosemann, Mirko; Scholze, Jürgen; Lipsky, Peter E.; Dörner, Thomas. Dysregulation of chemokine receptor expression and function by B cells of patients with primary Sjögren's syndrome. Arthritis & Rheumatism. 2005-07, 52 (7). ISSN 0004-3591. doi:10.1002/art.21129 (英語).
- ^ 17.0 17.1 Wijsenbeek, Marlies; Kreuter, Michael; Olson, Amy; Fischer, Aryeh; Bendstrup, Elisabeth; Wells, Christopher D.; Denton, Christopher P.; Mounir, Baher; Zouad-Lejour, Leila; Quaresma, Manuel; Cottin, Vincent. Progressive fibrosing interstitial lung diseases: current practice in diagnosis and management. Current Medical Research and Opinion. 2019-11, 35 (11) [2023-06-08]. ISSN 1473-4877. PMID 31328965. doi:10.1080/03007995.2019.1647040. (原始內容存檔於2023-06-09).
- ^ 18.0 18.1 Wang, Yong; Hou, Ziliang; Qiu, Meihua; Ye, Qiao. Risk factors for primary Sjögren syndrome-associated interstitial lung disease. Journal of Thoracic Disease. 2018-04, 10 (4) [2023-06-08]. ISSN 2072-1439. PMC 5949459 . PMID 29850114. doi:10.21037/jtd.2018.03.120. (原始內容存檔於2023-06-09).
- ^ 19.0 19.1 19.2 19.3 19.4 王剛玉; 馬建華. 干燥综合征的消化系统表现. 《中國社區醫師》. 2009年1月, 11–2. [永久失效連結]
- ^ 賀聯印; 王京華、王申五、楊鐵生、杜紹財、樊春紅. EB病毒与干燥综合征发病相关性的研究. 《中華醫學雜誌》. 1994年2月, 2. (原始內容存檔於2022-05-11).
「結果說明乾燥症候群患者EB病毒感染率較正常人明顯增高,且EB病毒感染與靶器官的損害有關,提示靶器官控制EB病毒細胞內複製的免疫機制出現異常。」
(頁面存檔備份,存於網際網路檔案館) - ^ Franceschini F, Cavazzana I. Anti-Ro/SSA and La/SSB antibodies. Autoimmunity. February 2005, 38 (1): 55–63. PMID 15804706. doi:10.1080/08916930400022954.
- ^ Vitali, C.; Bombardieri, S.; Jonsson, R.; Moutsopoulos, H. M.; Alexander, E. L.; Carsons, S. E.; Daniels, T. E.; Fox, P. C.; Fox, R. I. Classification criteria for Sjögren9s syndrome: a revised version of the European criteria proposed by the American-European Consensus Group. Annals of the Rheumatic Diseases. 2002-06-01, 61 (6): 554–558 [2017-07-05]. ISSN 0003-4967. PMC 1754137 . PMID 12006334. doi:10.1136/ard.61.6.554. (原始內容存檔於2020-10-23) (英語). (頁面存檔備份,存於網際網路檔案館)
- ^ 23.0 23.1 Dr. J. Parks, Ancaster ON Canada
- ^ Flaherty, Kevin R.; Wells, Athol U.; Cottin, Vincent; Devaraj, Anand; Walsh, Simon L.F.; Inoue, Yoshikazu; Richeldi, Luca; Kolb, Martin; Tetzlaff, Kay; Stowasser, Susanne; Coeck, Carl. Nintedanib in Progressive Fibrosing Interstitial Lung Diseases. New England Journal of Medicine. 2019-10-31, 381 (18) [2023-06-08]. ISSN 0028-4793. doi:10.1056/NEJMoa1908681. (原始內容存檔於2023-06-09) (英語).
- ^ 25.0 25.1 Voulgarelis M, Skopouli FN. Clinical, immunologic, and molecular factors predicting lymphoma development in Sjogren's syndrome patients. Clin Rev Allergy Immunol. 2007, 32 (3): 265–74. PMID 17992593. doi:10.1007/s12016-007-8001-x.
- ^ Tzioufas AG, Voulgarelis M. Update on Sjögren's syndrome autoimmune epithelitis: from classification to increased neoplasias. Best Pract Res Clin Rheumatol. 2007, 21 (6): 989–1010. PMID 18068857. doi:10.1016/j.berh.2007.09.001.
- ^ 27.0 27.1 Smedby KE, Baecklund E, Askling J. Malignant lymphomas in autoimmunity and inflammation: a review of risks, risk factors, and lymphoma characteristics. Cancer Epidemiol. Biomarkers Prev. 2006, 15 (11): 2069–77. PMID 17119030. doi:10.1158/1055-9965.EPI-06-0300.
- ^ Ramos-Casals, Manuel; Brito-Zerón, Pilar; Seror, Raphaèle; Bootsma, Hendrika; Bowman, Simon J.; Dörner, Thomas; Gottenberg, Jacques-Eric; Mariette, Xavier; Theander, Elke; Bombardieri, Stefano; De Vita, Salvatore. Characterization of systemic disease in primary Sjögren's syndrome: EULAR-SS Task Force recommendations for articular, cutaneous, pulmonary and renal involvements. Rheumatology (Oxford, England). 2015-12, 54 (12) [2023-06-08]. ISSN 1462-0332. PMC 6281074 . PMID 26231345. doi:10.1093/rheumatology/kev200. (原始內容存檔於2023-06-09).
- ^ Manthorpe R, Svensson A, Wirestrand LE. Late neonatal lupus erythematosus onset in a child born of a mother with primary Sjögren's syndrome. Ann. Rheum. Dis. November 2004, 63 (11): 1496–7. PMC 1754813 . PMID 15479901. doi:10.1136/ard.2003.014944.
- ^ Yu, Kuang-Hui; See, Lai-Chu; Kuo, Chang-Fu; Chou, I.-Jun; Chou, Meng-Jiun. Prevalence and incidence in patients with autoimmune rheumatic diseases: a nationwide population-based study in Taiwan. Arthritis Care & Research. 2013-02, 65 (2) [2023-06-08]. ISSN 2151-4658. PMID 22899470. doi:10.1002/acr.21820. (原始內容存檔於2023-06-09).
- ^ WENG, MENG-YU; HUANG, YU-TUNG; LIU, MING-FEI; LU, TSUNG-HSUEH. Incidence and Mortality of Treated Primary Sjögren’s Syndrome in Taiwan: A Population-based Study. The Journal of Rheumatology. 2011-01-15, 38 (4). ISSN 0315-162X. doi:10.3899/jrheum.100883.
- ^ Scofield RH, Asfa S, Obeso D, Jonsson R, Kurien BT. Immunization with short peptides from the 60-kDa Ro antigen recapitulates the serological and pathological findings as well as the salivary gland dysfunction of Sjögren's syndrome. J Immunol. 2005, 175 (12): 8409–14. PMID 16339583. doi:10.1007/s12016-007-8001-x.
- ^ Kurien BT, Asfa S, Li C, Dorri Y, Jonsson R, Scofield RH. Induction of oral tolerance in experimental Sjögren's syndrome autoimmunity. Scand J Immunol. 2005, 61 (5): 418–25. PMID 15882433. doi:10.1111/j.1365-3083.2005.01593.x.
外部連結
編輯- 本文的原始文本取自於公共領域資源:
- www.ninds.nih.gov/health_and_medical/disorders/sjogrens_doc (頁面存檔備份,存於網際網路檔案館)
- Sjögren's Syndrome Foundation
- Role of MHC Class II Molecules in the Development of Sjögren’s Syndrome in the NOD Mouse
- Sjögren's Syndrome article by Mayo Clinic staff (頁面存檔備份,存於網際網路檔案館)
- Sjögren's Syndrome International Collaborative Clinical Alliance (SICCA) (頁面存檔備份,存於網際網路檔案館)
- Green tea may help prevent autoimmune diseases. Medical College of Georgia. April 18, 2007 [2007-04-20]. (原始內容存檔於2010-06-16). (頁面存檔備份,存於網際網路檔案館)