钆特酸
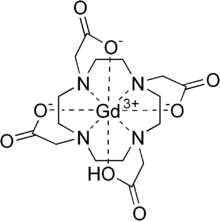
钆特酸(INN:gadoteric acid,简写Ga-DOTA),为钆离子(Ga3+)的大环配体DOTA形成的螯合物。在医学上是一种钆造影剂(gadolinium-based contrast agents,GBCA),属大环离子型造影剂,用于磁共振成像造影[2]。其动力学稳定常数,是已知稳定常数和解离半衰期最大的螯合物[3][4]。
 | |
| 临床资料 | |
|---|---|
| 商品名 | Artirem, Dotarem(多它灵), Clariscan等[1] |
| 其他名称 | DOTA-Gd,Gd-DOTA, Gadoterate meglumine(钆特酸葡胺) (USAN US) |
| 给药途径 | 静脉注射 |
| ATC码 | |
| 法律规范状态 | |
| 法律规范 |
|
| 药物动力学数据 | |
| 血浆蛋白结合率 | 几乎无 |
| 药物代谢 | 几乎无 |
| 生物半衰期 | 约90分钟(血浆) 2-3分钟(分布) |
| 排泄途径 | 原体药物经肾,极少部分经粪便排出 |
| 识别信息 | |
| |
| CAS号 | 72573-82-1 |
| PubChem CID | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| 化学信息 | |
| 化学式 | C16H25GdN4O8 |
| 摩尔质量 | 558.65 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
医学上常以其葡甲胺盐的形式,即钆特酸葡胺(USAN:Gadoterate meglumine)进行注射给药[5][6]。
历史
编辑钆特酸由法国加柏公司(Guerbet)研制开发,以商品名Dotarem(多它灵)于1989年获准在法国上市,2013年3月20日通过美国FDA批准用于MRI造影[7]。
医学用途
编辑钆特酸中心离子Ga3+具有强顺磁性,可缩短磁共振(MRI)中T1弛豫时间,形成像衬度,为阳性造影剂。但高浓度下T2弛豫时间缩短占优为阴性造影剂,高浓度常用于动脉期血管造影[2]。
其被批准用于2岁以上患者的全身MRI检查,可用于大脑、脊髓以及血管检查。其本身无法透过血脑屏障,但大脑血管发生病变部分则可透过血脑屏障,因此可识别脑部肿瘤[8]。其以钆特酸葡胺注射液形式进行静脉注射,药物可在身体中存在数年[5][6]。
药理学
编辑钆特酸和第一代MRI造影剂马根维显理化性能和临床应用相似。经静脉注射后,钆特酸先经血管扩散,然后迅速扩散细胞外空间。钆特酸通过肾脏以原体药物排泄,少部分分泌到肠胃道经粪便排出。钆特酸非选择性地分布在所有脑外组织的细胞外空间中,无器官特异性。钆特酸蛋白质结合力非常低因此通过肾脏相对较快地排泄。[2]
风险
编辑钆特酸作为含钆制剂,体外研究表明其具有的神经毒性,但相比于线性钆螯合物,作为大环螯合物的钆特酸相比风险更低[9][10]。在标准用量下,在大脑可检测到药物残留[11]。
同时具有肾源性系统纤维化(Nephrogenic systemic fibros,NSF)风险,但目前未有相关案例报道,因此不适用于肾功能受损患者[12][13]。
合成
编辑由DOTA与氢氧化钆先在80摄氏度螯合12小时,再用氨水室温下碱化使pH=11即得到钆特酸Ga-DOTA。
钆特酸进一步与葡萄糖和甲胺还原胺化得到的葡甲胺1:1混合成盐,即可得到钆特酸葡胺[14][15]。
参考文献
编辑- ^ Gadoteric Acid International. Drugs.com. 6 January 2021 [21 January 2021]. (原始内容存档于2019-08-17).
- ^ 2.0 2.1 2.2 2.3 何国祥; 王毅翔. 造影剂药理学及临床应用. 上海: 上海科学技术出版社. 2002. ISBN 7532362264.
- ^ P Caravan, JJ Ellison, TJ McMurry, RB Lauffer. Gadolinium (III) chelates as MRI contrast agents: structure, dynamics, and applications. Chemical Reviews. 1999, 99: 2293−2352. doi:10.1021/cr980440x.
- ^ Herborn, Christoph U. MD; Honold, Elmar MD; Wolf, Michael; Kemper, Jörn MD; Kinner, Sonja MD; Adam, Gerhard MD; Barkhausen, Jörg MD. Clinical Safety and Diagnostic Value of the Gadolinium Chelate Gadoterate Meglumine (Gd-DOTA). Investigative Radiology. 2007, 42 (1): 58–62. doi:10.1097/01.rli.0000248893.01067.e5.
- ^ 5.0 5.1 Dotarem- gadoterate meglumine injection. DailyMed. [29 August 2021]. (原始内容存档于2024-12-06).
- ^ 6.0 6.1 Clariscan- gadoterate meglumine injection, solution. DailyMed. [29 August 2021]. (原始内容存档于2024-12-12).
- ^ Hollmer M. Dotarem: A safe(r) gadolinium-based contrast imaging agent. FierceBiotech. 6 January 2014 [2024-06-25]. (原始内容存档于2021-08-21).
- ^ DrugBank (编). Gadoteric acid. DrugBank. 22 August 2016 [2024-06-25]. (原始内容存档于2019-08-17).
- ^ Bower DV, Richter JK, von Tengg-Kobligk H, Heverhagen JT, Runge VM. Gadolinium-Based MRI Contrast Agents Induce Mitochondrial Toxicity and Cell Death in Human Neurons, and Toxicity Increases With Reduced Kinetic Stability of the Agent. Investigative Radiology. August 2019, 54 (8): 453–463 [2024-06-25]. PMID 31265439. S2CID 164486744. doi:10.1097/RLI.0000000000000567. (原始内容存档于2024-12-13).
- ^ Alexander Radbruch , Lukas D. Weberling, Pascal J. Kieslich, Oliver Eidel, Sina Burth, Philipp Kickingereder, Sabine Heiland, Wolfgang Wick, Heinz-Peter Schlemmer, Martin Bendszus. Gadolinium Retention in the Dentate Nucleus and Globus Pallidus Is Dependent on the Class of Contrast Agent. RADIOLOG. 2015, 275 (3): 783–791. doi:10.1148/radiol.2015150337.
- ^ Stanescu AL, Shaw DW, Murata N, Murata K, Rutledge JC, Maloney E, et al. Brain tissue gadolinium retention in pediatric patients after contrast-enhanced magnetic resonance exams: pathological confirmation. Pediatric Radiology. March 2020, 50 (3): 388–396. PMID 31989188. S2CID 210913930. doi:10.1007/s00247-019-04535-w.
- ^ Todd DJ, Kay J. Gadolinium-Induced Fibrosis. Annual Review of Medicine. 2016, 67: 273–91. PMID 26768242. doi:10.1146/annurev-med-063014-124936.
- ^ Csilla Balassy, Donna Roberts, Stephen F. Miller3. Safety and efficacy of gadoteric acid in pediatric magnetic resonance imaging: overview of clinical trials and post-marketing studies. Pediatr Radiol. 2015, 45: 1831–1841. doi:10.1007/s00247-015-3394-9.
- ^ S KauráLuthra, V MorissonáIveson, NE Felicity, J Nicholas. Gd 3+ cFLFLFK conjugate for MRI: a targeted contrast agent for FPR1 in inflammation. Chemical communications. 2013, 49 (6): 564–566. doi:10.1039/C2CC37460A.
- ^ 韩晓丹,郭春. 钆特酸葡甲胺. 中国药物化学杂志. 2013, 23 (5): 1.
