磷酸
磷酸(英語:phosphoric acid)或稱為正磷酸(英語:Orthophosphoric acid),化學式,是一種常見的無機酸,不易揮發,不易分解,幾乎沒有氧化性。具有酸的通性,是三元弱酸,其酸性比鹽酸、硫酸、硝酸弱,但比醋酸、硼酸等強。由五氧化二磷溶於熱水中即可得到。正磷酸工業上用硫酸處理磷灰石即得。用硝酸使磷氧化,可以得到較純的磷酸;一般是83%-98%的稠厚溶液,如果再濃縮,可以得到無色晶體。磷酸在空氣中容易潮解;加熱會逐漸失水得到焦磷酸,進一步失水得到偏磷酸。磷酸容易自行結合成多種化合物如焦磷酸(pyrophosphoric acid)或三聚磷酸(triphosphoric acid)等。
| 磷酸 | |
|---|---|
| |

| |

| |
| IUPAC名 trihydroxidooxidophosphorus phosphoric acid | |
| 別名 | 正磷酸、原磷酸 |
| 識別 | |
| CAS號 | 7664-38-2 16271-20-8(半水化合物) |
| PubChem | 1004 |
| ChemSpider | 979 |
| SMILES |
|
| InChI |
|
| InChIKey | NBIIXXVUZAFLBC-UHFFFAOYAI |
| UN編號 | 1805 |
| EINECS | 231-633-2 |
| ChEBI | 26078 |
| RTECS | TB6300000 |
| KEGG | D05467 |
| 性質 | |
| 化學式 | H3PO4 |
| 摩爾質量 | 97.995 g·mol⁻¹ |
| 外觀 | 白色固體或黏稠液體(>42 °C) |
| 密度 | 1.885 g/mL (液態) 1.685 g/mL (85%水溶液) 2.030 g/mL (25°C晶體) |
| 熔點 | 42.35 °C (無水化合物) 29.32 °C (半水化合物) |
| 沸點 | 158 °C(分解) |
| 溶解性(水) | 5.48 g/mL |
| pKa | 2.148, 7.198, 12.319 |
| 黏度 | 2.4–9.4 cP (85% aq. soln.) 147 cP (100%) |
| 熱力學 | |
| ΔfHm⦵298K | -1288 kJ·mol−1[1] |
| S⦵298K | 158 J·mol−1·K−1[1] |
| 危險性 | |
| 歐盟危險性符號 | |
| 警示術語 | R:R34 |
| 安全術語 | S:S1/2-S26-S45 |
| MSDS | ICSC 1008 |
| 歐盟編號 | 015-011-00-6 |
| NFPA 704 | |
| 閃點 | 不可燃 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
除了用作化學試劑之外,磷酸也可主要用於製藥、鐵銹轉化劑、食品添加物、溶劑、電解液、肥料、冶金、飼料等,也有在醫學美容及牙科的用途。
磷酸為三元酸,可解離出三個氫離子,因此可形成三種不同的酸根,分別是:磷酸二氫根H2PO4−、磷酸氫根HPO2−
4以及磷酸根PO3−
4。
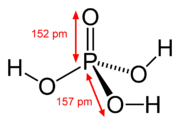
結構
編輯以磷為中心、四個氧環繞其周圍,其中包括一個雙鍵氧和三個羥基。三個可解離的氫原子分別與三個氧原子結合。
化學性質
編輯純磷酸的無水化合物在室溫下為白色晶體,熔點42.35 °C,溶化後為黏稠液體。
正磷酸具有極大的極性,因此磷酸極易溶於水。
正磷酸的中心磷(P)的氧化數為+5,而周圍氧原子(O)的氧化數為-2,氫離子為+1。
磷酸為無毒性的無機物,是一種三元弱酸。三元酸的意思是可在水中解離出三顆H+的酸性物質,磷酸的解離過程如下:Ka1、Ka2和Ka3為化學式在25°C下的解離常數
- H3PO4(s) + H2O(l) ⇌H3O+(aq) + H2PO4−(aq) Ka1= 7.11×10−3
- H2PO4−(aq)+ H2O(l) ⇌H3O+(aq) + HPO42−(aq) Ka2= 6.32×10−8
- HPO42−(aq)+ H2O(l) ⇌ H3O+(aq) + PO43−(aq) Ka3= 4.49×10−13
由於磷酸的多元酸性質,使它的pH值幅度較大,造成它的緩衝現象。又由於其無毒性又容易取得,實驗室及工業常拿無毒磷酸鹽與弱酸(如檸檬酸)混合物作為緩衝溶液,
磷酸時廣泛存在於生物體中,特別是磷酸化醣類,如DNA、RNA以及ATP。
如果將正磷酸加熱,數個磷酸分子的單體會脫水聚合起來,如:
兩個磷酸相連脫去一個水,形成焦磷酸(pyrophosphoric acid, )
如果數個磷酸環狀相接起來,並脫去一分子水,會形成偏磷酸(metaphosphoric acid),通式為:(HPO3)n。中文命名為n偏磷酸(n≥3)。[2]偏磷酸是一種具脫水性的物質,因此常被用作乾燥劑。要進一步將偏磷酸脫水相當困難,需使用極強的脫水劑搭配加熱(單純加熱無效),才可將偏磷酸脫水形成磷酸酐(五氧化二磷,phosphorus pentoxide,化學式: ,分子式:P4O10),磷酸酐具有極強的脫水性,可用作酸性物質的乾燥劑。
若在超強酸(superacids,比H2SO4還強的酸)中作用,磷酸會形成理論上具腐蝕性的酸性物質,四羥基合鏻離子(tetrahydroxylphosphoniumion)。以氟銻酸(fluoroantimonic acid, )作超強酸為例:
- H3PO4 + HSbF6 → [P(OH)4+][SbF6]−
水溶液
編輯磷酸濃度的計算方法([A]為莫耳濃度)[A] = [H3PO4] + [H2PO4−] + [HPO42−] + [PO43−]
下表是磷酸在不同濃度下的pH、及磷酸的各共軛鹼濃度。
| [A] (mol/L) | pH | [H3PO4]/[A] (%) | [H2PO4−]/[A] (%) | [HPO42−]/[A] (%) | [PO43−]/[A] (%) |
|---|---|---|---|---|---|
| 1 | 1.08 | 91.7 | 8.29 | 6.20×10−6 | 1.60×10−17 |
| 10−1 | 1.62 | 76.1 | 23.9 | 6.20×10−5 | 5.55×10−16 |
| 10−2 | 2.25 | 43.1 | 56.9 | 6.20×10−4 | 2.33×10−14 |
| 10−3 | 3.05 | 10.6 | 89.3 | 6.20×10−3 | 1.48×10−12 |
| 10−4 | 4.01 | 1.30 | 98.6 | 6.19×10−2 | 1.34×10−10 |
| 10−5 | 5.00 | 0.133 | 99.3 | 0.612 | 1.30×10−8 |
| 10−6 | 5.97 | 1.34×10−2 | 94.5 | 5.50 | 1.11×10−6 |
| 10−7 | 6.74 | 1.80×10−3 | 74.5 | 25.5 | 3.02×10−5 |
| 10−10 | 7.00 | 8.24×10−4 | 61.7 | 38.3 | 8.18×10−5 |
鑑別
編輯可以使用硝酸銀和蛋白質對正、偏、焦磷酸進行鑑別。硝酸銀可以與正磷酸生成黃色的磷酸銀沉澱,而與焦磷酸、偏磷酸生成白色沉澱,但偏磷酸能使蛋白沉澱。[3]
製備
編輯磷酸有三種製備方法,加熱法(thermal process)、潮濕製造法(wet process)及乾窯法(dry kiln process)
加熱法
編輯燃燒磷單質產生五氧化二磷並且溶於水產生磷酸。此方法可生產較純的磷酸,因為在煉製磷的過程中已經去除許多雜質,然而仍需去除藏在裏面的砷。 純磷的現代製法大部分是將磷酸鈣與砂(主要成分為二氧化矽)及焦炭一起放在電爐中加熱。化學式如下:
潮濕製造法
編輯反應:(X為鹵素)
硫酸鈣溶解度較小,因此可以被過濾掉。
以此方法最初製造出來的磷酸濃度大約含有23%至33%的 ,再進行蒸餾或稀釋調整成想要的濃度。商品級的磷酸約54%,而超磷酸的濃度約70%.[4][5]
用途
編輯性質
編輯濃磷酸約75–85%左右,為澄清、無色、無味、非揮發性的濃稠液體。磷酸雖然無毒性,但85%的濃磷酸具有腐蝕性。
在如此高的濃度下,濃磷酸中的磷酸分子會聚合起來形成聚磷酸。
與鹵化物的反應
編輯磷酸與鹵化物會產生氫鹵化物氣體,在實驗室可以此法製備鹵化氫。
NaCl(s) + H3PO4(l) → NaH2PO4(s) + HCl(g) NaBr(s) + H3PO4(l) → NaH2PO4(s) + HBr(g) NaI(s) + H3PO4(l) → NaH2PO4(s) + HI(g)
鐵銹轉化劑
編輯磷酸可作為鐵銹轉化劑的成分,磷酸可將紅棕色的Fe2O3轉為黑色的FePO4,予以剝除後可露出新的金屬面,也可暫不進行剝除,讓他作為金屬面的保護層,防止其進一步的氧化。
鐵銹轉化劑有時被配置成液體供金屬浸泡。有時被配置成凝膠狀,暱稱「海軍果醬(naval jelly)」,可塗抹在垂直或陡峭的斜面上。
食品添加劑
編輯藥用
編輯磷酸也被應用於牙科及美容上。牙科方面,磷酸可用於清潔牙面及牙齒美白。
磷酸也被添加於防暈藥。
其他應用
編輯除了以上的應用外,磷酸還有下列用途:
- 含有磷-31的磷酸可作為核磁共振的外標物
- 高性能液相色譜法
- 溫氏法(Wentworth Process):作為活性碳的氧化劑。[7]
- 磷酸燃料電池中的電解液。
- 作為烯烴和水加成的催化劑以製造醇類。
- 作為銅電鍍拋光的電解液。
- 作為助焊劑
- 在半導體製程當中,磷酸可做為蝕刻的溶劑,例如:磷酸與過氧化氫的混合物可將InGaAs轉為InP,達到蝕刻的目的[8]。
- 蝕刻氮化矽,磷酸可將Si3N4轉化為SiO2。[9]
- 做為緩衝溶液。
- 作為皮革處理及洗滌劑的分散媒。
- 作為保養品中pH值的調節劑[10]。
- 建築業上用磷酸以移除礦物沉積物、水泥圖片及水漬。
- 水耕法中用作pH值的調節劑,也可作為植物磷養分的直接來源。
- 水族箱中,使用磷酸作為消除綠斑藻的工具,以及有利於水草生長
生物學影響
編輯飲料添加物
編輯磷酸用在食品添加劑,素來有骨質疏鬆症的疑慮。以往的調查是藉由問卷選填飲用可樂及其他碳酸飲料的頻率,發現飲用碳酸飲料的受試者較易有骨質疏鬆症的問題。研究指出,飲用碳酸飲料者沒有比其他人攝取更多的磷,但身體的鈣磷比卻顯著的降低。《美國臨床營養學雜誌》(American Journal of Clinical Nutrition)中的有項研究[11]在1996年至2001年使用雙倍能量的X光去探測1672位女性及1148位男性的骨密度,發現磷酸確實會降低骨密度,此研究提供了比以往使用問卷調查更有利的證據。
另一項臨床研究指出,磷的攝取會降低骨密度。但此實驗以磷的總攝取量為主,並未明確證明使骨密度降低的主因是磷酸。[12]
但在Heaney及Rafferty使用鈣平衡的方法對於20至40歲的女人一日習慣飲用三杯以上(680 ml)碳酸飲料進行的臨床研究,卻發現含磷酸的碳酸飲料與鈣流失無關。[13]研究比較了水、牛奶以及各種非酒精飲料(兩種含咖啡因,兩種不含咖啡因,兩種含磷酸,兩種含檸檬酸)。他們發現,相較於水,只有牛奶以及另外兩項含有咖啡因的飲品會增加尿液中的鈣含量,而添加有磷酸的咖啡因飲料和含咖啡因的飲料鈣量流失速度差不多,並沒有擴大咖啡因造成流失鈣質的影響。由於研究顯示咖啡因所造成的鈣質流失會逐漸補回來[14],而磷酸在實驗中又沒有對鈣質流失造成影響。Heaney及Rafferty認為前面實驗受試者骨質疏鬆的原因是受試者飲用碳酸飲料,造成牛奶攝取量的漸少,造成鈣攝取量不足。
參見
編輯參考文獻
編輯- ^ 1.0 1.1 Zumdahl, Steven S. Chemical Principles 6th Ed.. Houghton Mifflin Company. 2009: A22. ISBN 0-618-94690-X.
- ^ acid The Columbia Encyclopedia, Sixth Edition.
- ^ 北京師範大學無機化學教研室等編. 第四版 下冊
- ^ Thomas, W P and Lawton, W S "Stable ammonium polyphosphate liquid fertilizer from merchant grade phosphoric acid" 美國專利第4,721,519號, Issue date: January 26, 1988
- ^ Super Phosphoric Acid 0-68-0 Material Safety Data Sheet (PDF). J.R. Simplot Company. May 2009 [4 May 2010]. (原始內容 (PDF)存檔於2011年7月16日).
- ^ Current EU approved additives and their E Numbers. Foods Standards Agency. 14 March 2012 [22 July 2012]. (原始內容存檔於2013-07-19).
- ^ Toles, C.; Rimmer, S.; Hower, J.C. Production of activated carbons from a washington lignite using phosphoric acid activation. Carbon (Elsevier BV). 1996, 34 (11): 1419–1426. ISSN 0008-6223. doi:10.1016/s0008-6223(96)00093-0.
- ^ Wet chemical etching. (頁面存檔備份,存於互聯網檔案館) umd.edu
- ^ Wolf, S.; R.N. Tauber. Silicon processing for the VLSI era: Volume 1 – Process technology. 1986: 534. ISBN 0-9616721-6-1.
- ^ Ingredient dictionary: P. Cosmetic ingredient dictionary. Paula's Choice. [16 November 2007]. (原始內容存檔於2008年1月18日).
- ^ Katherine L. Tucker, Kyoko Morita, Ning Qiao, Marian T. Hannan, L. Adrienne Cupples, Douglas P. Kiel. Colas, but not other carbonated beverages, are associated with low bone mineral density in older women: The Framingham Osteoporosis Study. The American Journal of Clinical Nutrition. 2006-10, 84 (4): 936–942 [2019-05-25]. ISSN 0002-9165. PMID 17023723. doi:10.1093/ajcn/84.4.936. (原始內容存檔於2019-06-27).
- ^ S. Elmståhl, B. Gullberg, L. Janzon, O. Johnell, B. Elmståhl. Increased incidence of fractures in middle-aged and elderly men with low intakes of phosphorus and zinc. Osteoporosis international: a journal established as result of cooperation between the European Foundation for Osteoporosis and the National Osteoporosis Foundation of the USA. 1998, 8 (4): 333–340 [2019-05-25]. ISSN 0937-941X. PMID 10024903. doi:10.1007/s001980050072. (原始內容存檔於2019-10-11).
- ^ R. P. Heaney, K. Rafferty. Carbonated beverages and urinary calcium excretion. The American Journal of Clinical Nutrition. 2001-9, 74 (3): 343–347 [2019-05-25]. ISSN 0002-9165. PMID 11522558. doi:10.1093/ajcn/74.3.343. (原始內容存檔於2019-09-27).
- ^ M. J. Barger-Lux, R. P. Heaney, M. R. Stegman. Effects of moderate caffeine intake on the calcium economy of premenopausal women. The American Journal of Clinical Nutrition. 1990-10, 52 (4): 722–725 [2019-05-25]. ISSN 0002-9165. PMID 2403065. doi:10.1093/ajcn/52.4.722. (原始內容存檔於2019-09-20).
外部連結
編輯- International chemical safety card 1008 (頁面存檔備份,存於互聯網檔案館)
- National pollutant inventory – Phosphoric acid fact sheet (頁面存檔備份,存於互聯網檔案館)
- NIOSH Pocket guide to chemical hazards (頁面存檔備份,存於互聯網檔案館)
- Excel spreadsheet containing phosphoric acid titration curve, distribution diagram and buffer pH calculation (頁面存檔備份,存於互聯網檔案館)


