雷尼替丁
雷尼替丁(ranitidine、中华药典名:雷尼替定[1])又译雷尼得定[2],常用商品名Zantac,是一种抑制胃酸[3]产生的组胺类H2受体阻抗剂。它常用于治疗消化性溃疡(如胃溃疡和十二指肠溃疡)以及胃食管反流病。此外,该药或许还能改善荨麻疹的症状[4]。本品可经口服、肌肉注射,或静脉注射给药[3] 。
 | |
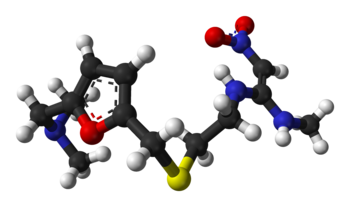 | |
| 临床资料 | |
|---|---|
| 读音 | /rəˈnɪtɪdiːn/ |
| 商品名 | Zantac, others |
| 其他名称 | Dimethyl [(5-{[(2-{[1-(methylamino)- 2-nitroethenyl]amino}ethyl)sulfanyl] methyl}furan-2-yl)methyl]amine |
| AHFS/Drugs.com | Monograph |
| MedlinePlus | a601106 |
| 核准状况 |
|
| 怀孕分级 |
|
| 给药途径 | 口服、静脉滴注 |
| ATC码 | |
| 法律规范状态 | |
| 法律规范 | |
| 药物动力学数据 | |
| 生物利用度 | 39 to 88% |
| 药物代谢 | 肝脏 |
| 生物半衰期 | 2–3 小时 |
| 排泄途径 | 30–70% 肾脏 |
| 识别信息 | |
| |
| CAS号 | 66357-35-5 |
| PubChem CID | |
| IUPHAR/BPS | |
| DrugBank | |
| ChemSpider | |
| UNII | |
| KEGG | |
| ChEBI | |
| ChEMBL | |
| CompTox Dashboard (EPA) | |
| ECHA InfoCard | 100.060.283 |
| 化学信息 | |
| 化学式 | C13H22N4O3S |
| 摩尔质量 | 314.40 g·mol−1 |
| 3D模型(JSmol) | |
| |
| |
注射剂常见副作用包含头痛以及灼热感,严重副作用则包含肝脏疾病、心跳过缓、肺炎,且可能使胃癌更不易发现[3]。本品也可能提升伪膜性结肠炎的风险[5]。妊娠期间给药目前显示安全。本品属于组织胺H2受体阻抗剂,可降低胃酸的分泌[3]。
雷尼替丁最早于1976年由葛兰素制药(Glaxo Pharmaceuticals)发现,现属于葛兰素史克的一部分[6][7]。本品列名于世界卫生组织基本药物标准清单之中,为基础公卫体系必备药物之一[8]雷尼替丁为一学名药。[3]。本品批发价每颗约位于0.01至0.05美金之间[9]。美国境内一剂约需0.05美金[3]。
临床应用
编辑在许多国家,特定剂量的雷尼替丁制剂是非处方药品。
美国以外,雷尼替丁常与铋(作为一个温和的抗生素)合成的柠檬酸盐(雷尼替丁枸橼酸铋)用于治疗幽门螺杆菌感染。这一组合通常是与克拉霉素(一种抗生素)一起使用。
警告和注意事项
编辑美国食品药品监督管理局(FDA)得知,有些雷尼替丁药物(包括商品名为Zantac的药物)中含有低剂量的 N-亚硝基二甲胺(NDMA)。NDMA分类为可能的人类致癌物[10]。加拿大的卫生单位也发表声明,指出他们在雷尼替丁中检测到NDMA[11],并且要求制造商停止在加拿大贩售雷尼替丁药物,直至产品中的NDMA浓度在安全范围内才能再次贩售[12]。由于欧盟委员会的要求,欧盟药物管理局已在全欧盟审查含有雷尼替丁的药物[13][14]。中华民国卫生福利部食品药物署已要求含有雷尼替丁的药物,先进行预防性下架[15]。
山德士(Sandoz)公司已针对所有含有雷尼替丁的药物提出“预防性下架”(precautionary distribution stop)[16][17]。
历史
编辑史克公司(Smith, Kline & French)发明了第一种组胺H2受体拮抗剂西咪替丁。葛兰素公司(Glaxo)为了与史克公司竞争,发明了雷尼替丁。雷尼替丁是合理化药物设计的产物,是根据当时相当完善的组胺H2受体模型和定量构效关系(QSAR)设计的。
葛兰素公司进一步完善了这个模型。他们用一个呋喃环取代了西咪替丁上的咪唑环,这使得雷尼替丁大为发展,有更好的耐受性,更少的不良反应,更长的作用时间,以及10倍于西咪替丁的活性。因为雷尼替丁对于细胞色素P450的亲和力只有西咪替丁的10%,所以其副作用较少,但其他的H2受体拮抗剂如法莫替丁和尼扎替丁则与细胞色素P450没有明显的活性。[18]
雷尼替丁出现于1981年,并于1988年称为世界上销售最多的处方药。但是当更有效的质子泵抑制剂出现后,他已经逐渐被奥美拉唑等药物所取代。
参考文献
编辑- ^ 中华药典第六版 页1304
- ^ 佳得胃10公絲注射液(雷尼得定)可能會有的適應症住院病人伴隨有病理性胃酸分泌過高之症狀,頑固性(難治的)十二指腸潰瘍或不能口服之病人消化性潰瘍之短期替代療法,以及相關成分和詳細資料 | 早安健康. www.edh.tw. [2022-07-04]. (原始内容存档于2022-07-05) (中文(台湾)).
- ^ 3.0 3.1 3.2 3.3 3.4 3.5 Ranitidine. The American Society of Health-System Pharmacists. [Dec 1, 2015]. (原始内容存档于2017-05-01).
- ^ Fedorowicz, Z; van Zuuren, EJ; Hu, N. Histamine H2-receptor antagonists for urticaria.. The Cochrane database of systematic reviews. 14 March 2012, 3: CD008596. PMID 22419335.
- ^ Tleyjeh, IM; Abdulhak, AB; Riaz, M; Garbati, MA; Al-Tannir, M; Alasmari, FA; Alghamdi, M; Khan, AR; Erwin, PJ; Sutton, AJ; Baddour, LM. The association between histamine 2 receptor antagonist use and Clostridium difficile infection: a systematic review and meta-analysis.. PloS one. 2013, 8 (3): e56498. PMID 23469173.
- ^ Fischer, Janos. Analogue-based Drug Discovery II. John Wiley & Sons. 2010: 4 [2017-03-15]. ISBN 9783527632121. (原始内容存档于2016-03-05).
- ^ Hara, Takuji. Innovation in the pharmaceutical industry the process of drug discovery and development. Cheltenham, U.K.: Edward Elgar. 2003: 94 [2017-03-15]. ISBN 9781843765660. (原始内容存档于2016-03-05).
- ^ WHO Model List of EssentialMedicines (PDF). World Health Organization. October 2013 [22 April 2014]. (原始内容存档 (PDF)于2014-04-23).
- ^ Ranitidine. International Drug Price Indicator Guide. [2015-12-01]. (原始内容存档于2017年5月10日).
- ^ Statement alerting patients and health care professionals of NDMA found in samples of ranitidine. Food and Drug Administration (FDA). 2019-09-13 [2019-09-15]. (原始内容存档于2019-09-26). 本文含有此来源中属于公有领域的内容。
- ^ Recalls and safety alerts. Health Canada assessing NDMA in ranitidine. 13 September 2019 [2019-09-19]. (原始内容存档于2019-09-19).
- ^ Health Canada requests that companies stop distributing ranitidine drugs in Canada while it assesses NDMA; some products being recalled - Recalls and safety alerts. Health Canada. 2019-09-17 [2019-09-19]. (原始内容存档于2019-09-19).
- ^ EMA to provide guidance on avoiding nitrosamines in human medicines. European Medicines Agency (EMA) (新闻稿). 2019-09-13 [2019-09-19]. (原始内容存档于2019-12-31).
- ^ EMA to review ranitidine medicines following detection of NDMA. European Medicines Agency (EMA) (新闻稿). 2019-09-13 [2019-09-19]. (原始内容存档于2020-02-13).
- ^ 中华民国卫生福利部食品药物管理署. 食藥署要求全面預防性下架含ranitidine成分藥品,經檢驗確認合格後,始得重新上架。. 2019-09-20 [2019-09-21]. (原始内容存档于2020-10-20) (中文).
- ^ Bomey, Nathan. Ranitidine warnings: Generic Zantac distribution halted on cancer fear. USA Today. September 19, 2019 [2019-09-20]. (原始内容存档于2019-09-20).
- ^ Palmer, Eric. Novartis doesn't wait for FDA investigation and halts distribution of its generic Zantac. FiercePharma. 2019-09-19 [2019-09-20]. (原始内容存档于2019-09-20).
Novartis on Wednesday said it was stopping worldwide distribution of its generic versions of the antacid while regulators investigate the fact that the impurity N-nitrosodimethylamine (NDMA) has been detected these ranitidine-based drugs.
- ^ Goodman and Gilman's page 972 11th addition